
某化学兴趣小组为了测定某稀硫酸的溶质质量分数,取100g稀硫酸于烧杯中,向烧杯中逐滴滴入质量分数为10%的氢氧化钠溶液,反应过程中所得溶液的酸碱度变化如图:
(1)当加入氢氧化钠溶液的质量为a g时,所得溶液中的溶质是 (填化学式);
当加入氢氧化钠溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
(2)稀硫酸的溶质质量分数是多少?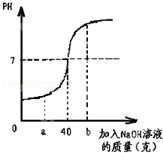
(1)H2SO4、Na2SO4;红; (2)4.9%
解析试题分析:(1)根据图示中关于反应进行时pH的变化情况分析可知:当加入氢氧化钠溶液的质量为a g时溶液的pH小于7,溶液显酸性说明此时硫酸有剩余,所以溶质中含有剩余的硫酸和氢氧化钠与稀硫酸反应生成的硫酸钠;当加入氢氧化钠溶液的质量为b g时,溶液的pH大于7,该溶液呈碱性,所以该溶液能使酚酞试液变红。
(2)依据加入氢氧化钠40g时溶液的pH等于7,说明此时氢氧化钠和稀硫酸恰好反应,据此依据化学方程式的计算求解即可。由图象可知当加入氢氧化钠溶液40g时反应恰好进行;
设稀硫酸的溶质质量分数为x
H2SO4+2NaOH=2H2O+Na2SO4
98 80
100x 40g×10%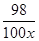 =
=
解得x=4.9%
考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算


 优等生题库系列答案
优等生题库系列答案科目:初中化学 来源: 题型:计算题
实验室中有一包含有少量氧化铜的铜粉.同学们欲测定这包铜粉中单质铜的质量分数.现称取20g样品放入烧杯中,逐滴滴入质量分数为10%的稀硫酸至固体不再减少,共用稀硫酸49g.试计算:这包含有少量氧化铜的铜粉中单质铜的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
现有Cu与另一种金属(可能是Mg、Fe、Zn中的一种)形成的粉末。现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70.0 | 70.0 | 70.0 | 70.0 |
| 剩余固体质量/g | 13.6 | 11.2 | 8.8 | 8.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
如图是已破损的维生素C(简写Vc,)其化学式:C6H8OX,的说明书部分信息。已知维生素C由碳、氢、氧三种元素组成。请回答:
(1)Vc中碳、氢元素的质量比为 ;
(2)Vc的化学式为 ;
(3)小辉妈妈每天服用该Vc片剂,小辉建议妈妈可食用西红柿来代替Vc片,若100g[西红柿含Vc30mg,则小辉妈妈每天食用西红柿 g即可达到服用上述Vc片的效果。
(4)最近根据市场调查发现不合格奶粉有所抬头。根据标准,合格奶粉每100克中含蛋白质约18克,蛋白质中氮元素的平均质量分数为16%,现测定某奶粉每100克中含有氮元素的质量为2.5克。则这种奶粉是否为“合格”奶粉?(列出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合.加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其它杂质不与盐酸反应)。试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取40克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸18.25克,求废水中氢氧化钾的质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(9分)盐酸和氯化坝的混合溶液40g,其中盐酸的溶质质量分数为10%.向混合溶液中加入9%的硫酸溶液20g恰好完全反应.计算:
(1)生成沉淀的质量是多少克?
(2)反应后所得溶液中盐酸的质量分数.(计算结果精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
称取NaCl和BaCl2的固体混合物32、5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)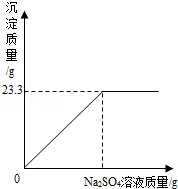
(1)完全反应后生成BaSO4沉淀 g.
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
2013年3月底,上海、浙江一带出现H7N9禽流感.这种病毒首先在鸡、鸭等飞禽身上发现.对鸡、鸭舍进行消毒时常用15%的过氧乙酸溶液,过氧乙酸的化学式是CH3COOOH(即:C2H4O3).试计算:
(1)一个过氧乙酸分子中有 个原子.
(2)过氧乙酸中碳、氢、氧元素的质量比 .
(3)配制15%的过氧乙酸溶液100克,需过氧乙酸 克,水 mL.(ρ水=1g/cm3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com