
如图是已破损的维生素C(简写Vc,)其化学式:C6H8OX,的说明书部分信息。已知维生素C由碳、氢、氧三种元素组成。请回答:
(1)Vc中碳、氢元素的质量比为 ;
(2)Vc的化学式为 ;
(3)小辉妈妈每天服用该Vc片剂,小辉建议妈妈可食用西红柿来代替Vc片,若100g[西红柿含Vc30mg,则小辉妈妈每天食用西红柿 g即可达到服用上述Vc片的效果。
(4)最近根据市场调查发现不合格奶粉有所抬头。根据标准,合格奶粉每100克中含蛋白质约18克,蛋白质中氮元素的平均质量分数为16%,现测定某奶粉每100克中含有氮元素的质量为2.5克。则这种奶粉是否为“合格”奶粉?(列出计算过程)
(1)72:8(或9:1) (2分) (2)C6H8O6(2分) (3)200(2分)
(4分)(4)解:因为每100克中含有氮元素的质量为2.5克。(1分)
所以蛋白质的质量=2.5克÷16℅ (1分) =15.625克<18克(不合格)(2分)
解析试题分析:(1)碳氢的质量比为:(12*6):(1*8)=72:8=9:1;(2)根据维C的相对分子质量为176,设氧的原子个数为x,则12*6+1*8+16*x=176,x=6,故化学式为C6H8O6;(3)一日3次,每次2片,故一天吃6片,故一天所补充的维C为10mg*6=60mg;设需要吃西红柿的质量为x,则(30mg/100g)*x=60mg,x=200g;(4)元素的质量除以元素的质量分数等于物质的质量。
考点:化学式的计算


科目:初中化学 来源: 题型:计算题
一化学小组为了测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.称取该铜矿样品30g于烧杯中,逐滴滴入质量分数为10%的稀盐酸至刚好完全反应,共用去稀盐酸146g.(假设铜矿中的杂质不与稀盐酸反应,也不溶于水)
试求:
(1)稀盐酸中HCl的质量是多少克?
(2)铜矿中碱式碳酸铜的质量是多少克?其质量分数是多少?
(3)反应后所得氯化铜溶液中溶质的质量分数是多少?
(反应的化学方程式为:Cu2(OH)2CO3+4HCl═2CuCl2+CO2↑+3H2O.反应中各物质的相对分子质量:Cu2(OH)2CO3~222
HCl~36.5 CuCl2~135 CO2~44 H2O~18)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
工业上,高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳。现有100吨石灰石,煅烧一段时间后,质量变为78吨。
则(1)制得二氧化碳多少吨?
(2)石灰石中CaCO3的质量分数为多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。现取8g石灰石样品与足量的50g稀盐酸完全反应后,称得容器内的物质总质量为55.36g。
试回答下列问题:
(1)反应后容器内的物质有 。
(2)反应产生二氧化碳的质量为 。
(3)该石灰石样品中碳酸钙的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004。牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。右图是某乳业公司纯牛奶包装标签的部分文字。请仔细阅读后回答下列问题:
(1)包装标签上脂肪≥3.3g,是指100mL牛奶中含脂肪的质量至少3.3g.那么一盒牛奶含钙至少 g(保留到0.01g);
(2)求羟基磷酸钙中钙元素的质量分数(保留为0.1%);
(3)若人体每天至少需要0.6g钙,且这些钙有90%来自牛奶,则一个人每天至少要喝多少盒牛奶?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.
(1)向含有Vc的溶液中滴加紫色石蕊,溶液变红,说明Vc具有的性质是 .
(2)食品中的Vc被氧气氧化时,其含量的变化如图所示,由此可得出的结论有 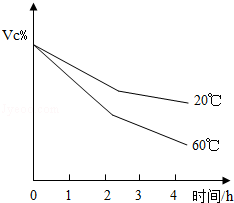
(3)小杰对某果汁饮料中Vc的含量进行测定.反应原理为C6H8O6+I2=C6H6O6+2HI,其中碘元素在反应中的 化合价变化是 .实验时取果汁饮料10mL,用煮 沸并冷却的蒸馏水稀释至50mL,向其中逐滴加入稀碘水至恰好完全反应,测得消耗碘(I2)的质量为25.4mg.则每100mL该果汁饮料中含Vc的质量是 .
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某化学兴趣小组为了测定某稀硫酸的溶质质量分数,取100g稀硫酸于烧杯中,向烧杯中逐滴滴入质量分数为10%的氢氧化钠溶液,反应过程中所得溶液的酸碱度变化如图:
(1)当加入氢氧化钠溶液的质量为a g时,所得溶液中的溶质是 (填化学式);
当加入氢氧化钠溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
(2)稀硫酸的溶质质量分数是多少?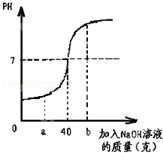
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示。
(1)反应完全后产生氧气的质量为
(2)欲从反应后的混合物中回收二氧化锰,应进行的操作是 、干燥。
(3)计算该过氧化氢溶液中溶质的质量分数(结果保留至0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将8.1g氧化锌固体放入100g稀硫酸中,恰好完全反应.试计算:
①可生成硫酸锌多少克?
②所用稀硫酸的溶质质量分数是多少?(化学方程式:ZnO+H2SO4=ZnSO4+H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com