
【题目】下图中图1是t ℃时相同质量的甲、乙两物质同时放入100 g水中的溶解情况,图2是它们的溶解度曲线图,下列说法不正确的是( )
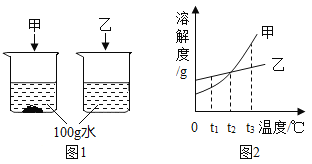
A.t2℃时,甲、乙两物质的溶解度相等
B.t2 >t> t1
C.若使图1中的甲全部溶解,可采用升高温度的办法
D.将t2℃时两物质的饱和溶液降低到t1℃时均有晶体析出
科目:初中化学 来源: 题型:
【题目】近日,卫生部等五部委日前下发联合公告,将三聚氰胺限量值标准从乳制品扩展到整个食品中,我国食品中三聚氰胺的标准得到统一,公告规定婴儿配方食品中三聚氰胺的限量值为1mg/kg,其他食品中三聚氰胺的限量值为2.5mg/kg。则回答
(1)三聚氰胺(C3H6N6)中C元素的化合价为+4价,则N元素的化合价是___。为安全起见,一般采用三聚氰胺制造的食具都会标明“不可放进微波炉使用”。试解释原因_______。
(2)“凯式定氮法”是通过测奶品中含氮量来折算奶品中蛋白质含量的一种方法。不法分子为了提高氮的含量,向1Kg牛奶中添加2.52g三聚氰胺添加进奶品中冒充蛋白质,则冒充蛋白质的质量(已知蛋白质中所含氮元素的质量分数约为16%)为(____)
A 2.52g B 4.44g C 10.5g D 12.32g
(3)三聚氰胺被称为冒充蛋白质的“蛋白精”,含三聚氰胺的毒奶粉需要进行焚烧方法处理,焚烧时烟尘经过滤后排入空气中,燃烧时生成三种物质,其中一种物质在空气中含量最多,则相关的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体(不含结晶水)的溶解度曲线如图所示,有关分析正确的是( )
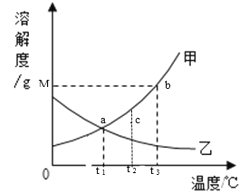
A. a对应的甲、乙两种溶液,溶质的质量相等
B. t3℃时,甲、乙两种饱和溶液中,溶质的质量甲>乙
C. t2℃时,c点所对应两种溶液的溶质质量分数甲>乙
D. 将t3℃时,甲、乙两种不饱和溶液、降温到t1℃后,都能变为饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,
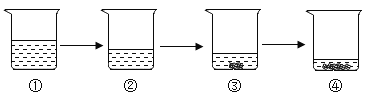
可以作出的正确判断是( )
A.在①→②过程中,氯化钠的质量分数保持不变
B.在②→③过程中,氯化钠的溶解度不断增大
C.在③→④过程中,水的质量分数不断增大
D.在②→④过程中,氯化钠的质量分数先不变后增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国多地纷纷出台学校塑胶跑道新标准,最重要的变化是还引入了一个挥发物质总量检测的概念,以防止标准外的有害物质蒙混过关。二甲苯是一种传统的有害挥发物质,化学式为C8H10。请通过计算回答:
(1)二甲苯由___种元素组成,每个二甲苯分子中原子总数为_____。
(2)二甲苯中碳、氢元素的质量最简比为_____。
(3)二甲苯中氢元素的质量分数为_____(计算结果保留0.1%)。
(4)若检测某不合格塑胶中含有21.2mg二甲苯,其中含____mg碳元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学与人类生活息息相关。请回答下列问题。
(1)炒菜时油锅中的油不慎着火,用锅盖将其盖灭的原理是________。
(2)油炸食物不宜多吃,因长时间煎炸会产生有毒物质丙烯醛(C3H4O).丙烯醛在空气中完全燃烧时,生成二氧化碳和水,请写出丙烯醛完全燃烧的化学方程式____________。
(3)青少年处于生长发育期,为预防患佝偻病,可以多吃奶制品、虾皮等食物,补充人体需要的_________元素。
(4)生活中将硬水转化为软水常用的方法是________。
(5)南昌“藜蒿炒腊肉”风味独特,清香扑鼻。从分子角度解释“清香扑鼻”的原因是_______
(6)海水通常浑浊也含有很多杂质,要使海水成为饮用水,需要采取的操作方法是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从Ca、C、H、O、Fe、Cl、N七种元素中选择适当的元素按要求填空:(用化学用语填空)
①2个氧分子______ 。
②n个碳酸根离子_______ 。
③氯化亚铁中铁显正2价_____。
④充入食品包装袋中的防腐的单质是______。
⑤家中白酒的主要成分是_____。
⑥能用于改良酸性土壤的氧化物是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是一种重要的化工原料,也是实验室中常用的化学试剂,下面是对硫酸 的组成、性质、制取等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的组成
(1)在溶液中解离出的阳离子全部是氢离子的物质统称为酸,检验硫酸中的阴 离子可选择的试剂为_____。
(探究二)硫酸的性质
(2)浓硫酸的特性:用小木棍蘸取少量浓硫酸,放置一会后,可观察到_____。
(3)浓硫酸的稀释:实验室用 98%的浓硫酸配制 100 g 溶质质量分数为 20%的 稀硫酸,应加水的质量为_____g(结果精确到 0.1 g)。
(4)稀硫酸的化学性质:如图为某同学进行的相关实验:
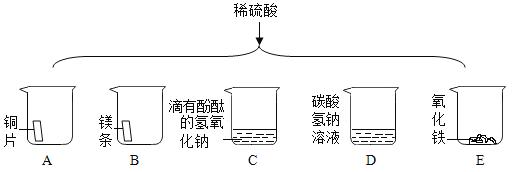
①有气泡产生的是_____(填字母序号)。
②写出烧杯 C 中发生反应的化学方程式_____。
(探究三)硫酸的工业制法
工业上以黄铁矿(主要成分为 FeS2)为原料生产硫酸的工艺流程如图所示:
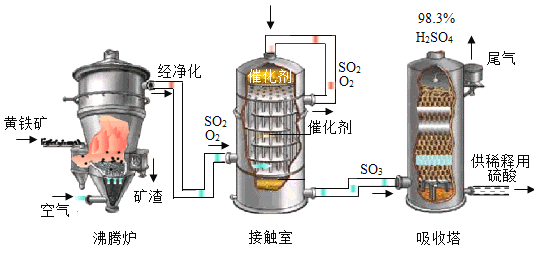
(5)黄铁矿在加入沸腾炉前要进行粉碎,其目的是_____ 。
(6)接触室中发生反应的化学方程式为_____。
(7)依据生产硫酸的工艺流程图,下列说法中正确的是_____ (填字母序号)。
A 吸收塔中得到的产品为混合物
B 催化剂能够加快 SO2 的反应速率和增大 SO3 的产量
C 沸腾炉排出的矿渣可供炼铁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上采用离子交换膜电解槽电解饱和食盐水,可得到高浓度的烧碱溶液(含NaOH 35%~48%),某兴趣小组欲验证一化工厂生产的NaOH溶液是否达到了高浓度标准,进行了如下操作,请你参与计算:
(1)用37%的浓盐酸配制200g7.3%的盐酸,需要加水(密度为1gmL﹣1)_____mL.(计算结果保留一位小数)
(2)采集该化工厂电解槽中的NaOH溶液20g,向其中滴入所配制的盐酸,当溶液的pH=7时,消耗盐酸100g,判断电解槽中NaOH溶液是否达到高浓度标准_________。(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com