
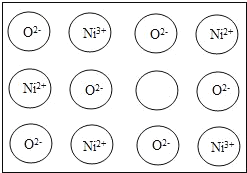
【题目】天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值都发生了变化。某氧化镍样品组成为Ni0.97O,则该晶体中Ni3+与Ni2+的离子数之比为_____。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列关于燃烧现象的解释或分析正确的是( )
A. 中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B. 中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C.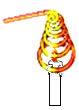 中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D.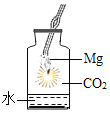 中镁条剧烈燃烧的现象可知,燃烧不一定需要氧气
中镁条剧烈燃烧的现象可知,燃烧不一定需要氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究某稀盐酸中溶质的质量分数,甲、乙两同学分别取溶质质量分数相等的稀盐酸100g,甲同学向其中加入氧化铜8g,反应结束后观察到固体全部消失;乙同学向其中加入氧化铜16g,反应结束后观察到固体有剩余。下列有关实验的推断不正确的是( )
A.反应后乙同学所得溶液中一定不含盐酸
B.反应后向甲同学所得的溶液中滴加过量氢氧化钠溶液,一定会有蓝色沉淀生成
C.反应后甲、乙两同学所得的溶液中溶质的质量分数不一定相等
D.原稀盐酸中溶质的质量一定大于7.3克小于14.6克
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢化钙固体是登山运动员常用的能源提供剂。某兴趣小组拟选用如下装置制备氢化钙。(提示:氢化钙通常用氢气与钙加热制得,金属钙的化学性质很活泼,容易与氧气、水反应。)
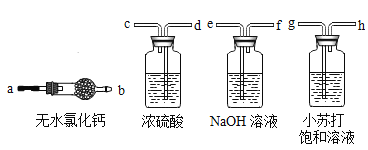
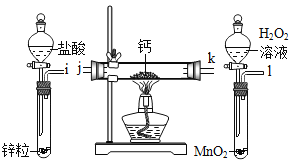
请回答下列问题:
(1)氢化钙属于离子化合物,其阴离子符号为_____。
(2)请选择必要的装置,按气流方向连接顺序为_____→a(填仪器接口的字母编号)。
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;_____(请按正确的顺序填入下列步骤的标号)。
A 加热反应一段时间
B 收集气体并检验其纯度
C 关闭分液漏斗活塞
D 停止加热,充分冷却
(4)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色。该同学据此判断,上述实验确有CaH2生成。
①写出CaH2与水反应的化学方程式_____;
②该同学的判断不准确,原因是_____。
(5)通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
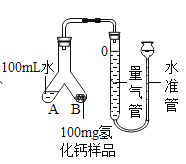
①检查装置气密性,装入药品,按图(固定装置省略)所示连接仪器。
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0mL。
回答下列问题:
(5)如何判断样品与水完全反应:_____。
(6)反应生成氢气的体积为_____mL。
(7)已知该实验条件下,氢气的密度为0.09mg/mL。样品中氢化钙的纯度为_____。(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向20g某赤铁矿石(主要成分是Fe2O3,假设杂质不溶于水,也不与酸反应)样品中,逐渐加入稀硫酸,充分反应。实验相关数据如图所示。
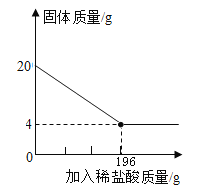
(1)20g赤铁矿石样品中氧化铁的质量为______g
(2)计算试验中所用稀硫酸溶质的质量分数(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)下列有关说法不正确的是( )
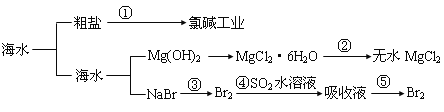
A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能的过程
B.过程②中结晶出的 MgCl2·6H2O 要在 HCl 氛围中加热脱水制得无水 MgCl2
C.在过程③⑤中溴元素均被氧化
D.过程①中除去粗盐中的 SO42- 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH 溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中甲、乙分别表示两种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法正确的是( )
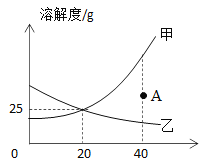
A.图中A点表示甲、乙两种物质在40℃时均达到饱和
B.甲、乙两种饱和溶液,当温度从40℃降至20℃时,一定析出相同质量的晶体
C.将40℃等质量的甲、乙两种饱和溶液降温至20℃后,剩余溶液中的溶剂的质量关系为甲小于乙
D.0℃时,甲、乙具有相同的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四种操作(或治疗)过程,其中正确的是( )
A. 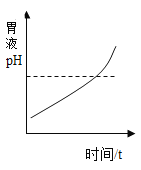 用胃舒平主要成分[主要成分Al(OH)3]治疗胃酸过多时pH变化情况
用胃舒平主要成分[主要成分Al(OH)3]治疗胃酸过多时pH变化情况
B. 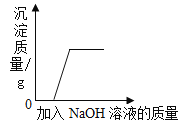 向氯化铁溶液中加入氢氧化钠溶液直至过量
向氯化铁溶液中加入氢氧化钠溶液直至过量
C. 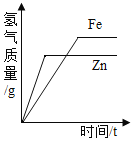 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
D. 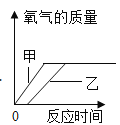 用过氧化氢分解制取氧气:加入二氧化锰(甲)与单独加热(乙)生成氧气的质量
用过氧化氢分解制取氧气:加入二氧化锰(甲)与单独加热(乙)生成氧气的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黑枸杞富含花青素,享有“花青素之王”的美誉。某小组对黑枸杞提取液进行了探究。
I.探究黑枸杞提取液能否充当酸碱指示剂。
(查阅资料)花青素易溶于水,溶液呈紫色。
(实验准备)将3.0 g黑枸杞粉放入30 mL蒸馏水中,充分溶解后制得黑枸杞提取液。
(进行实验)
实验1-1:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
颜色 | 粉红 | 粉红 | 粉红 | 浅紫 | 浅紫 | 紫 | 紫 | 蓝 | 蓝 | 深蓝 | 深蓝 | 灰绿 | 黄 | 黄棕 |
实验1-2:室温时,向试管中分别加入相同体积的6种物质,各滴3滴黑枸杞提取液。实验结果如下:
物质 | 白醋 | 稀盐酸 | 牛奶 | 蒸馏水 | 纯碱水 | 氢氧化钠溶液 |
颜色 | _____ | 粉红 | 紫 | 紫 | 灰绿 | 黄 |
(解释与结论)
(1)若白醋的pH为3,向白醋中滴加黑枸杞提取液后,颜色为______。
(2)根据实验现象,不能确定牛奶呈中性的理由是______。
(3)向纯碱水中加黑枸杞提取液,再滴入稀盐酸至过量,观察到的实验现象为______。
II.探究影响黑枸杞提取液中花青素稳定性的因素。
(查阅资料)利用花青素含量与吸光度大小呈正比的关系,可衡量花青素的含量进而判断花青素的稳定性。
(实验准备)在一定条件下配制出黑枸杞提取液备用。
(进行实验)
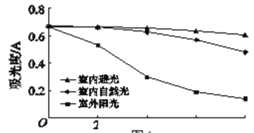
实验2-1:相同温度下,在3支试管中加入相同体积的黑枸杞提取液,分别放置在室内避光、室内自然光和室外阳光的条件下12小时(结果如图)。
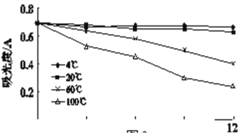
实验2-2:相同光照条件下,在4支试管中加入相同体积的黑枸杞提取液,分别放置在4 ℃、20 ℃、60 ℃、100 ℃的条件下12小时(结果如图)。
(解释与结论)
(4)实验2-1的目的是______。
(5)实验2-2的结论是______。
(反思与评价)
(6)由实验可知,黑枸杞提取液能充当酸碱指示剂,但在保存时应注意______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com