
����Ŀ����һ�ձ���ʢ��42.2gCaCO3��CaCl2�ķ�ĩ״����������264.6gˮ��ʹ������еĿ�������ȫ�ܽ⡣Ȼ������������μ������ʵ���������Ϊ10%��ϡ���ᣬ�ձ������ܹ������ʵ�������������ϡ�����������ϵ������ͼ��ʾ�����������ش��������⣺

���ڵ���ϡ����Ĺ����У��۲쵽�����������ǣ�
��_______________________
��_______________________
�Ƶ�����10%��ϡ������ͼ��A��ʱ���ձ�����Һ�ﺬ�е������ǣ�д��ѧʽ��______________��
�ǵ�����10%��ϡ����146gʱ����B�㣩����ͨ�����㣬���ʱ�ձ������ò�������Һ����������������______________
���𰸡� �������ʲ����ܽ� �������������������ð���� CaCl2 10%
�������� (1).̼��ƹ�����ϡ���ᷴӦ�������������CaCO3+2HCl=CaCl2+H2O+CO2����������10%��ϡ������ͼ��A��ʱ��ϡ����㣬�ձ�����Һ�ﺬ�е�������CaCl2 ���ǵ�����10%��ϡ����146gʱ����B�㣩��̼�����ϡ����ǡ�÷�Ӧ���跴Ӧ����̼��Ƶ�����Ϊx,�����Ȼ��Ƶ�����Ϊy�����ɶ�����̼������Ϊw
CaCO3 + 2HCl = CaCl2+ H2O+ CO2��
100 73 111 44
x 146g��10% y w
![]() =
= ![]() ���x=20g����������CaCl2 ��������42.2g-20g=22.2g
���x=20g����������CaCl2 ��������42.2g-20g=22.2g
![]() =
=![]() ���y=22.2g
���y=22.2g
![]() =
=![]() ��� w=8.8g
��� w=8.8g
�ձ������ò�������Һ������Ϊ��42.2g+264.6g+146g-8.8g= 444g�����ʵ�����Ϊ��22.2g+22.2g=44.4g�������ò�������Һ��������������Ϊ��![]() ��100%=10%
��100%=10%


 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӻ��������ĽǶȿ��ǣ�����ȼ������������ǣ� ��
A. ���� B. ���� C. ú D. ��Ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ǵ�һλ�ġ���Ϊ�Ѿ����ڷ����µ��Ҵ��ߣ������������Ѿ�Ȯ���Ѿ�Ȯ�ܸ������巢������ζ�����Ҵ��ߡ����۵ĽǶȷ����Ѿ�Ȯ�ܷ����Ҵ��ߵ���Ҫԭ����
A�����ӵ�������С
B����ͬ�������ʲ�ͬ
C�����Ӳ����˶�
D�����Ӽ��м��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ������֮Դ������Ӧ���˽�ˮ������ˮ��Դ������˵��������� �� ��
A. ��ˮ�ķ���ͨ���г��������ˡ�����������
B. ����ˮ������ClO2������ClO2����Ԫ�صĻ��ϼ�Ϊ+4
C. ͨ�����˵ķ������Խ�������ˮ�Ĺ���������ˮ���뿪��
D. ���ˮʱ�����������������������Ϊ1:2��������Ϊ1:8.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�Ͼɽ����к���ͭ����Au��������Ni��������Au���Ʊ�CuSO45H2O������������£�
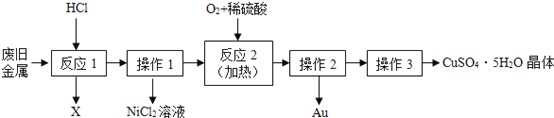
����˵����ȷ���ǣ� ��
A����Ӧ1��������ΪH2O
B������1�Ͳ���2�õ���������Ϊ©�����ձ��Ͳ�����
C�����ֽ����Ľ������˳��Ϊ��Cu��Ni��Au
D����Ӧ2�Ļ�ѧ����ʽΪ��2Cu+O2+2H2SO4![]() 2CuSO4+2H2O
2CuSO4+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�����ʡ�
��1���ҹ�ϡ����������������ǰ�У���ͼ���棨Ce����Ԫ�����ڱ��е���Ϣʾ��ͼ����ԭ�ӵ���������________��

��2��Ϊ�Ƚ��桢п�Ľ�����ԣ����������Լ�ʵ��һ�����е���____
A���桢����п��Һ B���桢п��ϡ���� C���桢п������ͭ��Һ
��3����ֹ������ʴ�ɽ�Լ������Դ����������ʴҪ����������������ϡ��������������⣬д���÷�Ӧ��ѧ����ʽ_______________________
��4��ͭ����һ�ֽ���M�Ļ���M������Al��Fe��Ag�����ڸû�����м���������ϡ���������ݲ�������M��������______������Ӧ��ɺ�______����ʵ��������������õ�ͭ����Һ������Һ�м���пƬ���������һ���ɫ���ʣ���M��________��ȡһ������ԭ�����Ͷ�뵽һ������AgNO3��Һ�У���ַ�Ӧ�Է�Ӧ������Һ�����ƶ���ȷ����_________��
A����Һ��һ����M������ B��������һ����Ag��Cu
C��������һ����Ag D����Һ��һ����Ag+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������д��ѧ����ʽ�������������ǣ�
A. �������ⶨ�����ɷ�ʱ�����õĻ�ѧ��Ӧ֮һ:2Hg+O2![]() 2HgO
2HgO
B. ���ú�����������ҩ������θ�����:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
C. �����ˮʵ��ʱ,�����Ļ�ѧ��Ӧ:2H2O![]() 2H2�� +O2��
2H2�� +O2��
D. ��Ȼ��¯����ʻ�ɫ���ҹ��׳��ֺ�ɫ:CH4+O2![]() C��+2H2O
C��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ӳ��ij��ѧ��Ӧ������������ʱ��Ĺ�ϵ������������ȷ����
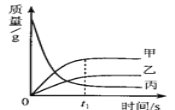
A���÷�Ӧ�ǻ��Ϸ�Ӧ
B������Է�������������
C�����Ƿ�Ӧ�������������
D��t1ʱ����������һ�����ڼס��ҵ�����֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����д�����з�Ӧ�Ļ�ѧ����ʽ�����ڣ�1������4������ע����Ӧ�������͡�
��1��˫��ˮ��������̻��________________________________��________��
��2������ȼ��_____________________________________________��
��3����ҵ����______________________________________________��
��4����ʯ������ˮ���ɼ�___________________________________ ��________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com