
【题目】为了从硝酸亚铁和硝酸银的混合溶液中,提取并回收银,小燕设计了如下的实验方案:
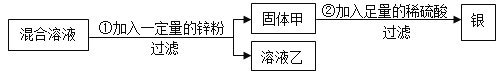
(1)若溶液乙为无色溶液,则固体甲一定含有的物质是_____,可能含有的物质是_____,写出一个在步骤①中肯定发生的反应的化学方程式_____。
(2)若溶液乙为浅绿色溶液,则溶液乙中溶质的组成可能是_____或_____(填物质的名称或化学式)。
【答案】铁、银 锌 Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag) Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2、AgNO3
【解析】
(1)在金属活动性顺序中,锌>铁>氢>银,在硝酸亚铁和硝酸银的混合溶液中,加入一定量的锌,锌先与硝酸银反应生成了硝酸锌和银,若硝酸银完全反应锌再与硝酸亚铁反应生成了硝酸锌和铁,乙为无色溶液,说明硝酸亚铁和硝酸银全部参加化学反应,锌能与硝酸亚铁反应生成硝酸锌和铁,能与硝酸银反应生成硝酸锌和银,故固体甲中含有铁和银,可能有剩余的锌,发生反应的方程式是:Zn+Fe(NO3)2═Zn(NO3)2+Fe、Zn+2AgNO3═Zn(NO3)2+2Ag;
(2)若溶液乙为浅绿色溶液,说明了溶液中含有硝酸亚铁,锌完全发生了反应,溶液中一定含有硝酸锌、硝酸亚铁,可能含有硝酸银。所以溶液乙中溶质的组成可能是Zn(NO3)2、Fe(NO3)2或Zn(NO3)2、Fe(NO3)2、AgNO3。
故答案为:(1)铁、银;锌;Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag)。
(2)Zn(NO3)2、Fe(NO3)2;Zn(NO3)2、Fe(NO3)2、AgNO3。


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:初中化学 来源: 题型:
【题目】请结合图示实验装置,回答下列问题。
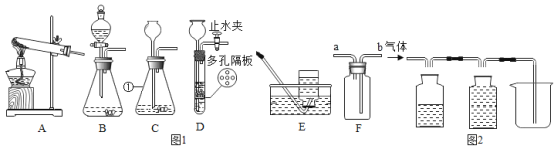
(1)写出标号①的仪器名称:______。
(2)实验室用纯净物加热制取氧气,应选择的发生装置是_____(选填序号),反应的化学方程式为_____。
(3)若选择D装置制取二氧化碳,在反应过程中,使反应停止的操作是______。
(4)若用E装置收集氧气,当导管口有气泡_____时才能将导管伸入集气瓶中。若用 F 装置收集二氧化碳,气体应从__端通入(选填“a”或“b”)。
(5)实验室用电石(固体,主要成分CaC2)和水反应制取乙炔(C2H2)气体,该反应极剧烈,为控制反应速率,发生装置应选____(填序号).用电石制得的乙炔气体中常混有酸性气体,为了得到较纯净的C2H2,可将气体通过氢氧化钠溶液后,用排水法收集,请在答卷图2将除杂及收集装置补画完整____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映其对应关系的是
A.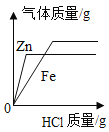 向装有等质量锌、铁的两只烧杯中分别加足量等浓度的稀盐酸
向装有等质量锌、铁的两只烧杯中分别加足量等浓度的稀盐酸
B.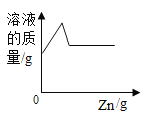 向硝酸银和硝酸铜混合溶液中加入过量的锌粉
向硝酸银和硝酸铜混合溶液中加入过量的锌粉
C. FeCl3和HCl混合液中加入NaOH溶液
FeCl3和HCl混合液中加入NaOH溶液
D.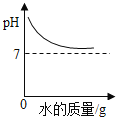 常温下向装有澄清石灰水的烧杯中逐渐加水
常温下向装有澄清石灰水的烧杯中逐渐加水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学为了测定CaCl2和NaCl的混合物中CaCl2的含量,他们取样品25.8g于烧杯中,加入134.2g水全部溶解,再多次加入某Na2CO3溶液充分反应。加入Na2CO3溶液 与产生沉淀的质量如下表所示:
Na2CO3溶液/g | 10 | 10 | 10 | 10 | 10 | 10 |
沉淀质量/g | 5 | 10 | 15 | 20 | 20 | m |
(1)Na2CO3中钠、碳、氧三种元素的质量比为_____,表中m=_____。
(2)样品中CaCl2的质量是____;恰好完全反应时,所得溶液中溶质的质量分数是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列化学反应化学方程式
(1)一氧化碳在空气中燃烧_____;
(2)氢氧化铜溶液与稀硫酸反应______________;
(3)用盐酸除铁锈_____;
(4)铝与硫酸铜溶液反应_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】X、Y两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
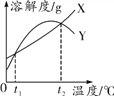
A. 溶剂不变时,t1℃ X的饱和溶液升温至t2℃仍是饱和溶液
B. 溶剂不变时,分别将t1℃ X、Y的饱和溶液升温至t2℃,所得溶液中溶质的质量分数相等
C. 相同温度时,X的溶解度一定大于Y的溶解度
D. Y的溶解度随温度的升高而增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向稀硫酸中加入Ba(OH)2溶液,溶质质量变化如图所示,下列说法不正确的是
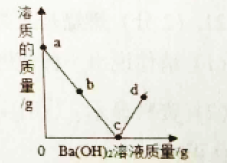
A.a点处溶液中只有一种溶质
B.b点处溶液中加入铁粉有气泡生成
C.c点处溶液中含较多Ba2+、OH-、SO42-、H+
D.d点处溶液中滴加酚酞溶液,溶液变红色
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组利用废烧碱(含少量Na2CO3、NaCl、MgCl2、CaCl2等)制Na2CO3·10H2O。
【制取流程】
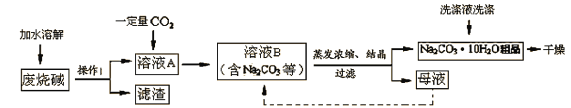
【相关资料】①Na2CO3+H2O+CO2=2NaHCO3
②2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
③在NaHCO3溶液中加入BaCl2溶液,可发生反应:2NaHCO3+BaCl2=BaCO3↓+2NaCl+ H2O+CO2↑
④碳酸钠的饱和溶液在不同温度下析出的晶体如下图所示:
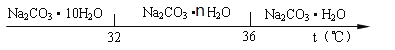
【问题讨论】
(1)滤渣主要成分为Mg(OH)2和 ,产生Mg(OH)2的化学方程式 。
(2)操作Ⅰ需使用的玻璃仪器有:烧杯、 和玻璃棒。
(3)取少量溶液B,加入BaCl2溶液,充分混合,若观察到 (填现象),则溶液B中含NaHCO3。
(4)结晶后,过滤时的温度须低于 ℃。
(5)“母液”不能沿流程中虚线路径循环使用,原因是 (选填序号)。
①“母液”不含Na2CO3
②“母液”多次循环后,NaCl含量增加
【组成确定】
(6)取少量粗产品,加水溶解,加足量 (选填数字序号,下同),充分搅拌,再加少量 ,无沉淀,证明其中不含NaCl。
①AgNO3溶液 ②稀盐酸 ③稀硝酸
(7)兴趣小组同学取32.8g干燥粗产品,用如图所示装置(夹持仪器省略)进行实验:
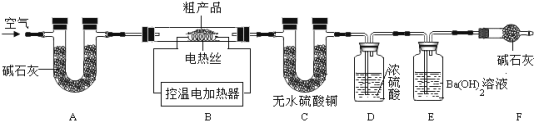
查阅资料1:Na2CO3·10H2O加热至32℃,开始分解失水,充分加热可完全失水;NaHCO350℃时开始分解270℃时完全分解;Na2CO3受热不分解。
查阅资料2:Ba(OH)2溶液能吸收CO2:Ba(OH)2+CO2=BaCO3↓+H2O
①实验前要先 ,再装入粗产品;
装置A的作用是 。
②粗产品加热至270℃,据 (填装置编号及现象),可知粗产品中含NaHCO3。测得C、D共增加m1,E质量增加m2,则m1∶m2 (填“>”、“=”或“<”)9∶22。
实验测得m2=1.1g,则可推算32.8g粗产品中含有NaHCO3的质量为 g。
③当加热至36℃时,测得B中剩余固体27.4g,则该剩余固体是 (填化学式)和NaHCO3的混合物。(此空2分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酱油在使用及储藏过程中颜色会变深,逐渐降低品质。实验小组通过实验研究温度、氧气、光照3个因素对酱油颜色的影响。
(查阅资料)① 通过色差仪检测L*值可监控酱油颜色变化,酱油颜色越深,L*值越小。
② 保鲜瓶具有的特点是挤出盛放的物质后,空气不会进入。
(实验准备)
将等量样品(同品牌、同批次、初始L*值为43.82的酱油)分装到500 mL的不同容器中,密封。
(进行实验)
实验1:将装有样品的多个透明玻璃瓶置于不同温度的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。
编号 | 温度 | 15天 | 30天 | 45天 |
1-1 | 5 ℃ | 43.77 | 43.53 | 42.91 |
1-2 | 28 ℃ | 43.71 | 43.19 | 42.85 |
1-3 | 45 ℃ | 43.67 | 42.55 | 40.89 |
实验2:将装有样品的两个容器置于28 ℃的恒温箱中。每15天,分别倒出100 mL酱油,剩余样品放回恒温箱。用色差仪检测倒出样品的L*值,结果如下。
编号 | 容器 | 15天 | 30天 | 45天 |
2-1 | 透明玻璃瓶 | 43.45 | 42.36 | 41.30 |
2-2 | 透明保鲜瓶 | 43.72 | 42.98 | 42.53 |
实验3:将装有样品的多个容器置于28 ℃的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。

(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2的目的是_____。
(3)实验3欲研究光照对酱油颜色的影响,应选用的容器是_____。
(4)家庭常使用透明玻璃瓶盛放酱油。解释“在相同时间内,使用过的酱油比未开封的酱油颜色深”可依据的实验是_____(填编号)。
(反思与评价)
(5)结合本实验,你对使用或储藏酱油的建议是_____。
(6)酱油在酿造过程中,有时会产生过量的铵盐(如NH4Cl)影响酱油的口感。可用碳酸钠除去铵盐,原理如下,补全该反应的化学方程式。Na2CO3 + 2NH4Cl === 2NaCl + 2NH3↑ + H2O +_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com