
【题目】我们生活在一个丰富多彩的物质世界。
(1)请从C、H、O、Na、Ca五种元素中选择一种或几种元素,写出符合下列要求的化学用语。
① 人体中最多的物质 ___________; ② 改良酸性土壤的碱_______________;
③ 最简单的有机物______________; ④ 汽水中含有的酸 _______________。
(2)日常生活与化学息息相关。 “3·15”晚会科研人员模拟人体内部环境,使用西红柿和蟹肉进行实验,发现蟹肉中微量的有机砷(C3H11AsO2)没有转化为有毒的砒霜(As2O3),证实“食物相克:西红柿和螃蟹一起吃会产生砒霜”是谣言。
①写出As2O3中砷元素的化合价__________。
②若有机砷转化为砒霜,该转化属于__________(填“物理变化”或“化学变化”)。
③小明发现,妈妈炒菜时加一点酒和醋能使菜味香可口。查阅资料,发现原来酒和醋发生了化学反应,生成了一种有芳香气味的物质。该反应的方程式类似于C3H7COOH + CH3OH![]() C3H7COOCH3 + H2O,请仿写出乙醇与醋酸反应的化学方程式___。
C3H7COOCH3 + H2O,请仿写出乙醇与醋酸反应的化学方程式___。
【答案】H2O Ca(OH)2 CH4 H2CO3 ![]() 化学变化 CH3COOH + C2H5OH
化学变化 CH3COOH + C2H5OH![]() CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
【解析】
(1)①人体中最多的物质是水,化学式H2O; ② 改良酸性土壤的碱是氢氧化钙,化学式Ca(OH)2;③最简单的有机物甲烷,化学式CH4; ④ 汽水中含有的酸是碳酸,化学式为H2CO3,故填:H2O Ca(OH)2 CH4 H2CO3;
(2)①As2O3中砷元素的化合价为x,因为氧元素显-2价,所以2x+(-2)×3=0,x=+3价,故填:![]() ;
;
②若有机砷转化为砒霜,由于有新物质的生成,所以该转化属于化学变化,故填:化学变化;
③乙醇与醋酸反应的化学方程式CH3COOH + C2H5OH![]() CH3COOC2H5 + H2O,故填:CH3COOH + C2H5OH
CH3COOC2H5 + H2O,故填:CH3COOH + C2H5OH![]() CH3COOC2H5 + H2O。
CH3COOC2H5 + H2O。


科目:初中化学 来源: 题型:
【题目】盐城悦达汽车以其优良的性价比得到了越来越多消费者的喜爱.
(1)汽车电路中导线是金属铜,是利用了铜的_____性.
(2)汽车外壳主要是钢,钢的硬度_____纯铁,钢的熔点_____纯铁(填“>”“<”“=”).
(3)关于乙醇汽油的下列说法中不正确的是_____(填序号).
A使用乙醇汽油可减少大气污染 B乙醇可以用粮食发酵而成
C使用乙醇汽油可以明显减少温室效应 D使用乙醇汽油可节省石油资源
(4)全世界每年因生锈损失的钢铁,约占世界年产量的四分之一。
某学生想探究铁生锈是否必须同时有空气和水,他将干净的铁钉放入A、B、C三支干净的试管中,再各加入某些物质或用品进行研究。
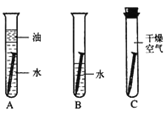
①一周后,编号为_____的试管中铁钉明显生锈,说明铁与_____和_____反应生成了铁锈。
②比较吐鲁番盆地和海南岛两地,铁生锈相对较慢的地区是_____,理由是_____。
(5)现有银、铜、铁三种金属,某研究小组的同学为探究银、铜、铁的金属活动性顺序,设计了三个实验:
Ⅰ.将铁片浸入稀硫酸中;Ⅱ.将银片浸入稀硫酸中;Ⅲ.将铁片浸入硫酸铜溶液中。
①实验Ⅰ的现象是:有气泡产生,溶液由无色逐渐变为浅绿色。反应的化学方程式为_____;反应产生的气体可用_____的方法检验。
②上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象):_____。
根据以上探究,三种金属的活动性由强到弱的顺序是_____。
③将银、铁两种金属分别放入_____溶液中,即可验证这三种金属的活动性强弱。
(6)100吨含氧化铁80%的赤铁矿可炼得含杂质4%的生铁多少吨?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
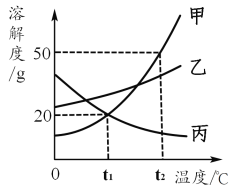
(1)气体的溶解度随温度变化的情况与______(填“甲”、“乙”或“丙”)相似。
(2)t2℃时,将65g甲固体加入到100g水中,充分溶解并恢复到原温度后,得到溶液的质量为________g。
(3)要使接近饱和的乙溶液变为饱和溶液,可采用的一种方法是________。
(4)若将t2℃时甲的饱和溶液降温到t1℃,则其溶液的溶质质量分数会________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性。现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X是( )
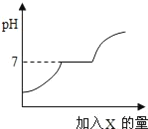
A. 水B. 澄清石灰水C. 纯碱溶液D. 稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件。现有一块50.00g黄铜样品,某同学利用一种未知浓度的稀盐酸来测定样品中Cu的质量分数。有关数据如图。问:
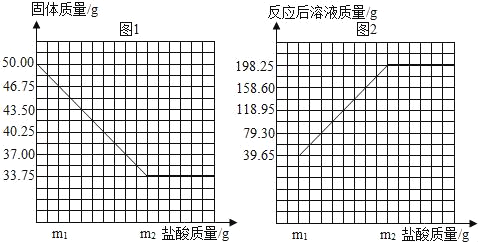
(1)黄铜中Cu的质量分数。
(2)样品完全反应产生的H2的质量。
(3)稀盐酸的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如下图所示,下列叙述正确的是( )
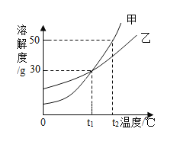
A. 甲和乙的溶解度相等且均为30g
B. 甲物质的溶解度随温度的升高而减小
C. t1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
D. 将t2℃甲的饱和溶液降温到t1℃,有固体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锌是促进人体生长发育的必须微量元素。下图为锌元素在元素周期表中的相关信息及原子结构示意图。下列说法正确的是( )
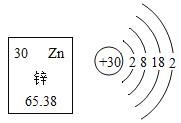
A. 锌属于非金属元素 B. 锌原子的中子数为30
C. 锌的相对原子质量为65.38g D. 锌原子在化学反应中易失去电子形成Zn2+
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硼及其化合物在工业上有很多用途。
(1)硼氢化钠(NaBH4)具有优良的还原性,在化学领域有着广泛的应用。利用硼精矿(主要成分为B2O3,含有少量Al2O3、SiO2、FeCl3等)制取NaBH4的流程如下图。
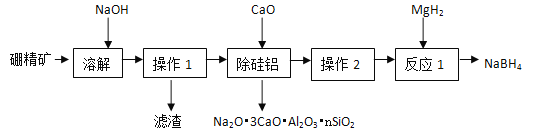
已知:①B2O3+2NaOH=2NaBO2+H2O;
②偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在;
③Al2O3、SiO2均可与NaOH溶液反应生成可溶性钠盐。
回答下列问题:
(1)①操作1是____,滤渣主要成分为______(填化学式)。
②写出加快硼精矿溶解速率的措施(写一种)_______。
③除硅铝步骤加入CaO而不加入氯化钙的原因有:_____
I.能将硅、铝以沉淀除去;II.。
(2)单质硼可用于生成具有优良抗冲击性能硼钢,以硼酸(H3BO3)和金属镁为原料可以制备单质硼(B)。其制备过程先后通过两个化学反应,写出相关化学方程式:
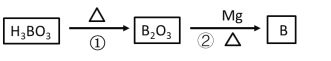
①分解反应____
②置换反应____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学发现实验台上整齐摆放的药品中(如图所示),有一试剂瓶的标签受损.
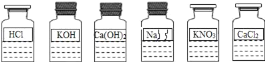
(提出问题)这瓶试剂的成分究竟是什么?
(讨论)根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是_____.
A 酸 B 碱 C 盐.
(猜想)①可能是NaOH溶液;②可能是Na2CO3溶液;③可能_____.
(设计并实验)
(1)小明用洁净干燥的玻璃棒蘸取该溶液到湿润的pH纸上,测得其pH=10,他判断这是一种碱性溶液.对他的操作方法、测量结果及结论的评价,正确的是_____.
A 方法正确,结果准确,且结论正确.
B 方法正确,结果偏小,但结论正确.
C 方法不正确,结果偏大,但结论不正确.
D 方法正确,结果准确,但结论不正确.
(2)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择如图所示已有的试剂就能鉴别出来.它们又进行了实验.
操作步骤 | 实验现象 | 结论及化学方程式 |
取样于试管中,_____ | _____ | _____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com