
【题目】镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体,细心的小明同学发现,镁条燃烧除生成白色固体外,还有少量的淡黄色固体生成,经查阅资料得知:淡黄色固体是由镁条和空气中的氮气化合产生的,写出该反应的化学方程式__,产生的白色固体比淡黄色固体多的原因是__。他还发现镁条在空气中久置表面会变黑,实验小组同学设计并进行实验,探究镁条变黑的条件。
[猜想假设]常温下,镁条变黑可能与O2、CO2、水蒸气有关。
[查阅资料]常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
[设计实验]通过控制与镁条接触的物质,利用右图装置(镁条长度为3cm,试管容积为20mL) ,分别进行下列5个实验,并持续观察20天。

实验操作 | 实验现象 |
1.先充满用NaOH浓溶液洗涤过的空气,再加人2mL浓硫酸 | 镁条始终无明显变化 |
2.加人NaOH浓溶液 | 镁条始终无明显变化 |
3.先加人2mL浓硫酸,再通入约4mLCO2 | 镁条始终无明显变化 |
4.先加入4mL饱和Na2SO3溶液,再充满CO2 | 镁条始终无明显变化 |
5.先加入2mL蒸馏水,再通入约4mL CO2 | 镁条第3天开始变黑,至第20天全部变黑 |
[解释与结论]①实验1的目的是_;②实验3中,试管内气体主要含CO2和__;③得出“镁条变黑一定与CO2有关”结论,依据的两个实验是___(填序号);④由上述实验可知,镁条变黑的条件是__。
[反思与评价]①在猜想假设时,同学们认为镁条变黑与N2无关,理由是_____;
②实验1和实验2中,NaOH浓溶液的作用是__;③欲进一步证明镁条表面的黑色物质中含有碳酸盐,你的实验方案是__。
【答案】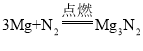 氧气的化学性质比氮气活泼 检验只用O2是否会使镁条变黑 O2(N2可不写) 2和5 镁条与空气中的O2、CO2、水蒸气同时作用 常温下氮气的化学性质不活泼,很难与其他物质反应 吸收空气中的CO2 取适量样品加入试管中,向试管中加入足量稀盐酸,并将产生的气体通入澄清的石灰水,若澄清石灰水变浑浊,则证明黑色物质中有碳酸盐。
氧气的化学性质比氮气活泼 检验只用O2是否会使镁条变黑 O2(N2可不写) 2和5 镁条与空气中的O2、CO2、水蒸气同时作用 常温下氮气的化学性质不活泼,很难与其他物质反应 吸收空气中的CO2 取适量样品加入试管中,向试管中加入足量稀盐酸,并将产生的气体通入澄清的石灰水,若澄清石灰水变浑浊,则证明黑色物质中有碳酸盐。
【解析】
镁条和空气中的氮气反应生成氮化镁,化学方程式为: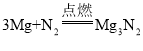 ;产生的白色固体比淡黄色固体多,说明镁和氧气更容易发生反应,氧气的化学性质比氮气更活泼;
;产生的白色固体比淡黄色固体多,说明镁和氧气更容易发生反应,氧气的化学性质比氮气更活泼;
实验1:用 NaOH浓溶液洗涤空气除去二氧化碳,再加人2mL浓硫酸吸收水蒸气,空气中只剩氮气和氧气,所以实验1的目的是检验镁条变黑是否与氧气有关;
实验2:只加入NaOH浓溶液除去空气中的二氧化碳,空气中还剩氮气、氧气和水蒸气,所以实验2的目的是检验镁条变黑是否与氧气和水蒸气有关;
实验3:先加入2mL浓硫酸吸收水蒸汽,再通入约4mLCO2,空气中还剩氮气、氧气和二氧化碳,所以实验3的目的是检验镁条变黑是否与氧气和二氧化碳有关;
实验4:先加入4mL饱和Na2SO3溶液除去氧气,再充满CO2,空气中还剩氮气、水蒸气和二氧化碳,所以实验4的目的是检验镁条变黑是否与水蒸气和二氧化碳有关;
实验5:先加入2mL蒸馏水,再通入约4mL CO2,空气中还剩氮气、氧气、水蒸气和二氧化碳,所以实验5的目的是检验镁条变黑是否与氧气、水蒸气和二氧化碳有关;
根据控制变量法分析,要得出“镁条变黑一定与CO2有关”结论,实验的唯一变量是有无二氧化碳,并且无二氧化碳的实验镁条不变黑,有二氧化碳的实验镁条变黑,所以符合条件的两个实验是实验2和实验5。
根据5个实验的实验现象可知,镁条变黑与氧气、水蒸气和二氧化碳都有关。
①在猜想假设时,同学们认为镁条变黑与N2无关,因为常温下氮气的化学性质不活泼,很难与其他物质反应;
②实验1和实验2中,NaOH浓溶液的作用是吸收空气中的二氧化碳;
③欲进一步证明镁条表面的黑色物质中含有碳酸盐,可以取适量样品加入试管中,向试管中加入足量稀盐酸,并将产生的气体通入澄清的石灰水,若澄清石灰水变浑浊,则证明黑色物质中有碳酸盐。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。
(1)如图所示是四种粒子的结构示意图。
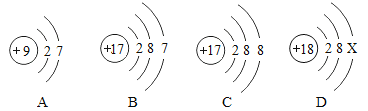
①D中的x=____________.C粒子的符号为=___________。
②A和B两种粒子的_________相同,所以它们具有相似的化学性质。
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图所示。
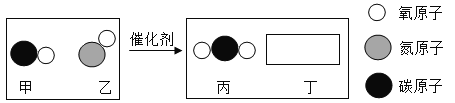
①已知丁是一种单质,则丁是_________(写化学式)。
②根据图示得出的结论中,正确的有_________(填字母)。
A 化学反应是原子的重组过程 B 该反应是置换反应
C 参加反应的甲和乙的质量比为14∶15 D 生成丙和丁的分子个数为1∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
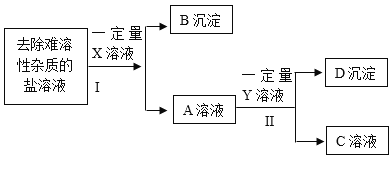
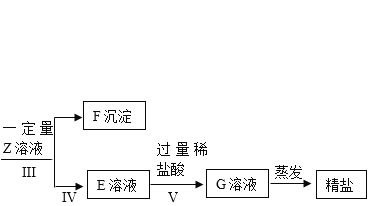
【题目】小明除去粗盐中不溶性杂质后,采用如下流程进一步除去粗盐中的可溶性杂质氯化镁、氯化钙、硫酸钠。在操作的过程中由于粗心,小明只确定所加入的X溶液是氯化钡溶液,而Y和Z溶液不确定分别是碳酸钠溶液和氢氯化钠溶液中的哪一种,且X. Y. Z所用的量也不确定。
请回答下列问题:
(1)加入X溶液后发生反应的化学方程式是_________________。
(2)小明取适量D沉淀于烧杯中加入足量的稀盐酸,观察到_________________,确定Y溶液是氢氧化钠溶液。
(3)小明为了确定粗盐中的可溶性杂质是否完全除干净以及所加入溶液是否还有剩余,对E溶液成分进行检验与分折,设计实验方案如下:
实验操作步骤 | 实验现象 | 实验结论 |
步骤一:取少量E溶液于试管中加入足量氯化钡溶液,过滤,向沉淀中加入过量稀硝酸 | 产生白色沉淀; 沉淀部分溶解 | 证明 E溶液中含有的物质是 ① _____________,没有的是 ②____________ |
步骤二:向步骤一反应后所得滤液中加入③____________溶液 | 观察到: ④_________________ | 证明滤液中含有NaOH,则没有的物质是⑤_______________ |
[总结归纳]为了完全除去粗盐中的可溶性杂质,所加入的反应物要_________________。
[拓展延伸]在除去粗盐中可溶性杂质的过程中。小亮认为若实验室中没有氯化钡溶液可以用____________溶液来替换。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的实验装置回答问题。
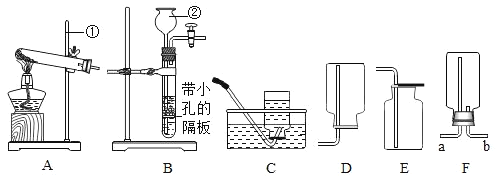
(1)请写出仪器名称:②_________________ 。
(2)实验室若用装置 B 制备氧气,涉及到的化学方程式为:_________________。
(3)实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为:_________________,用装置 B 制备二氧化碳的优点是:_________________,若用F 装置收集二氧化碳气体,二氧化碳应该从_________________(“a”或“b”)端进入。
(4)过氧化钠(化学式为 Na2O2)可用在呼吸面具中作为氧气来源。它能跟二氧化碳反应生成碳酸钠和一种能供给呼吸的气体。 发生反应的化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NH4C1和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4C1 | 3.33 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
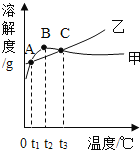
A.甲为NH4C1的溶解度曲线
B.两种物质的溶解度均随温度升高而增大
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,加入的甲、乙固体质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组选用如图装置进行常见气体的实验室制取。提示:常温下CO2难溶于饱和的 NaHCO3溶液。回答下列问题:

(1)仪器①的名称为_______;A中试管口的棉花作用是______________。
(2)若实验室要加热KMnO4制取较纯净的氧气,选择的装置组合是_____,反应的化学方程式为____________________________ 。
(3)实验室常用大理石和稀盐酸,选取B、D装置制取CO2,用此方法制得的CO2中混有HCl.为了除去CO2中混有的HCl,可在B、D装置之间连接F装置,导管口a应连接_____(填“b”或“c”),此时F装置中盛装的试剂为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类是学习化学常用的方法。
(1)物质或离子的名称往往与所含元素的化合价关系密切:如MnO4-(高锰酸根离子)、MnO42-(锰酸根离子),根据ClO3-(氯酸根离子)推测: ClO4-的名称为①______;根据过氧化钾(K2O2)、氧化钾(K2O)等;推测过氧化钙的化学式为②_____。
(2)在初中化学学习中,有些物质溶解性用“—”表示,说明该物质不存在或遇到水会发生“水解”反应。例如:碳酸铜遇水会发生反应 CuCO3 + H2O =Cu(OH)2 ↓ + CO2↑碳酸镁与碳酸铜类似,请仿照写出碳酸镁遇热水发生反应的化学方程式① __ ,反应中各元素的化合价② ___(填“有”或“没有”)改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下图及所给信息回答问题。
装置及药品:①石灰石 ②稀硫酸 ③二氧化锰 ④高锰酸钾 ⑤稀盐酸 ⑥过氧化氢溶液

(1)小英同学选择A装置制取氧气,反应的化学方程式为__________________________,她选择E装置收集氧气,则a端应与_________端相连。
(2)小东同学欲在实验室制取二氧化碳,则他选择的药品是________(填序号),实验室制取二氧化碳的化学方程式为 ______________________________________;用________装置收集二氧化碳,证明二氧化碳已收集满的方法是__________________________。
(3)甲是蒸发溶液的实验,仪器a的名称是______,用玻璃棒不断搅拌的目的是_______。

(4)乙是探究燃烧条件的实验,打开分液漏斗的活塞前,白磷不燃烧,而打开后,白磷燃烧。比较打开前后的现象,证明白磷燃烧需要___________,烧杯中水的作用是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属及其合金在日常生活中具有广泛的应用。
(1)保护金属资源的有效途径是防止金属腐蚀、_______和________。
(2)所谓烤蓝是钢铁零件表面处理的一种防腐蚀的工艺。其原理就是钢铁在高温条件下与水蒸气反应,在钢铁零件表面生成一层致密的氧化层(主要成分是Fe3O4)和氢气,反应的化学方程式为:_______。
(3)工业上冶炼金属铁的原理是用CO还原Fe2O3,反应的化学方程为______;小明家里建造了一栋楼房,共用了20t含杂质1%的钢铁,冶炼这些钢铁,需要含Fe2O3 80%的赤铁矿石的质量= _____(填表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com