
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①根据氯离子的检验方法进行分析判断.
②根据食盐和纯碱的化学性质进行分析判断.
③根据鸡蛋壳的主要成分是碳酸钙,能与酸反应,进行分析判断.
④根据甲醇不与白酒、食醋、蔗糖、淀粉等物质反应,进行分析判断.
解答 解:①检验自来水中含有Cl-,氯离子可用硝酸酸化的硝酸银溶液进行检验,若存在Cl-会生成白色沉淀,利用这些物质不能完成.
②食盐主要成分是氯化钠,纯碱主要成分是碳酸钠,醋酸可以与碳酸钠反应生成气体,不能与食盐反应,可用食醋鉴别食盐和纯碱,利用这些物质能完成.
③鸡蛋壳的主要成分是碳酸钙,将鸡蛋壳放入食醋中,可以检验鸡蛋壳能否溶于酸,利用这些物质能完成.
④甲醇不与白酒、食醋、蔗糖、淀粉等物质反应,无法检验白酒中是否含甲醇,利用这些物质不能完成.
故②③能完成.
故选:C.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:解答题
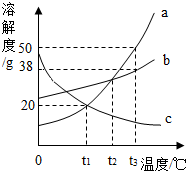 如图是a、b、c三种物质的溶解度曲线.根据图回答:
如图是a、b、c三种物质的溶解度曲线.根据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
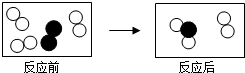
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
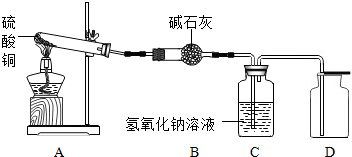
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com