
【题目】氯酸钾有多种用途,常作氧化剂、火箭推进剂等,它易溶于水,在加热时可缓慢释放氧气,但在氧化铜等催化作用下加热会快速放出氧气。小华利用氯酸钾制取氧气来验证氧化铜的催化作用,并探究反应后剩余固体的成分。
(查阅资料)①氯化钾、氧化铜加热不分解;
②硫酸铜易溶于水,溶解度随温度的升高而增大;
③![]()
I.催化剂的制备

(1)步骤1的目的是除去不溶性杂质,步骤1所用到的玻璃仪器有_____。
(2)步骤2的目的是得到CuSO4.5H2O晶体,实验操作是_____、降温结晶、过滤、洗涤、干燥。
Ⅱ.加热氯酸钾制取氧气并探究剩余固体的成分
小华设计了以下两组实验,在相同条件下加热,并记录产生VL氧气所需要的时间,实验发现t1>t2,说明氧化铜可以加快氯酸钾的分解,相关数据如下表。
实验编号 | 反应前氯酸钾的质量 | 加入氧化铜的质量 | 生成VL 氧气所用的时间 | 反应后剩余固体的质量 |
ⅰ | 24.5g | 0 | t1 | m |
ⅱ | 24.5g | 2.0g | t2 | 21.7g |
(1)实验ⅰ中反应后剩余固体的质量m=_____。
(2)探究实验ⅱ反应后剩余固体的成分和氧化铜的催化作用,部分数据如下表。
实验步骤 | 现象或结论 |
①将反应后剩余固体继续加热,直至冷却后连续两次称量固体的质量保持不变。 | 若有气体生成,则说明含有氯酸钾,该反应的化学方程式为_____。 |
②将①加热后剩余固体在足量水中充分溶解,过滤、洗涤、干燥、称量 | 若滤渣的质量为_____,可进一步说明氧化铜对氯酸钾分解有催化作用。 |
③收集、合并②的滤液和洗涤液,加入过量硝酸银溶液,充分反应后过滤、洗涤、干燥、称量 | 理论上可得到沉淀的质量为_____。 |
【答案】玻璃棒、烧杯和漏斗 蒸发浓缩 19.7g ![]() 2g 34.5g
2g 34.5g
【解析】
I、(1)步骤1的目的是除去不溶性杂质,为过滤操作,步骤1所用到的玻璃仪器有玻璃棒、烧杯和漏斗。
(2)步骤2的目的是得到![]() 晶体,实验操作是蒸发浓缩、降温结晶、过滤、洗涤、干燥。
晶体,实验操作是蒸发浓缩、降温结晶、过滤、洗涤、干燥。
Ⅱ、(1) 实验ⅰ、实验ⅱ中硫酸钾的质量均为24.5g,实验ⅱ中催化剂氧化铜的质量为2g,均生成了VL氧气,故实验ⅰ中反应后剩余固体的质量m=21.7g-2g=19.7g。
(2) ①t1>t2,将反应后剩余固体继续加热,直至冷却后连续两次称量固体的质量保持不变,氧化铜应是催化剂,氧化铜做催化剂,氯酸钾受热分解生成氯化钾和氧气,反应的化学方程式为![]() ;
;
②将①加热后剩余固体在足量水中充分溶解,过滤、洗涤、干燥、称量,若滤渣的质量为2g,可进一步说明氧化铜对氯酸钾分解有催化作用。
③收集、合并②的滤液和洗涤液,加入过量硝酸银溶液,充分反应后过滤、洗涤、干燥、称量,得到氯化银固体,根据氯元素质量守恒,
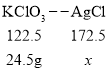
![]()
x=34.5g;
故理论上可得到沉淀的质量为34.5g;
故有:
实验步骤 | 现象或结论 |
①将反应后剩余固体继续加热,直至冷却后连续两次称量固体的质量保持不变。 | 若有气体生成,则说明含有氯酸钾,该反应的化学方程式为 |
②将①加热后剩余固体在足量水中充分溶解,过滤、洗涤、干燥、称量 | 若滤渣的质量为2g,可进一步说明氧化铜对氯酸钾分解有催化作用。 |
③收集、合并②的滤液和洗涤液,加入过量硝酸银溶液,充分反应后过滤、洗涤、干燥、称量 | 理论上可得到沉淀的质量为34.5g。 |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:
【题目】a、b两种固体物质的溶解度曲线如图所示。回答下列问题:
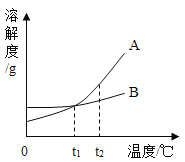
(1)t1℃时a、b的溶解度_____(填相等或不相等);
(2)t2℃时,两种物质的饱和溶液中_____(填a或b)溶质质量分数大;
(3)使b物质结晶的最好方法是_____;
(4)把t1℃时a的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图装置图填空:
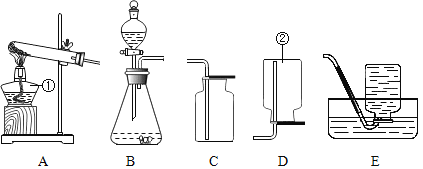
(1)写出如图中标有序号的仪器名称:①_____;②_____.
(2)实验室制取气体时,组装好仪器后,应先_____,再添加药品.
(3)实验室用过氧化氢和二氧化锰制取氧气时,应选用的发生装置是_____(选填装置序号),该装置的优点是_____,用C装置收集氧气时,验满的方法是_____.
(4)甲烷是一种无色无味、难溶于水、密度比空气小的气体.实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选用_____,收集装置应选用_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镍在元素周期表中的信息如下图所示,下列有关镍元素的说法不正确的是

A. 原子序数是28 B. 属于金属元素
C. 原子中的质子数是28 D. 相对原子质量为58.69 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知在同温同压下,气体的体积比等于其分子数之比;室温下,将可能含有CO2、N2、O2的混合气体,先通过炙热的焦炭,反应后恢复至室温气体体积增大;接着通过足量灼热的氧化铜,反应后恢复至室温气体体积无变化,但有红色物质生成;再通入足量氢氧化钠溶液, 最后收集到的剩余气体,可使燃着的木条熄灭。关于该混合气体的成分判断,下列说法中正确的是( )
A.一定含有O2和CO2,可能含有N2
B.一定含有N2和CO2,可能含有O2
C.一定含有O2,且至少含有CO2 和N2中的一种
D.一定含有N2,且至少含有CO2 和 O2中的一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。请结合图示完成下列问题:
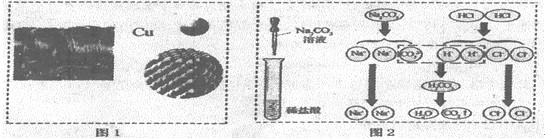
(1)图1中,“Ca”表示多种信息,如表示铜元素、金属铜单质,还能表示 ;
(2)从微粒的角度说明图2反应的实质是 ;
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其反应的微观示意图如图3所示:
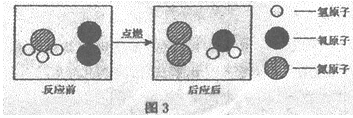
该反应的化学方程式为 ,其基本反应类型属于 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中盛有一定质量的氧化镁和氧化铜的固体混合物,向其中加入7.3%的稀盐酸300g,恰好完全反应,得到该温度下的不饱和溶液316g。则下列相关计算中,正确的是
A.氧化镁和氧化铜的固体混合物质量为16g
B.混合物中氧元素质量为6.4g
C.最终所得溶液中含有溶质的质量为32.5g
D.最终所得溶液中含有氯元素的质量为21.3g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】医疗上的生理盐水中含有A、B、C、D四种元素A、B、C、D的原子序数依次增大
(1)D元素的名称是______
(2)A与B可形成原子个数比1:1的分子,其化学式为_______,该分子中B的化合价是_______
(3)A、B、C形成化合物X的名称为________,其固体溶于水时要______(填“吸热”或“放热”),在X的水溶液中滴加少量CuSO4溶液,现象是_________,A与D形成化合物Y,Y与X在水溶液中反应的化学方程式为_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】变化观与守恒观是化学学科的基本观点。下列有关说法中,不正确的是( )
A.电解水前后,氢、氧元素的质量均没变B.原子得到或失去电子后,其带电情况可能不变
C.复分解反应前后,所有元素的化合价都不变D.10g硫与10g氧气反应,生成20g二氧化硫
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com