
【题目】构建模型和知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的化学性质知识网络,如图所示。
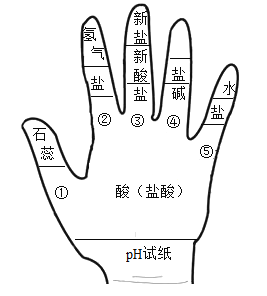
请结合图示回答下列问题:
(1)写出一个符合图中②的一种盐的化学式____________;
(2)写出一个符合图中③的化学方程式_______________;
(3)图中⑤的性质在工业上可用于___________(填用途)。
【答案】ZnCl2或FeCl2等(含有氢之前金属的盐酸盐溶液合理即可) HCl+AgNO3=AgCl↓+HNO3或CaCO3+2HCl═CaCl2+H2O+CO2↑等(合理即可) 除铁锈
【解析】
(1)盐酸与活动性在氢之前的活泼金属反应生成盐酸盐和氢气,符合图中②的一种盐的化学式可以是:ZnCl2或FeCl2或其他氢之前金属的盐酸盐;
(2)图中③表示的是盐与盐酸反应生成新盐和新酸,只要符合复分解反应发生的条件即可,如HCl+AgNO3=AgCl↓+HNO3或CaCO3+2HCl═CaCl2+H2O+CO2↑等;
(3)图中⑤表示的是金属氧化物和酸反应生成盐和水,该性质在工业上可用于除铁锈。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】下列属于复分解反应的是( )
A.3Fe+2O2![]() Fe3O4B.CaCO3
Fe3O4B.CaCO3![]() CaO+CO2↑
CaO+CO2↑
C.CuSO4+2NaOH=Cu(OH)2↓+Na2SO4D.C+2CuO![]() 2Cu+CO2↑
2Cu+CO2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)生产①涤纶衣服、②生铁、③食盐、④塑料水杯所使用的主要材料中,属于有机合成材料___________(填序号)。
(2)生活中由于食物的腐烂变质,造成很大的浪费。铁粉常用于食品保鲜,其原因是____________________________________________。
(3)能源、环境与人类的生活和社会发展密切相关。施用化肥可以提高粮食产量,但滥用会造成环境污染。下列物质中,能用做钾肥的是______________________(填字母)。
A K2SO4 B CO(NH2)2 C NH4NO3 D Ca(H2PO4)2
(4)汽车是现代生活中不可缺少的代步工具。汽车电路中的导线一般是用铜做的,这是利用了铜的延展性和_________性;车体的主要材料为钢,是一种铁的合金,工业上用一氧化碳和赤铁矿石炼铁的反应化学方程式为________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红同学发现妈妈揉面粉时在面粉中加入一种白色粉末,做出的面包疏松多孔,口感很好。她很感兴趣,想探究这种“神奇粉末”的成分。妈妈告诉她所用的白色粉末就是以下三种商品中的一种。
商品 |
|
|
|
成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
[提出问题]白色粉末是哪一种商品?
[查阅资料]
(1)20℃时碳酸钠的溶解度为21.6g,20℃时碳酸氢钠的溶解度为9. 8g。
(2)氯化钙溶液与碳酸氢钠溶液混合不发生反应。
[提出猜想]
猜想1:_______________
猜想2:食用小苏打
猜想3:快速发酵粉
[进行实验]
小红取少量白色粉末于试管中,加入适量蒸馏水,白色粉末溶解,无其他明显现象,猜想__________不正确。为进一步探究这种白色粉末的成分,小红又设计了下面三个实验方案,并进行实验得出了结论。
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取白色粉末于试管中,加水完全溶解,加入稀盐酸 | 有无色气体产生 | 猜想2正确 |
方案二 | 取白色粉末于试管中,加水完全溶解,加入__________。 | 无明显现象 | |
方案三 | 20℃时,在100克水中加入12克该白色粉末,充分溶解 | ___________ |
[实验反思]
经过思考,认为方案一不能得出猜想2正确的结论,理由是__________________(用化学方程式表示)。
[实验拓展]
若小红同学想继续对食用小苏打的成分碳酸氢钠的酸碱度进行探究,她可选用下列中的___________ (填字母)进行实验。
A紫色石蕊溶液
B无色酚酞溶液
CpH试纸
DpH计
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组在探究金属与酸的反应时,观察到镁、锌、铁分别与稀盐酸反应产生气泡速率不同。某同学提出问题:影响化学反应速率的因素有哪些?化学兴趣小组运用以下试剂对影响化学反应速率的因素开展探究活动。
提供试剂:15%的稀盐酸、15%的稀盐酸、铝粉、铁粉、铝片
(提出问题)影响化学反应速率的因素有哪些?
(猜想与假设)
猜想1:物质的性质;猜想2:反应的温度;
猜想3:反应物的浓度;猜想4:___________。
(实验探究)(实验中只能使用提供的试剂)
实验 | 实验操作 | 实验现象 | 实验结论 |
验证猜想1 | 分别向盛有等体积的______两支试管中加入等体积的 15%的稀盐酸 | 盛有_______的试管中产气泡更快 | 物质的性质影响反应速率 |
验证猜想2 | 分别向盛有等体积的铁粉的两支试管中加入等体积的15%的稀盐酸,加热其中一支试管 | 加热试管中产生气泡更快 | 温度越_____,反应速率越快 |
验证猜想3 | 向盛有等质量铁粉的两支试管分别加入__________ | 加入_____试管中产生气泡更快 | 反应物的浓度越大,反应速率越快 |
验证猜想4 | 分别向盛有等质量铝粉和铝片试管中加入等体积5%的稀盐酸 | 盛有铝粉的试管中产生气泡更快 | ________,应速率越快 |
(实验拓展)兴趣小组将未打磨的铝片和稀盐酸放入密闭容器中,用传感器探究反应过程中温度和压强的变化(如下图所示)。下列有关说法正确的是___(填序号)。
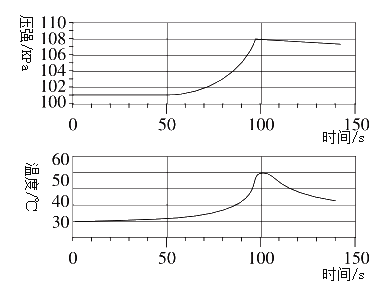
A 铝与盐酸反应吸收热量 B 50s时,溶液中的溶质为AlCl3
C 0~50 s,铝与盐酸反应 D 100~140s,压强减小是因为温度降低
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具。
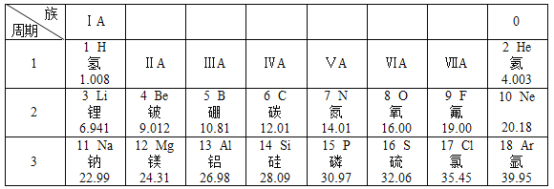
请分析图中信息回答相关问题:
(1)上述表中地壳含量最多的元素是____________(填元素符号), 该元素原子的核电荷数为______ ,该元素的原子在化学反应中容易______________(填“得”或“失”)电子。
(2)氯原子和氩原子化学性质不同的原因是_____________________。
(3) 14元素形成的氧化物化学式是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是氧元素,钠元素在元素周期表中的相关信息及有关粒子的结构示意图,下列说法错误的是( )
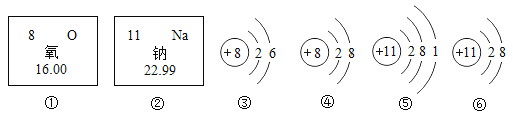
A. 氧元素的原子序数为8
B. ![]() 的结构示意图是
的结构示意图是![]()
C. 氧元素与钠元素的本质区别是最外层电子数不同
D. ![]() 两种元素可组成化学式为
两种元素可组成化学式为![]() 的化合物
的化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某探究小组的同学通过查阅资料得知:在加热条件下,镁不仅能与水反应还能与氯化铵溶液反应。小组同学对此产生兴趣,他们将砂纸打磨过的镁条加入氯化铵溶液中并加热,迅速产生大量气体。为确定生成气体的成分,他们进行如下探究:
(查阅资料)(1)镁与氯化铵溶液反应生成两种气体,每种气体只含有氮、氢两种元素中的一种或两种;
(2)镁与水在加热条件下反应生成氢氧化镁和氢气;
(3)氨气是一种极易溶于水的气体,能与酸反应。
(提出问题)该气体成分是什么?
(作出猜想)猜想一:H2和 N2
猜想二:N2和 NH3
猜想三:__________
(实验探究)
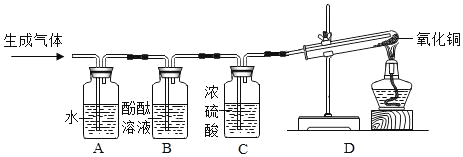
步骤一:小组同学闻气体气味,发现该气体有刺激性气味。则猜想_____________不成立。
步骤二:同学们把产生的气体通入盛有水的 A 装置中除去___________,再将剩余气体依次通入 B、C、D 装置中,一会儿后,加热试管中的氧化铜,观察到 B 中溶液不变色,C 中无明显现象,D 中黑色粉末变成红色固体,试管口有小水珠。装置 C 的作用是____________(合理即可),装置 D 中发生反应的化学方程式为__________。
(得出结论)猜想________________成立。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室里配制 100g10%的 Na2SO4溶液,请回答下列问题:
(1)配制的步骤可以概括为计算、称量和量取、_____________ 、装瓶。
(2)配制该溶液需要 Na2SO4固体_______g,需要水________mL(水的密度是 1g/cm3)。
(3)将 Na2SO4 和水依次倒入烧杯中,需用玻璃棒搅拌,其目的是___________ 。
(4)用溶质质量分数为 12%的 Na2SO4溶液来配制 500g 溶质质量分数为 6%的 Na2SO4 溶液,需要12%的Na2SO4溶液__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com