
【题目】以下是实验室制取气体的装置图,回答下列问题
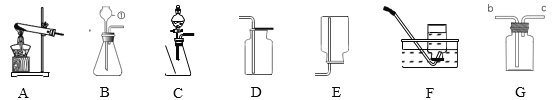
(1)仪器①的名称_____
(2)实验室利用A装置制取氧气的化学方程式_____
(3)实验室可用装置B或C制取H2,C装置相对于B装置,优点有_____,使用G装置收集H2,气体应从_____(填“b”或“c”)端通入
(4)某化学家根据绿色化学中原子转化利用率为100%的理念,为了同时制备氢气和氧气,设计了如下的各步化学反应(Br相对原子质量80)
①CaBr2+H2O![]() CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg![]() HgBr2+H2↑
HgBr2+H2↑
③HgBr2+CaO![]() HgO+CaBr2 ④2HgO
HgO+CaBr2 ④2HgO![]() 2Hg+O2↑
2Hg+O2↑
若要通过上述方法制备8g的氧气,理论上需要溴化钙的质量为_____g,上述制备气体的方法中存在的缺点是_____(只写一点即可)
(5)将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是将气体通入下图装置进行探究
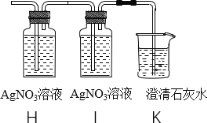
①实验室制取CO2的化学方程式为_____
②装置H、K中溶液变浑浊,I中溶液不变浑浊,则原石灰水未变浑浊的原因是_____
③装置I的作用是_____
【答案】长颈漏斗 ![]() 便于控制反应的速率 c 100 制备过程中使用了汞,可能造成重金属中毒或污染(或反应需要加热,耗费较多能源) CaCO3+2HCl=CaCl2+H2O+CO2↑ 二氧化碳中含有HCl气体 证明氯化氢(HCl)气体已被除尽
便于控制反应的速率 c 100 制备过程中使用了汞,可能造成重金属中毒或污染(或反应需要加热,耗费较多能源) CaCO3+2HCl=CaCl2+H2O+CO2↑ 二氧化碳中含有HCl气体 证明氯化氢(HCl)气体已被除尽
【解析】
(1)据图可知仪器①的名称是:长颈漏斗;
(2)利用A装置制取氧气时,因为试管口没有一团棉花,应该是利用氯酸钾制取氧气,反应的化学方程式为:![]() ;
;
(3)C装置相对于B的优点有:控制反应的发生和停止;用G装置收集H2,气体应从短管进入,因为氢气的密度比空气小;
(4)设制备8g的氧气,理论上需要溴化钙的质量为x,根据元素守恒观,由四个化学方程式得出如下关系:
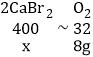
![]()
x=8g;
反应过程中生成汞,所以循环过程需要很高的能量,且使用重金属汞,产生污染;
(5)①实验室制取CO2的化学反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
②装置H、K中溶液变浑浊,I中溶液不变浑浊,则原石灰水未变浑浊的原因是:二氧化碳中含有氯化氢气体;
③装置I的作用是:证明氯化氢气体已被除尽。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.
国内首创
优质硝酸铵
NH4NO3
含氮量全球最高(38%)
国内首创
优质硝酸铵
NH4NO3
含氮量全球最高(38%)
(1)请你写出小强的计算过程和判断依据.计算过程:_____.
结论:该广告_____(“是”或“不是”)虚假广告.
(2)小强认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。
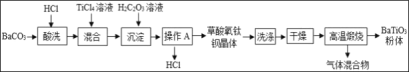
(1)BaTiO3中Ti元素的化合价是_____。
(2)“酸浸”过程中发生反应的化学方程式为_____。
(3)“操作A”的名称是_____。
(4)“绿色化学”理念提倡循环利用,流程中能循环使用的物质是_____。
(5)现有394kg BaCO3,理论上可以制备BaTiO3的质量为_____kg.( BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿原酸(C16H18O9)被誉为“第七类营养素”,可从栽种较广的杜仲(中药材)中提取,下列有关绿原酸的说法正确的是
A. 一个绿原酸分子中含有 43 个分子
B. 在一定条件下,绿原酸可燃烧生成 CO2 和H2O
C. 绿原酸中碳元素的质量分数为![]() × 100%
× 100%
D. 绿原酸分子中氢氧元素的质量比为 2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆圈代表不同的原子.下列说法正确的是( )

A.此反应有单质生成
B.原子在化学变化中是可分的
C.此反应有三种新物质生成
D.参加反应的两种分子的个数比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,回答问题.
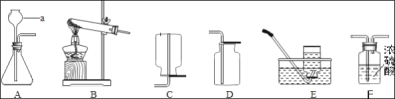
(1)仪器a的名称是_____.
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为_____,选用的发生装置是_____,(填字母序号,下同)充分反应后,剩余物中含的物质化学式为_____,可用_____方法加以分离.
(3)实验室制取并收集一瓶干燥的二氧化碳,化学反应方程式为_____.
(4)实验室用4%的氢氧化钠溶液和二氧化锰制取氧气.若配制4%的过氧化氢溶液110g,需要质量分数为20%的过氧化氢溶液(密度为1.1g/cm3)_____mL,在实验室稀释过氧化氢溶液的主要步骤有:计算、量取、_____、装瓶并贴上标签.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线,下列说法正确的是
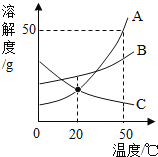
A.除去A中混有的少量B,可采用降温结晶的方法
B.50℃时A的饱和溶液中,溶质的质量分数为50%
C.将C的饱和溶液变为不饱和溶液,可采用升高温度的方法
D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用煤直接做燃料如果不进行处理,会因煤中的硫生成SO2气体造成大气污染。常用两种方法治污,其一在煤中混入粉末状的石灰石,则燃烧产生的SO2会与CaCO3反应生成CaSO3进入炉渣而减少大气污染。其二向燃烧后的烟气喷洒石灰浆也可吸收SO2生成CaSO3。
(1)现用10000元分别购买两种原料来除去SO2,相关数据如下表:
方法 | 物质 | 相对分子质量 | 纯度 | 价格(元/t) | 除SO2的量/t |
A | 石灰石 | 100 | 90% | 200 | 0.288 |
B | 熟石灰 | 74 | 94% | 500 | 0.73 |
工业上多数采用方法B除SO2.其原因有两个分别是:_____;_____。
(2)取50g此炉渣(含24% CaSO3)逐滴加入20%的盐酸,请求出氯化钙和盐酸的相关数据,并在坐标图中画出相应的曲线图(纵坐标为氯化钙的质量,横坐标为盐酸的质量,标出曲线中必要的数据)。_____。
已知:①设炉渣已不含石灰石,炉渣其它成分不与盐酸反应;
②CaSO3和盐酸反应类似于CaCO3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com