
【题目】实验小组将澄清石灰水和碳酸钠溶液混合,充分反应后过滤,得到了滤液M,同学们对滤液M中溶质的成分进行探究,探究过程如下:
[猜想与假设]①含有NaOH;
②含有____.
③含有NaOH、Na2CO3;
④含有 NaOH、Na2CO3和Ca(OH)2。
[设计与实验]
(1)大家认为猜想_____一定不正确,其原因是_______。
(2)甲同学取滤液M样品,向其中加入足量的____,不产生气泡,则猜想③不正确。
(3)乙同学依据甲同学的实验结论继续实验,记录如下
实验操作 | 现象 | 结论 |
取一定量滤液M于试管中,加入__溶液 | ________ | 猜想②成立 |
相关反应的化学方程式为____。
[交流与反思]若将滤液M直接倒入下水道,对环境造成的影响是会污染水源。
(4)若假设①成立,取反应后的滤液M 100克,加入10克溶质质量分数为3. 65%的稀盐酸恰好完全反应,则滤液中溶质的质量分数是多少____?
【答案】NaOH和Ca(OH)2 ④ Na2CO3和Ca(OH)2不能共存(合理即可) 稀盐酸(合理即可) 碳酸钠 有白色沉淀产生 ![]() 0.4%
0.4%
【解析】
猜想与假设:
碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,澄清石灰水和碳酸钠溶液混合,当氢氧化钙过量时,反应后溶液中的溶质有NaOH和![]() ;当碳酸钠过量时溶液中的溶质有NaOH、Na2CO3;当二者恰好完全反应时溶液中的溶质有NaOH;所以猜想②:NaOH和Ca(OH)2;
;当碳酸钠过量时溶液中的溶质有NaOH、Na2CO3;当二者恰好完全反应时溶液中的溶质有NaOH;所以猜想②:NaOH和Ca(OH)2;
设计与实验:
(1)碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,氢氧化钙和碳酸钠不能共存,所以猜想④一定不成立;
(2)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳。猜想③不成立,溶液中的溶质没有碳酸钠,所以甲同学取滤液M样品,向其中加入足量的稀盐酸,不产生气泡;
(3)因为猜想②成立,可以通过加入碳酸钠溶液来检验氢氧化钙的存在。所以取一定量滤液M于试管中,加入碳酸钠溶液,有白色沉淀生成,则可验证猜想②成立;
碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,化学方程式为:![]() ;
;
(4)设滤液中溶质的质量分数是x,则
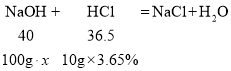
![]()
x=0.4%。
答:滤液中氢氧化钠的质量分数是0.4%。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:初中化学 来源: 题型:
【题目】已知:20℃时,a和b的溶解度分别为36g和88g。
| 序号 | ① | ② | ③ | ④ | ⑤ |
|
固体种类 | a | a | b | b | b | ||
固体的质量/g | 30 | 60 | 30 | 60 | 90 | ||
水的质量/g | 100 | 100 | 100 | 100 | 100 |
下列说法不正确的是
A.20℃时,⑤中溶质与溶剂的质量比为88:100
B.将t1℃时b的饱和溶液加水可变为不饱和溶液
C.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】社会发展让人们的出行更加方便,汽车逐渐走进寻常百姓家。请根据要求回答有关问题:
(1)在上图汽车的部件中主要由有机合成材料制成的是__________;
(2)在汽车的电路中主要使用的是铜线,这是利用了铜的______性;
(3)汽车表面的烤漆不仅美观,还能起到__________的作用
(4)化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题。我市自2018年开始推广使用车用乙醇汽油,到2019年实现全市全覆盖。乙醇(C2H5OH)燃烧的化学方程式是______________,推广使用乙醇汽油的好处是______________ ,______________ (写出两条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1898年德国人首次发现空气中的氮能被碳化钙固定而生成氰氨化钙(CaCN2),为合成氨工业奠定了基础,从而促进了氨碱工业的全面发展,工业上制取纯碱的部分流程如下:
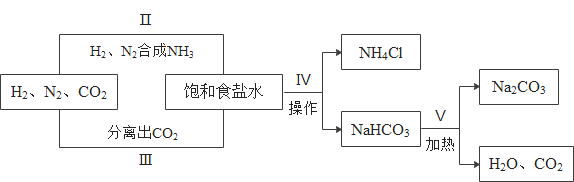
(1)氰氨化钙与水蒸气反应生成氨气和碳酸钙,该反应的化学方程式是____。
(2)碳酸氢钠只有在固态时,加热才会分解,则第IV步中操作的名称是___。
(3)实验室从混合气体H2、N2、CO2中分离出CO2的实验装置如图所示。广口瓶甲和分液漏斗中盛放的药品分别是______溶液(填化学式)、稀硫酸。
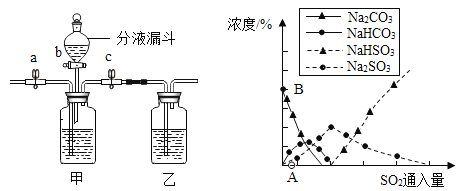
(4)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3,达到减少污染、节约资源的目的。反应过程中溶液组成变化如图所示。
①吸收初期(图中B点以前)反应的化学方程式为_______。
②不断通入SO2,最终产物是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室制取气体的常用装置。
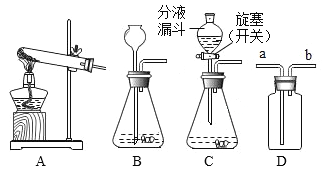
(1)请写出一个用图中装置制取氧气的化学方程式____。
(2)D装置是一储气瓶,若要用该储气瓶中的氧气,应从____(填“a”或“b”)端向储气瓶中注入水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应变化关系的是
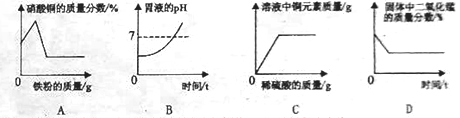
A. 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B. 用胃舒平[主要成分Al(OH)3]治疗胃酸过多时胃液pH的情况
C. 向盛有一定量氧化铜粉末的烧杯中不断加入稀硫酸至过量
D. 加热一定量氯酸钾和二氧化锰固体混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿的主要成分为二硫化亚铁(FeS2),可用于工业上冶炼铁和生产硫酸(如图)。下列说法错误的是( )
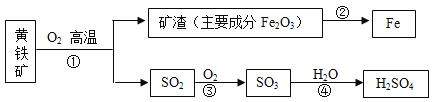
A.反应前将黄铁矿粉碎,能提高反应速率
B.FeS2中硫元素化合价为-1
C.反应②不属于四种基本反应类型的任一种
D.从①→③→④硫元素的化合价都不相同
查看答案和解析>>
科目:初中化学 来源: 题型:
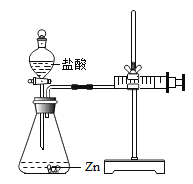
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。写出锌与盐酸发生反应的化学方程式为_______________________.
从实验现象可判断:金属活动性Zn_______Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是_______.
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是_______.
所用药品、实验数据如下表:
实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
1分钟 | 1﹣2分钟 | 2﹣3分钟 | 3﹣4分钟 | 4﹣5分钟 | 前5分钟共收集气体 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出结论】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是_________________.
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是_________________________.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】________________________________.
【实验方案】_____________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钠投入到NH4Cl溶液中,钠浮在液面上,熔成小球,四处游动,并生成大量气体。为确定气体的成分,进行下列实验探究。
(1)猜想:气体可能是HCl、NH3、H2中的一种或几种,作此猜想的理论依据是______。
(2)实验:甲同学为判断气体成分,查阅资料得知:2NH3+3CuO![]() 3Cu+N2+3H2O。于是设计了如下图实验装置:
3Cu+N2+3H2O。于是设计了如下图实验装置:
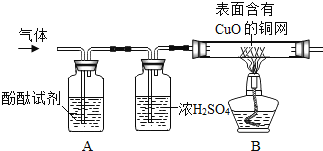
(3)现象与结论:A中观察到酚酞试剂变红色,证明有______;B中玻璃管内观察到固体表面由黑色变红色,证明有______。
(4)实验反思:①浓硫酸的作用是______。
②乙同学认为甲的设计不能确定是否含有HCl,于是他将气体通入酸化的______溶液中,无白色沉淀产生,则该气体中______HCl(填“有”或“无”)。
③写出Na与NH4Cl溶液反应的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com