
【题目】甲、乙、丙三种物质分别是高炉炼铁三种原料的主要成分,A~J 是初中化学常见的物质, 它们有如下转化关系(部分反应的生成物和反应条件已略去)。已知 B 在大气中的存在产生了温室应,H是通常状况下密度最小的气体,D 和 G 可以发生中和反应。

请回答下列问题:
(1)写出化学式: 甲______________, B______________;
(2)写出符合要求的化学方程式:
反应② ___________________,
反应③_____________________;
(3)在上述转化中,I 和 J 两种物质的组成元素相同,且反应⑤属于化合反应,则反应⑤的化学方程式为____________。
【答案】CaCO3 CO2 Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 3C+2Fe2O3![]() 3CO2↑+4Fe Fe+2FeCl3═3FeCl2
3CO2↑+4Fe Fe+2FeCl3═3FeCl2
【解析】
B在大气中会产生温室效应,可以推出B是二氧化碳,H是通常状况下密度最小的气体,可知H是氢气,甲、乙、丙又是高炉炼铁的三种主要原料,可知甲、乙、丙应该是氧化铁、碳、石灰石中的一种,甲又会生成二氧化碳,所以甲就是碳酸钙,A就是氧化钙,氧化钙和水反应会生成氢氧化钙,所以C就是氢氧化钙,D和G会发生中和反应,D和二氧化碳反应又会生成E,所以D是一种碱,G是一种酸,D是氢氧化钠就满足要求,G是稀盐酸、稀硫酸都行,那么E就是碳酸钠,丙和酸会反应生成I,可以推出丙就是氧化铁,乙就是碳,F就是铁,铁和酸反应会生成氢气,氧化铁和酸反应生成的是铁盐,铁盐和铁反应会生成亚铁盐,再将推出的各种物质代入转化图中推导合理。
由分析可知(1) 甲是CaCO3, B是CO2;
(2)反应② 碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;反应③碳和氧化铁在高温的条件下生成铁和二氧化碳,反应方程式为:3C+2Fe2O3![]() 3CO2↑+4Fe;
3CO2↑+4Fe;
(3)铁和盐酸反应生成氯化亚铁和氢气,氧化铁和盐酸反应生成氯化铁,又知道F是铁,依据反应物和生成物可知,氯化铁和铁反应生成氯化亚铁,反应方程式为:Fe+2FeCl3═3FeCl2。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:初中化学 来源: 题型:
【题目】请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
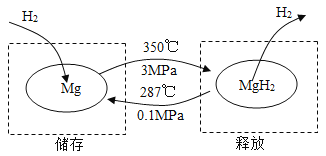
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示实验中得出的结果不正确的是

A.甲实验:划出刻痕,说明合金的硬度大于纯金属
B.乙实验:冷却后析出晶体,说明硝酸钾的溶解度随温度降低而减小
C.丙实验:反应后天平指针偏右,说明该反应不符合质量守恒定律
D.丁实验溶液由红色变为紫色,说明碳酸不稳定,受热易分解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组要配制100g质量分数为20%的碳酸钠溶液,下图是他配制碳酸钠溶液的实验操作示意图。请回答下列问题:
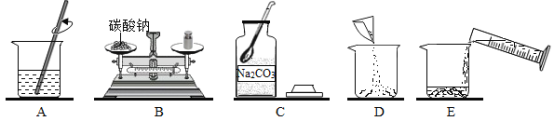
(1)计算配制100g溶质质量分数为20%的碳酸钠溶液所需:碳酸钠_____g;水_____mL,量取所需要的水应选择_____(选填“10 mL”、“50 mL”或“100 mL”)量筒。
(2)用上述图示的序号表示配制溶液的操作顺序:_____。
(3)在配制碳酸钠溶液的过程中应该用到的玻璃仪器分别有_____。
(4)如果称取的碳酸钠中含有少量水分,最后配制的碳酸钠溶液的浓度将_____(填“偏高”、“偏低”、或“无影响”)。
(5)用托盘天平正确称量所需的碳酸钠时,发现托盘天平的指针偏向左盘,应_____(填序号)
A 增加适量的碳酸钠固体 B 减少适量的碳酸钠固体 C 调节平衡螺母 D 增加砝码
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体的溶解曲线图,下列说法正确的是
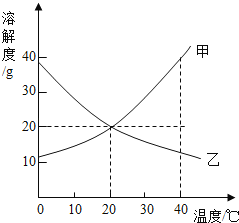
A.乙的溶解度随温度升高而增大
B.升高温度可使甲的不饱和溶液变为饱和溶液
C.20℃时,甲的饱和溶液的质量分数为 20%
D.将 40℃时甲、乙各自的饱和溶液降温到 20℃,所得溶液溶质质量分数:甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图中字母代表含硫元素的物质,下列判断错误的是
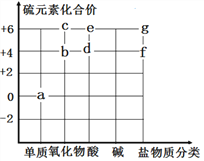
A. 物质d为H2SO3 ,读作亚硫酸
B. 物质b与氧气反应可生成物质C
C. 物质a在氧气中燃烧可以生成物质C
D. 物质Na2SO3、CaSO4可分别用f、g表示
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明它们的化学性质_____;
(2)在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
①比较两种铁矿石:磁铁矿(主要成分 Fe3O4)和菱铁矿(主要成分 FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是______;
②铝制品应用广泛,不易被腐蚀,是因为______(用化学方程式来表示);
(3)镁铝合金被誉为“21 世纪绿色金属结构材料”。一种镁铝合金 Mg17All2 是特殊的储氢材料,完全吸收氢气后得到 MgH2 和 Al,该反应的化学方程式为_____;
(4)钛和钛合金是 21 世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其_____(填字母序号)非常好;
A 可塑性 B 机械性能 C 抗腐蚀性能
(5)铁在潮湿的空气中易生成疏松的铁锈。已知:2FeCl3+Fe=3FeCl2
①铁锈的主要成分是________(填化学式),将生锈的铁制品放入一定量的稀盐酸中充分反应,变化过程中最多涉及______种化学反应基本类型;
②将 10g 表面生锈的铁钉(杂质已忽略)浸泡在 100g 溶质质量分数为 7.3%的稀盐酸中充分反应,观察到铁锈已完全消失。反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为 3.6g。则原生锈铁钉中铁元素的质量分数为______;
(6)利用“活泼金属”可以制得 H2 用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有________ (填字母序号)。
A 金属原料的成本 B 生成过程中的能耗和污染 C 金属的回收利用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料与人类的生产和生活密切相关。请回答:
(1)铜制成导线主要利用铜的__________;铝不容易被锈蚀,其原因是__________(用化学方程式表示);高炉炼铁就是利用焦炭与__________(写名称)反应生成的一氧化碳把铁矿石中铁还原出来。
(2)为了验证铝、铁、铜三种金属的活动性顺序,设计了下列四种方案,其中可行的是____。(填序号)
①将同样粗细铝、铁丝分别浸入到硫酸铜溶液中
②将同样粗细的三种金属丝分别浸入同样的稀硫酸中
③将同样粗细的三种金属丝分别放在氧气中燃烧
④将铁丝分别浸入到硫酸铝、硝酸铜溶液中
(3)对自行车钢架进行喷漆可以防止其生锈,原因是_____;用稀盐酸除去铁锈,该反应的化学方程式为__________。利用铁生锈的原理,“纳米α铁粉”用作食品保鲜剂,若用化学方法检验使用一段时间的“纳米α铁粉”是否完全失效,可选用 __________(填试剂名称)检验。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙通过化合反应制备丙,如图是三种分子的模型图,根据微观示意图得出的结论错误的是( )
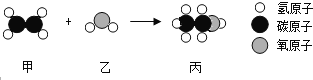
A. 甲的化学式为C2H4
B. 保持乙化学性质的最小微粒是水分子
C. 乙和丙都属于氧化物
D. 化学反应前后分子的种类都发生了改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com