
【题目】如表为元素周期表中部分元素的相关信息,请利用如表回答相关问题。
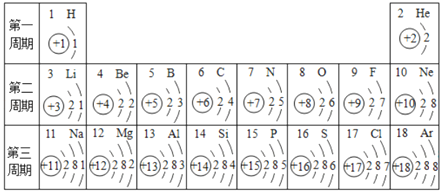
(1)碳原子的核电荷数是_____。
(2)12号元素的原子在化学反应中比较容易_____(填“得到”或“失去”)电子。
(3)在同一周期中,从左到右各元素的原子最外层电子数逐渐_____。
(4)一定条件下,将2.4gCH4与8.0g由8号元素组成的单质,在点燃条件下恰好完全反应,生成5.4gH2O、2.2gCO2和物质X,该化学方程式为3CH4+5O2![]() CO2+6H2O+2X,则X的化学式是_____。
CO2+6H2O+2X,则X的化学式是_____。
(5)将镁、钙、铁、铜四种等质量的金属投入到足量的稀硫酸中,反应速度最快的是_____,产生氢气最多的是_____。
【答案】6; 失去 增加 CO 镁; 镁
【解析】
(1)根据元素周期表可知碳原子的原子序数为6,由原子序数=核电荷数,因此碳原子的核电荷数为6;故答案为:6;
(2)12号元素原子最外层电子数是2,在化学反应中其原子比较容失去到2个电子变成离子;12号元素是镁,属于金属元素;
故答案为:失去;金属;
(3)在同一周期中,从左到右各元素的原子最外层电子数逐渐增加;故答案为:在同一周期中,从左到右各元素的原子最外层电子数逐渐增加。
故答案为:增加。
(4)8号元素是氧元素,故组成的单质是氧气,一定条件下,2.4gCH4与8.0g O2恰好完全反应,5.4gH2O、2.2gCO2和物质X.则X的质量=2.4g+8.0g﹣5.4g﹣2.2g=2.8g;2.4gCH4中含有碳元素的质量为:2.4g×![]() =1.8g,故含有氢元素的质量为:2.4g﹣1.8g=0.6g;5.4gH2O中含有氢元素的质量为:5.4g×
=1.8g,故含有氢元素的质量为:2.4g﹣1.8g=0.6g;5.4gH2O中含有氢元素的质量为:5.4g×![]() =0.6g;2.2gCO2中含有碳元素的质量为:2.2g×
=0.6g;2.2gCO2中含有碳元素的质量为:2.2g×![]() =0.6g,故X中含有1.8g﹣0.6g=1.2g的碳,不含有氢元素,含有氧元素的质量为:8.0g﹣(5.4g﹣0.6g)﹣(2.2g﹣0.6g)=1.6g,故X中碳原子和氧原子的原子个数比为:
=0.6g,故X中含有1.8g﹣0.6g=1.2g的碳,不含有氢元素,含有氧元素的质量为:8.0g﹣(5.4g﹣0.6g)﹣(2.2g﹣0.6g)=1.6g,故X中碳原子和氧原子的原子个数比为:![]() :
:![]() =1:1.故该物质是一氧化碳;故填:CO;
=1:1.故该物质是一氧化碳;故填:CO;
(5)将镁、钙、铁、铜四种等质量的金属投入到足量的稀硫酸中,只有镁和铁与稀盐酸反应,反应速度最快的是镁,产生氢气最多的是镁。故填:镁;镁。


 星级口算天天练系列答案
星级口算天天练系列答案科目:初中化学 来源: 题型:
【题目】我国民间有端午挂艾草的习俗。艾草含有丰富的黄酮素(化学式为C15H10O2),有很高的药用价值。请回答:
(1)黄酮素含有______种元素,碳、氢的原子个数比是______(最简整数比)。
(2)黄酮素的相对分子质量是______。
(3)黄酮素中碳、氢、氧元素的质量比为______。
(4)黄酮素分子中碳元素的质量分数是为______(计算结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月18日,中国又创下一项世界第一,在我国海域试开采可燃冰获得成功。预计在 2030年以前可燃冰资源会得到商业性开发利用,将在一定程度上缓解化石能源面临被耗尽的危险。可燃冰中的主要可燃成分是甲烷。
(1)目前使用的主要化石燃料有煤、______和天然气等。
(2)甲烷燃烧的化学方程式是_______。
(3)可燃冰属于未来的新能源,下列不属于新能源的是________(填序号)。
A.汽油 B.太阳能 C.氢能 D.核能
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图回答下列问题。
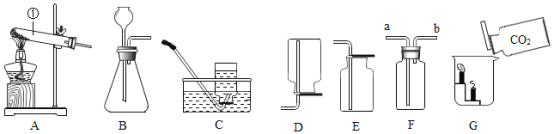
(1)写出标有①的仪器名称_____。
(2)写出实验室由A装置制取氧气的化学反应方程式_____。
(3)某同学要制取二氧化碳应选用的装置组合为_____,如果要选择F装置收集,则应该从_____端通入,如何验满?_____。B装置中长颈漏斗下端要形成液封,目的是_____,实验过程中该同学观察到B中反应太快,不利于气体收集,他可选择下列措施中的_____(填序号)解决该问题。
A.将长颈漏斗换成注射器
B.向装置中加入适量蒸馏水
C.将锥形瓶换成试管加带孔的塑料片
(4)如G图所示,将一瓶二氧化碳气体慢慢倒入放着蜡烛的烧杯中,现象为_____,可体现二氧化碳的性质为:_____、_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,请用所学化学知识回答下列问题。
(1)金刚石和石墨都是由碳元素组成的单质,但是由于_____,因此它们的物理性质存在着较大差异;
(2)用一氧化碳和磁铁矿石(主要成分是Fe3O4)炼铁,其反应的化学方程式是_____。
(3)铝制品形成致密保护膜的化学方程式是_____。
(4)小敏对妈妈说:“你说菠菜中富含铁,为什么我用磁铁无法把菠菜吸起来呢?”小敏认为的铁是指_____。(选填“铁元素”或“铁单质”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家发现,利用催化剂可有效消除室内装修材料释放的甲醛,其反应的微观示意图如下。下列有关该反应的说法不正确的是
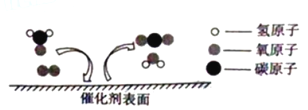
A. 属于置换反应
B. 可减少屮醛带来的室内空气污染
C. 其中催化剂可以加快甲醛的消除
D. 化学方程式为:CH20+02![]() CO2+H20
CO2+H20
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
尿素是一种白色晶体,化学式为C0(NH2)2,属于有机物,它是目前使用量最大的一种化学肥料。
尿素是蛋白质在体内代谢的产物。早在17371785年间,德国医生博哈夫和法国实验员鲁埃分别通过蒸发尿液获得了尿素。
1811年,英国化学家戴维将一氧化碳和氯气(Cl2)的混合物暴露在 円光中,获得光气(COCl2),再将光气与氨作用合成尿素。目前工业上用氨气和二氧化碳在一定条件下合成尿素。
尿素在土壤中酶的作阳下,转化成碳酸铵或碳酸氢铵,才能被作 物吸收利用,在土壤中不残留任何有害物质,长期施用没有不良影响。 尿素在转化前是分子态的,不能被土壤吸附,应防止随水流失。
依据文章内荇,回答下列问题。
(1)尿素中含有_______种元素。
(2)蒸发尿液可获取尿素,由此可以推测尿素的性质是_______。
(3)英国化学家戴维将光气与氨作用合成尿素,该反应的化学方程 式为:COCl2+4NH3=CO(NH2)2+2_____。
(4)合成尿素的微观示意图如下,该反应的化学方程式为_____________________。
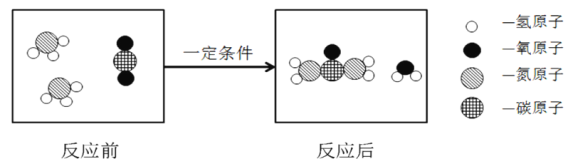
(5)下列说法正确的是______________(填字母序号)。
A.蛋白质在体内的代谢产物之一为尿素
B.尿素施用在土壤中,能够被作物直接吸收
C.尿素是一种含氮有机物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】苹果醋是一种利用苹果发酵制成的饮料,具有一定的保健功能.苹果酸(化学式为C4H6O5是这种饮料的有效成分.请计算:
(1)每个分子中含_________个原子;
(2)苹果酸中碳、氢、氧元素的质量比是(化成最简整数比)____________;
(3)67克苹果酸中含碳元素的质量有____________克.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com