
科目: 来源: 题型:
【题目】化学在材料、能源的研究和开发中起到重要的作用。
(1)可燃冰的主要成分是甲烷水合物,化学式是CH48H2O,在温度升高时会释放出甲烷。
①甲烷属于__________(填序号)。
A.混合物 B.纯净物 C.化合物 D.氧化物
②甲烷在充足的氧气中燃烧的生成物有__________________________。
(2)石墨烯(化学式为C)是从石墨中分离出的单层石墨片,它是世界上已知的最薄、最坚硬的新型材料,有良好的导电性和导热性。
①下列有关石墨烯的说法正确的是______________。
A.在常温下,化学性质不活泼 B.硬度比金刚石小 C.能够导电和导热
②将甲烷(CH4)在铜基体上高温发生分解生成氢气,同时碳原子会沉积吸附在铜的表面连续生长成石墨烯。该反应的化学方程式是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在化合物中,锑元素常显+3价或+5价。现有含锑元素的3种化合物:三氯化锑 SbCl3、三氧化二锑Sb2O3、锑酸钠NaSbO3。回答下列问题:
(1)用化学用语表示:
2个锑原子___________, SbCl3中含有的阳离子___________,锑酸钾__________。
(2)Sb2O5 是一种重要的阻燃剂。
①Sb2O5读作_________________;
②工业制取Sb2O5的化学方程式为:Sb2O3 + 2H2O2 =Sb2O5 + 2X,则X的化学式为_________。
(3)工业上常用碳与Sb2O3固体在高温下反应制得锑和二氧化碳,写出该反应的化学方程式是
_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案,不能达到实验目的是
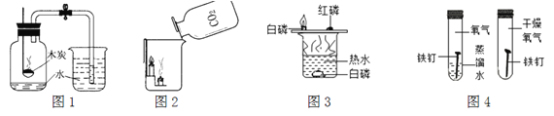
A. 图1测定空气里氧气的含量 B. 图2证明二氧化碳的密度比空气大
C. 图3探究可燃物燃烧需要的条件 D. 图4探究铁生锈需要与水接触的条件
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究木炭在高温条件下还原氧化铜所生成的气体产物是什么,课外兴趣小组进行了如下实验探究:
【提出问题】生成的气体产物是什么?
①【实验猜想】猜想1:只有CO2;
猜想2:只有________________(填化学式);
猜想3:含有CO和CO2。
若猜想1成立,木炭与氧化铜反应的化学方程式为____________________。
②【实验探究】基于猜想3,根据CO和CO2的性质,兴趣小组同学设计了下图装置进行探究。
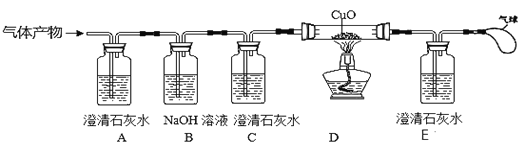
(提示:NaOH溶液能吸收CO2)
(Ⅰ)观察到A装置中的澄清石灰水变浑浊,证明气体产物中有CO2,A装置中的化学方程式是
___________________。
(Ⅱ)有两种实验现象都能分别证明气体产物中含有CO。
现象1:C装置中澄清石灰水___________________,E装置中出现浑浊的现象。
现象2:D装置中出现________________________________的现象。
(Ⅲ)C装置的作用是_________________________________。
(Ⅳ)图中气球的作用是____________________________。
【实验结论】通过实验探究,猜想3成立。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据实验装置图,回答问题。
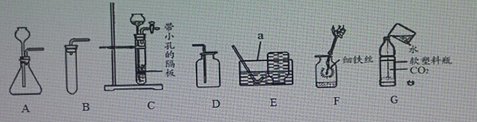
① 仪器a的名称是___________________。
② 用过氧化氢溶液和二氧化锰的混合物制取氧气。
(Ⅰ)请你在“A”、“B”两套装置中选择其中一套作为发生装置,并说明选择的理由。____________。
(Ⅱ)如用D装置收集O2,检验O2是否收集满的方法是__________________。
(Ⅲ)二氧化锰的作用是_______;反应结束后,要回收混合物中的MnO2,实验操作是_______。
(Ⅳ)探究溶质质量分数对过氧化氢分解速率的影响:分别取10mL 5%、15%、30%的过氧
化氢溶液三份,测定收集到100mL氧气所用的时间(其它实验条件均相同),记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液的溶质质量分数 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | ___________________________ | ||
(Ⅴ)用收集的氧气完成图F铁丝燃烧的实验,为使铁丝在氧气中持续剧烈燃烧,把光亮的细铁丝盘成螺旋状,_________,缓慢插入集气瓶中,观察到持续剧烈燃烧;该反应的化学方程为_______。
③ 用大理石和稀盐酸反应制取二氧化碳。
(Ⅰ)制取二氧化碳时,能随时控制反应的发生和停止,则选择的发生装置和收集装置是______(写序号)。
(Ⅱ)反应结束后,生成了0.2mol二氧化碳,求稀盐酸中参与反应的HCl的质量。__________(根据化学方程式列式计算)。
(Ⅲ)如图G向装满CO2 的软塑料瓶注入约1/3体积的水,立即旋紧瓶盖,振荡,再在软塑料瓶中滴入紫色石蕊试液,观察到的现象是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据电解水的实验,回答下列问题。
(I)从宏观上观察:如下图所示,若a管收集到8mL气体,则在相同条件下b管应收集到的气体是______mL。

(II)从微观上分析:说法正确的是__________(选填编号)。
A.水是由氢分子和氧分子构成的 B.水是由氢原子和氧原子构成的
C.每个水分子由2个氢原子和l个氧原子构成的 D.水是由水分子构成的
(III)从符号上表示:电解水的化学方程式为_________________。
(Ⅳ)说明水是一种化合物的实验事实是_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】水是一种重要的资源。请回答下列问题:
① 活性炭常用于净水,主要利用其___________性。
② 用来检验无水酒精中是否含有水的物质是____________。
③ 打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随_______而减小。
④ 在宏观、微观和符号之间建立联系是化学特有的思维方式。
⑤ 水是一种重要的溶剂,配制100g溶质质量分数为16%的氯化钠溶液,所需水的体积为_______mL(水的密度是1.0g/cm3);溶解时玻璃棒搅拌的目的是__________。
⑥ 甲、乙两种固体物质(不含结晶水,且不与水反应)的溶解度曲线如下图。
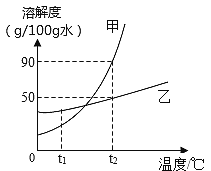
(I)甲、乙两种物质中溶解度受温度影响较大的是___________物质。
(Ⅱ)若将t2℃时甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法是_________。(任写一种即可)
(Ⅲ)若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是____________。
(IV)t1℃时,若将25g乙固体加入50g水中,充分搅拌后,仍有9.2g乙固体未溶解,则t1℃时乙的溶解度为______。
(V)t2℃接近饱和的甲溶液逐渐冷却至t1℃,下图中有关量随时间变化的趋势正确的是________。(选填编号)

查看答案和解析>>
科目: 来源: 题型:
【题目】联系学过的化学知识,回答下列问题。
① 空气中体积分数约为21%的气体是____________,作为植物光合作用原料的是__________(均用化学式表示)。
② 2017年5月我国首次海域可燃冰试采成功,可燃冰外观像冰,主要含有甲烷水合物,还含少量二氧化碳等物质。
(I)可燃冰属于______________(填“纯净物”或“混合物”)。
(II)2mol甲烷(CH4)中约含______________个原子(用科学记数法表示)。
(Ⅲ)工业上,可以利用甲烷获得氢气,其反应的微观示意图如下:
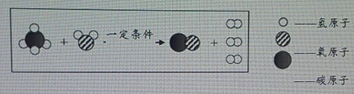
上图所示反应的化学方程式为______;反应物中含碳元素的物质中碳元素质量分数为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】属于分解反应的是
A. 2KMnO4![]() K2MnO4 + MnO2 + O2↑ B. CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
K2MnO4 + MnO2 + O2↑ B. CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
C. 2Na + Cl2![]() 2NaCl D. 2Mg + CO2
2NaCl D. 2Mg + CO2![]() 2MgO + C
2MgO + C
查看答案和解析>>
科目: 来源: 题型:
【题目】某氢氧化钙粉末中含有碳酸钙杂质,现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图-12所示。

图-12
(1)生成二氧化碳的质量是 g。
(2)计算样品中碳酸钙的质量分数(结果精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com