
科目: 来源: 题型:
【题目】某班同学用右图装置测定空气中氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是
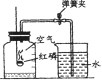
①甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
②甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
③乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
A.只有①③ B.只有②④ C.只有①②③ D.只有①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。实验小组为探究碘化钾变质原理,进行如下活动。
(查阅资料)
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2==2K2CO3+2I2乙:4KI+O2+2X=4KOH+2I2
⑴请将上述方程式补充完整,X的化学式是_____。
Ⅱ.KOH与NaOH都属于碱,二者的化学性质相似。
(进行实验)实验1:探究变质的原理
取适量碘化钾固体暴露于空气一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
⑵实验过程中产生的气体是_____。化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。理由是_____。
(进行实验)实验2:探究变质的条件
分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
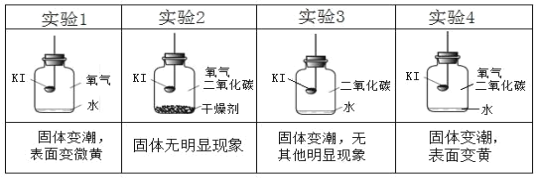
(解释与结论)
⑶对比实验_____(填序号),可以得出KI变质一定与水有关。对比实验_____(填序号),可以得出KI变质一定与氧气有关。
⑷从上述实验可推知,KI变质的条件是_____。
(提出问题)CO2的作用是什么?
(进行实验)
分别取10mL同浓度的KI溶液于3支试管中(试管编号1,2,3),再向试管2中通入CO2,向试管3中滴加几滴盐酸,分别用pH试纸测定溶液的pH;几分钟后,观察溶液的颜色。实验现象记录如下:
试管序号 | 1 | 2 | 3 |
溶液pH | pH=8 | pH=6 | pH=4 |
溶液颜色 | 无色 | 浅黄色 | 黄色 |
(解释与结论)
⑸①pH试纸的使用方法是_____。②CO2在KI变质过程中的作用是_____。
(反思与评价)
⑹探究KI变质条件时,同学们排除了氮气和稀有气体的影响,其原因是_____。
(拓展应用)
测定实验中使用的盐酸中所含溶质的质量分数。
⑺向烧杯中加入质量分数为10%的氢氧化钠溶液40g,再逐滴加入该盐酸,用pH计测定滴加过程中溶液的pH值。图2为滴加盐酸的质量与溶液pH的关系图。
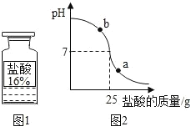
①a点对应的溶液中的溶质为_____(写化学式)。
②盐酸与氢氧化钠溶液反应是_____(选填“吸热”或“放热”)反应。
请以此次测定的数据,列式计算该盐酸的实际溶质质量分数。_____(写出计算过程)
⑻该盐酸的实际溶质质量分数与标签上标出的溶质质量分数不同的可能原因:_____(不考虑测量误差)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是化学兴趣小组同学设计的化学动力小车,在试管中加入两种试剂,塞紧塞子,将小车放在摩擦系数极小的道路上,过一会小车就向左运动了。
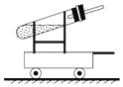
(可选试剂)①锌粉;②铁粉;③铜粉;④20%的稀硫酸;⑤干冰
⑴在加入的两种试剂总质量相同的条件下,若加一次药品能使小车在同一条水平道路上行程最远,应选择加入上述某一种金属,并且两种试剂使用的量要控制在恰好完全反应,此反应的化学方程式为_____;基本反应类型为_____。
⑵在加入的两种试剂总质量相同的条件下,要使小车运动的速度最快,应往试管中加入上述哪一种金属?_____(填序号),原因是_____;
⑶有的同学根据上述小车推进原理,发现不进行化学反应,也能使小车运动,则他在试管中投入的试剂可能是_____。(填序号)
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下图回答问题:
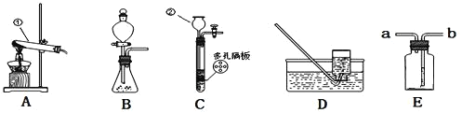
⑴仪器名称:①_____,②_____。
⑵用氯酸钾和二氧化锰混合制取氧气,可选用装置_____(选填序号)和D组合,反应的化学方程式为_____,二氧化锰的作用是_____。
⑶实验室可用装置B或C制氢气,C装置相对于B的优点有_____。氢气能用D装置收集的原因是_____。
⑷用大理石和稀盐酸制取二氧化碳,发生反应的化学方程式为_____,用E装置收集二氧化碳,二氧化碳验满时燃着的木条应放在_____(选填“a”或“b”)端口。
⑸利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。有关说法正确的是_____。
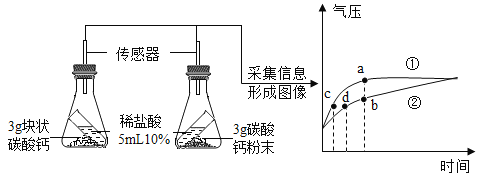
A 曲线①表示块状碳酸钙与稀盐酸反应
B b点表示碳酸钙与盐酸反应已停止
C 等质量碳酸钙粉末产生的CO2的质量最多
D 对比分析点c、d可知,相同的气压时,粉状碳酸钙与稀盐酸反应速率更快
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与日常生活密切相关。双休日在家小明记录了自己一天丰富的生活。
⑴清晨,小明给自己做了一份营养早餐。
①早餐包括全麦面包、鸡蛋、牛奶和橙子,其中富含蛋白质的食物是_____。
②橙子中富含Vc(C6H8O6),Vc中碳元素、氢元素、氧元素的最简质量比为_____。
⑵早餐后,小明给花儿浇浇水,施点肥。植物营养液的说明上写着“该营养液富含氮、磷、钾”,这里的氮、磷、钾是指组成物质的_____。(填“分子”、“原子”或“元素”)
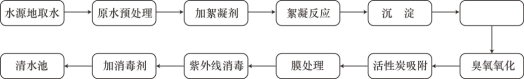
⑶完成老师布置的作业后,小明和妈妈乘坐电动汽车去参观自来水博物馆、植物生态园。自来水的制水工艺流程如下图所示:
①小明和妈妈乘坐的电动汽车,用充电桩给电动汽车充电,其电池在充电时将电能转换成_____能。充电桩上用作保险丝的武德合金属于_____(选填“金属材料”或“合成材料”)材料。
②自来水的制水工艺流程图中空缺的一步操作名称是_____。
③在植物生态园,闻到阵阵花香,小明从分子的角度给妈妈解释原因_____。
⑷晚上,小明和妈妈一起做晚饭。
①小明发现煮饭所用的大米为“富硒大米”,查阅资料后发现硒元素具有抗衰老、抑制癌细胞的功能。硒元素的信息如图。下列有关说法正确的是_____(填字母序号)。
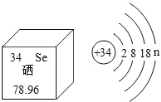
A硒属于金属元素
B硒元素的化学性质与硫元素相似
C硒的相对原子质量为78.96g
D硒元素位于元素周期表第四周期
②炒菜时小明发现家用燃气灶所用的清洁燃料是天然气,天然气的主要成分是_____(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是
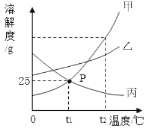
A. 将等质量的三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质
B. P 点表示t1℃时甲、丙两种物质的饱和溶液质量相等
C. t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
D. t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为 1∶4
查看答案和解析>>
科目: 来源: 题型:
【题目】随着科学的发展,新能源的开发不断取得突破。研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下(图中的微粒恰好完全反应)。下列说法正确的是
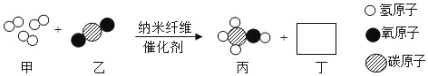
A. 反应前后原子数目发生改变B. 该反应不遵循质量守恒定律
C. 甲是单质,乙、丙、丁均为化合物D. 乙、丙都属于有机物
查看答案和解析>>
科目: 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴 趣小组的同学进行了如下实验,请你参与过程分析。

(查阅资料)
①草酸晶体在浓H2SO4作用下受热分解,化学方程式为:H2C2O43H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
②碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳
③铁的常见氧化物中铁的质量分数:

称取铁红样品10.0g,用上述装置进行实验,测定铁红的质量分数。
(1)D中充分反应后得到Fe粉的质量为mg,则_______<m<_______。
(2)实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是_______。
(实验评价)
(4)反思1:本实验中如果缺少F装置(不考虑其它因素),则测得样品中铁的质量分数会_____(填 “偏小”、“不变”或“偏大”)。
(5)反思2:请指出实验装置的一个明显缺陷_________。
(6)取出适量铁加入稀硫酸中恰好完全反应得到硫酸亚铁溶液,将一包由6.5克锌、4.8克镁、2.4克碳 混合而成的粉末,加入到此溶液中。实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量可能是(___________)
A 19g B 21g C 20g D 19.2g
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同 学们对此进行了探究。
(查阅资料)通常情况下,1体积水溶解1体积的CO2。
(实验探究)小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验。
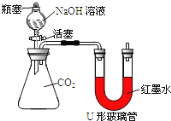
(1)打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面_____(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是______;请根据初中化学知识写出CO2与NaOH 溶液反应的化学方程式:_________
(2)小明认为小红的实验方案不严密,理由是__________,
(问题讨论)用图所示装置进行实验:
兴趣小组的同学们为此又设计了检验生成物的方法来证明。向反应后溶液中加入足量的BaCl2溶液,若有_______的现象,则说明两者确实反应生成了碳酸钠。为了进一步确认反应后 的溶液中是否有氢氧化钠剩余,可以向其中加入____,若出现_________现象则说明氢氧化钠仍有剩余。
(3)用气体压力传感器也可以研究二氧化碳与氢氧化钠的反应。
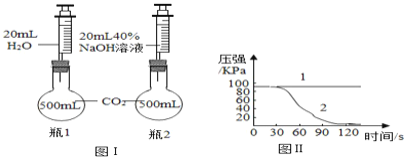
图Ⅰ表示的该实验的设计方案,图Ⅱ中曲线1和曲线2分别表示瓶1和瓶2内气压随时间的变化趋势。
①从曲线 1 可以看出添加20mL水之后,瓶中压强没有发生任何变化,请解释原因_______;曲线1____(能/不能)说明水和二氧化碳发生化学反应。
②对比曲线1和曲线2可知,二氧化碳和氢氧化钠一定发生了化学反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com