
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是
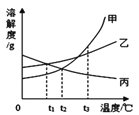
A. t2℃时,甲、丙两溶液中溶质的质量分数相等
B. 甲物质中混有少量乙物质,可用降温结晶的方法提纯甲
C. t3℃时,甲、乙、丙三种饱和溶液恒温蒸发等质量的水,则析出固体(不含水)的质量:甲>乙>丙
D. t3℃时,甲、乙两种饱和溶液降温到t2℃时析出固体的质量:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中不属于化合、分解、置换反应的是( )
A. Fe+2HCl═FeCl2+H2↑
B. 2NO+O2=2NO2
C. 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
D. 2NaCl![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】氮肥能促进作物的茎、叶生长茂盛,叶色浓绿。某同学发现他家中花盆里的花草生长迟缓,便施用了一种氮肥。如图是该氮肥包装标签的部分文字。试根据相关信息回答:
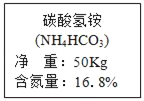
(1)这种化肥共含有_____种元素。
(2)碳酸氢铵的相对分子质量是_____。
(3)碳酸氢铵分子中各元素的原子个数比(即N:H:C:O)为_____。
(4)这种氮肥的纯度(即化肥中碳酸氢铵的质量分数)是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属和金属材料在生产、生活中有广泛的用途,请用金属的有关知识填空。
(1)锂电池可作为无人机的动力,其工作原理是:FePO4+Li![]() LiFePO4.在LiFePO4中锂元素显+1价,磷元素显+5价,则铁元素的化合价是_____。
LiFePO4.在LiFePO4中锂元素显+1价,磷元素显+5价,则铁元素的化合价是_____。
(2)钛(Ti)具有硬度大,密度小,熔点高,抗腐蚀性能好等优良性能,被誉为“未来金属”。已知Ti2(SO4)3溶于水溶液呈紫色。Ti2O3(紫黑色固体)在加热条件下可溶于硫酸,生成Ti2(SO4)3.可观察的现象是_____,反应的化学方程式为_____。
(3)工业上,用一氧化碳和赤铁矿炼铁的化学方程式为_____,计算用1000t含氧化铁80%的赤铁矿石,理论上能冶炼出铁的质量为_____t。
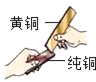
(4)黄铜片(铜锌合金)与铜片互相刻划时,(如图所示),纯铜片上留下明显的划痕,说明_____;
将它们分别放入稀硫酸中能产生气泡的是_____;涉及的化学反应可用化学方程式表示为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】认识溶液的变化。根据如图甲、乙、丙三种固体的溶解度曲线回答:
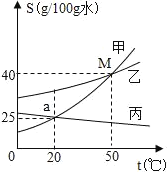
①M点表示的含义是_____。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为_____。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数_____(填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】向两支试管中分别加入2毫升蒸馏水,然后各滴入1到2 滴石蕊溶液,观察试管中溶液的颜色。将其中一支试管静置。向另一支试管中通入二氧化碳,观察现象,并与静置的试管中溶液的颜色进行对比。将通入二氧化碳的试管放在酒精灯火焰上加热,观察现象。
(1)证明水不能使石蕊溶液变色的实验操作及现象是_________。
(2)该实验证明二氧化碳和水反应生成了______,能使石蕊溶液变_____。
(3)加热涉及的反应化学方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀
盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.

(1)反应中生成二氧化碳质量;______
(2)通过计算说明每片钙片实际钙含量。说明是否与标注相符?______
(3)试计算所用稀盐酸的溶质质量分数.______
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在进行碳酸钠与酸反应的实验中,发现了一个有趣的现象。当把盐酸溶液逐滴加入到碳酸钠溶液中,开始没有气体产生,一段时间后才有气体产生。查阅资料得知,碳酸钠与盐酸溶液存在两个反应:Na2CO3+HCl═NaHCO3+NaCl;NaHCO3+HCl═NaCl+H2O+CO2↑.他又进行了以下实验:向等体积、含等碳原子数的碳酸氢钠溶液和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,并测得pH与时间的关系,如图甲、乙所示。他们将图甲和图乙的阴影部分进行叠加,发现两者基本重合。
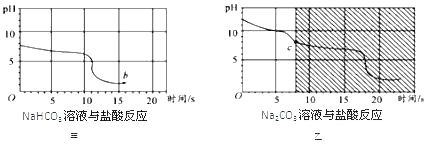
(1)结合图象分析,当把盐酸溶液逐滴加入碳酸钠溶液中,开始没有气体产生的原因是_____。
(2)图甲b点的溶质为_____(写化学式)。
(3)在本实验中加入足量的盐酸产生二氧化碳的量_____。
A 碳酸氢钠多 B 碳酸钠多 C 两者一样多
查看答案和解析>>
科目: 来源: 题型:
【题目】(12分)氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图10所示(固定装置省略)。
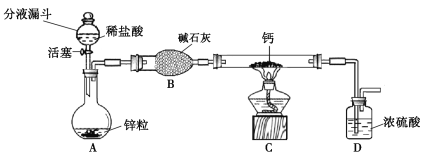
图10
回答下列问题:
(1)装置A中制取氢气的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中制取氢化钙的化学方程式为 。
(4)若不改变温度,整套装置气密性的检查方法是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图11(固定装置省略)所示连接仪器。
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化钙的纯度为 。(结果精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】2008年5月12日,四川汶川发生了里氏8.0级地震,全国人民抗震救灾,众志成城。为确保大地震之后无大疫,卫生部门用优氯剂、漂白粉等对饮用水等进行消毒。
(1)漂白粉的有效成分是Ca(ClO)2,氯元素的化合价是 。
(2)ClO2 是新一代饮用水的消毒剂,我国成功研制出制取ClO2 的新方法,其反应的微观过程图如下:
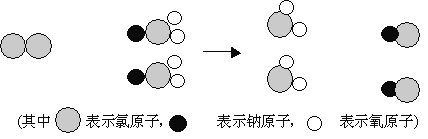
试回答:
ClO2 中氯元素的化合价为 ;
根据反应的微观过程图写出反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com