
科目: 来源: 题型:
【题目】升温、增大浓度、加大压强和使用催化剂均可以提高化学反应速率。现把镁条投入盛有稀盐酸的试管中,试管外璧发烫。产生氢气的速率变化情况(v)和反应进行的时间(t) 的关系如图所示,则下列说法错误的是( )
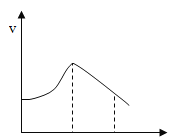
A. 反应过程中溶液的pH逐渐增大 B. t1~t2速率变化的主要原因是反应物的量较多
C. t2~t3速率变化的主要原因是盐酸的浓度逐渐减小 D. t1~t2速率变化的主要原因是反应放热使溶液温度升高
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象能正确反映其对应实验操作的是( )
|
|
|
|
A.高温煅烧一定质量的石灰石 | B.用等质量、等浓度的双氧水分别制取氧气 | C.向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 | D.某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是( )
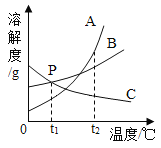
A.t 2℃时,A、B、C三种物质中,A物质的溶解度最大
B. P点表示t 1℃时B、C两物质的溶解度大小相等,该温度下B、C饱和溶液中所含溶质质量相同
C.t 1℃时,给A、B、C三种物质的饱和溶液加热(不考虑溶剂的蒸发),有晶体析出的是C物质
D.从A、B的混合物中提取A应采用降温结晶
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组在制取氧气的实验过程中,有如下实验设计方案,该方案的实验目的是:探究氯酸钾和二氧化锰的质量比对反应速率的影响。
编号 | 温度 | 催化剂 | 氯酸钾、二氧化锰的质量比 | 生成1升氧气所需时间/s |
实验Ⅰ | 400℃ | MnO2 | 1:1 | 153 |
实验Ⅱ | 400℃ | MnO2 | 2:1 | 240 |
小芳在实验时,误把氧化铜当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
猜想Ⅰ:除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂。
(设计实验)按下表进行实验,并测定开始产生气体时的温度(提示:开始产生气体的温度越低,表示反应速度越快)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾和二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾和氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾和氧化铁(质量比1︰1) | 390 |
(数据和结论)
(1)由实验_______与实验④对比,证明猜想合理;
(2)实验所用的三种物质中,催化效果最好的是_______。
(反思)
若要证明氧化铁是该反应的催化剂,还需验证它在化学反应前后的________和_______是否改变。
猜想Ⅱ:过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应可制取氧气。
(分析与反思)
同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气
你认为猜想______(填序号)一定是错误的,理由是________,过氧化钙与水反应虽然没有快速收集到大量氧气,但过氧化钙在水中持续、缓慢放出氧气,因此小林认为渔民用过氧化钙做增氧剂。写出此反应的符号表达式________。
(计算)
该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示。试计算:

(1)过氧化钙的相对分子质量为_______
(2)该产品中过氧化钙的质量分数至少为______。
(3)小组同学将3g某物质在制得的足量氧气中充分燃烧生成4.4g二氧化碳和1.8g水,求该物质中各元素的原子个数比(写出计算过程)。______
查看答案和解析>>
科目: 来源: 题型:
【题目】一碳化学是以分子中只含有一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学,合成气(CO、H2)可通过甲烷(CH4)的重整得到,例如CH4+H2O=CO+3H2。合成气可制取21世纪的新型燃料二甲醚。请阅读以下生产流程,回答问题:

(1)铜绿[化学式为Cu2(OH)2CO3]是由______种元素组成的,其中碳元素、氧元素的质量比为_______,其产物CuO中铜元素的化合价是_______。
(2)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得。用合成气制二甲醚时,还产生了水,写出该反应的符号表达式:_______。
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。仅用合成气为原料不可能得到的物质是_______ (填字母序号)。
A草酸(H2C2O4)
B甲醇(CH3OH)
C尿素[CO(NH2)2]
查看答案和解析>>
科目: 来源: 题型:
【题目】根据所学的知识并结合下列仪器,回答有关问题。
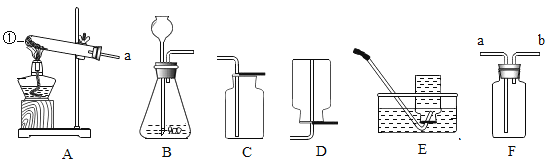
(1)仪器①的名称是________。
(2)实验室用高锰酸钾制取氧气,可选用的发生装置是______,该反应的符号表达式为_______,该反应的基本反应类型是______(填“化合反应”或“分解反应”),若用E来收集一瓶纯净的氧气,实验结束时应该先_______(填“移出导管”或“熄灭酒精灯”)。
(3)实验室用过氧化氢溶液制取并收集氧气应选用的装置组合是______,若用F装置(装置内没有水)来收集氧气,则气体应从________(填“a”或“b”)进入F中,当选用E装置收集完气体后,测得其纯度明显偏低,原因可能是______(填序号)
A高锰酸钾中混入了二氧化锰 B收集前,集气瓶中未注满水
C收集后,集气瓶中仍有少量水 D未见气泡连续均匀冒出时就开始收集
(4)利用如图的装置,可以粗略测定出空气中氧气的体积分数。实验过程如下:
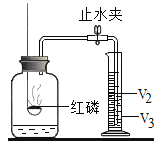
第1步:在一个容积为V毫升的集气瓶中加入V1毫升(少量)的水,量筒中预先装入V2毫升的水。
第2步:点燃燃烧匙内的红磷,并迅速伸入集气瓶中再塞紧塞子。
第3步:待反应结束并冷却后,松开止水夹。此时水进入集气瓶,最终量筒中的水面停止在刻度V3毫升处。
请回答下列问题:
①在此设计方案中,红磷燃烧的符号表达式是___________。
②实验中红磷必须要过量,目的是:__________。
③该方案中计算空气中氧气的体积分数的数学表达式为:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某物质由碳、氢、氧三种元素组成,下图为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是

A. 该物质由碳原子、氧原子、氢原子构成
B. 该物质化学式可表示为CH6O2
C. 分子中碳、氢、氧三种原子个数比为2:6:1
D. 该物质相对分子质量为105
查看答案和解析>>
科目: 来源: 题型:
【题目】镓(Ga)是灰蓝色或银白色的金属,主要用于电子工业和通讯领域,是制取各种镓化合物半导体的原料。下图是元素周期表中提供的镓元素的部分信息及镓原子的结构示意图。下列有关说法错误的是
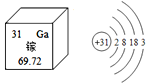
A. 镓元素位于第四周期,其原子核外共有31个电子
B. 镓元素属于非金属元素,镓原子在化学反应中容易得到电子
C. 镓的相对原子质量为69.72,原子核内质子数为31
D. 氧化镓的化学式为Ga2O3,其中镓元素的化合价为+3价
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组研究“影响H2O2 生成O2快慢的因素”的课题。通过查阅资料,他们提出如下猜想。
(提出猜想)催化剂和反应物浓度都会影响H2O2 生成O2 的快慢
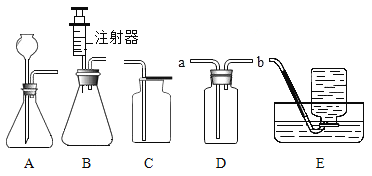
(实验过程)实验装置图如下:
实验操作:检查装置气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。实验记录
实验编号 | ① | ② | ③ |
反应物 | 5%H2O2 100 mL | 5%H2O2 | 3%H2O2 100 mL |
加入固体 | 0.5 g氯化钠固体 | 0.5 g二氧化锰 | |
收集气体的时间 | 165 s | 46 s | 80 s |
(1)实验②中加入H2O2的体积为_________mL。
(2)实验③中加入的固体和用量为___________。
(结论)该探究过程得出的结论是 ___________。
(反思)H2O2在常温下分解缓慢,加入MnO2 后反应明显加快。小红提出,为了更好的证明二氧化锰和氯化钠是否对H2O2 生成O2快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为______。
(实验拓展)小红用排水法收集的气体进行氧气的性质实验。
(1)小红进行硫磺和氧气的反应的性质实验时,在空气中与在氧气中对比燃烧,现象差别不明显。造成这种结果的原因是_________________。
(2)为探究影响过氧化氢分解速度的因素,小雨阅读课外资料得知:过氧化氢分解除了用二氧化锰,还可用氧化铜等物质作催化剂。于是在室温下做了如下实验,实验数据记录如下:
过氧化氢的质量 | 过氧化氢的浓度 | CuO的质量 | 相同时间内产生O2体积 | |
Ⅰ | 100.0g | 1% | 0.0g | 5 mL |
Ⅱ | 100.0g | 1% | 2g | 32 mL |
Ⅲ | 100.0g | 4% | 2g | 64 mL |
①本实验中,测量O2体积的装置是________(填编号)。
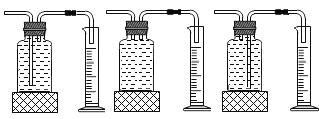
②通过对上表数据分析,I和II对比影响过氧化氢分解速率的因素是__________;III和II对比影响过氧化氢分解速率的因素是______
③写出该反应的文字表达式__________
④小雨进认为只根据加入CuO在反应中的现象还不能确定其为催化剂,还需验证__
⑤小雨利用上述原理制氧气,若达到可随时控制生成气体的速度的目的,应选择的发生装置________填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置图回答问题。
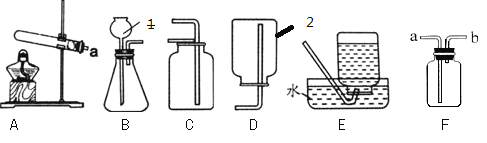
(1)标号仪器1的名称是____________ ,仪器2的名称是_________
(2)实验室加热高锰酸钾制取氧气并用排水法收集的主要操作步骤:①点燃酒精灯,先使试管受热均匀,然后对准试管中的药品部位加热;②将药品装入试管,用带导管的单孔橡皮塞塞紧试管;③收集完毕,将导管从水槽中取出;④检查装置的气密性;⑤用排水法收集氧气;⑥将试管固定在铁架台上;⑦熄灭酒精灯.
①正确的操作顺序是_______________
A ①②③④⑥⑤⑦ B ①⑥③②⑤④⑦ C ④②⑥①⑤③⑦ D ②③⑦①⑤④⑥
②该反应的文字表达式________________
③检验A装置气密性的操作__________________
④将药品装入试管后,在试管口塞棉花团的目的_____________
⑤A装置试管口为何斜朝下_____________
⑥收集氧气可以选取的收集装置 ____________ ,哪种方法收集的气体更纯______,假如使用F装置收集氧气,瓶中盛满空气,气体应从_____端通入。
⑦实验操作过程要注意先后顺序,如先检验装置气密性,再放药品,当实验完毕,拿出导气管,熄灭酒精灯的先后顺序___________,这样操作的原因______________
(3)通常状况下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室常用加热氯化铵和消石灰的固体混合物制取氨气,请完成下列问题:实验室制取氨气的发生装置应选择的发生装置是________;收集氨气,应采用的装置是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com