
科目: 来源: 题型:
【题目】在如图有关物质转化关系中,各物质均是初中化学常见的物质.其中A是紫红色金属,B、C组成元素相同,I是某建筑材料的主要成分,将F溶液倒入K的乳状物中搅拌后即配成农业上常用的杀菌剂波尔多液(图中反应条件已略去)
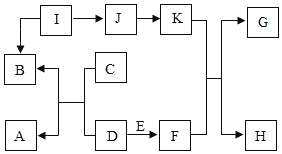
(1)I的化学式_____;
(2)由J转化为K的基本反应类型为_____.
(3)写出C与D反应的化学方程式_____;写出K与F反应的化学方程式_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
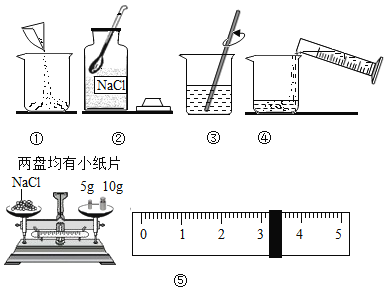
(1)用上图表示的序号表示配制溶液的正确操作顺序__________。
(2)图②中,有一种塑料仪器,其名称是______________。
(3)根据计算需要量取水的体积是_____________(水的密度为1 g/mL)。量取所需要的水应选择__________(选填“50 mL”、“100 mL”或“200 mL”)量筒。量取读数时,下图视线角度正确的是______________。 (选填字母标号)
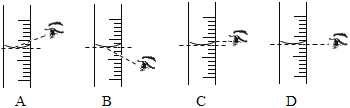
(4)溶解:用量筒量取所需的水,倒入装有氯化钠固体的烧杯里,用玻璃棒搅拌,其目的是______________。
(5)在配制过程中,能导致溶液中NaCl 质量分数小于10%的可能的原因是______________。
①用量筒量取水时仰视读数 ②向烧杯中倒NaCl时洒了一些 ③配制溶液的烧杯用水洗涤后未干燥就使用 ④氯化钠晶体不纯
A①②③④ B只有①③④ C只有①②③ D只有②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】重大科技创新成果是国之重器、国之利器,必须牢牢掌握在自己手上。2018年5月,由我国自主研发的航空母舰002号正式出海试车,标志着“中国制造”取得重要的技木突破。
(1)建造航母用到了钛合金,钛合金属于_________(填“纯净物”或“混合物”),工业制钛有一种反应为![]() ,X的化学式为______________。
,X的化学式为______________。
(2)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,主要利用了它们具有_________等性能(填字母)。
A熔点高、密度小、机械性能好
B熔点低,硬度大、韧性好
(3)航母外壳用涂料覆盖,是为了防止钢铁材料与____________接触而锈蚀。下列措施中哪一项不能有效防止金属锈蚀?___________(填字母序号)
A在金属表面刷漆
B制成耐腐蚀的合金
C用洗涤剂把金属制品表面油膜冼净
(4)航空母舰的动力由柴油燃烧提供,柴油是通过一种化石燃料提炼得到,写出化石燃料天然气的主要成分甲烷燃烧的化学方程式______________。
(5)某合金中含有金属(Sc),相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性Sc__________Zn(填“>”或“<”)。为探究Sc、Fe、Cu三种金属活动性顺序,某同学选用了下列药品进行实验,其中不可行的是______________。
AFe、Sc、盐酸、Cu(NO3)2溶液
BSc(NO3)2溶液、Cu(NO3)2溶液、Fe丝
CSc、Fe(NO3)2溶液、Cu丝
DFe(NO3)2溶液、Sc(NO3)2溶液、Cu丝
查看答案和解析>>
科目: 来源: 题型:
【题目】原子结构与元素的性质和物质的组成密切相关,请将答案填写在下面的横线上:
(1)镁原子的结构示意图为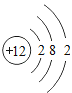 ,其在化学反应中易___________(填“得到”或“失去”)电子,其离子符号是____________ 。
,其在化学反应中易___________(填“得到”或“失去”)电子,其离子符号是____________ 。
(2)钠元素与氯元素组成的化合物是__________(化学式),构成该物质的微粒是__________(选填“分子”、“原子”、或“离子”)。
(3)与元素化学性质关系最密切的是____________(填字母编号)。
A元素的相对原子质量
B元素的核电荷数
C原子的核外电子数
D原子的最外层电子数
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是__________(填字母编号)。
A构成它们的原子大小不同
B构成它们的原子数目不同
C金刚石、石墨由不同种原子组成
D金刚石、石墨里碳原子排列方式不同
(5)铅元素相关信息如图所示。下列说法中正确的是___________。

A铅原子核内有82个质子
B相对原于质量为207.2 g
C铝有毒,儿童不能使用铅笔
D铅不能与稀硫酸反应,产生氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室通常用澄清石灰水检验二氧化碳的存在,若二氧化碳过量,会进一步与碳酸 钙、水反应生成易溶于水的碳酸氢钙(CaCO3+H2O+CO2═Ca(HCO3)2)。若向含有 Ca(OH)2 7.4g 的澄清石灰水里缓缓通入一定量的二氧化碳,反应后若生成 5g 沉淀,则通 入二氧化碳的质量可能为( )
A.2.2gB.4.4gC.6.6gD.13.2g
查看答案和解析>>
科目: 来源: 题型:
【题目】有等质量的镁和锌,前者放入质量分数为10%的稀盐酸中,后者放入质量分数为10%的稀硫酸中,产生氢气的质量随时间变化曲线如图所示。下列说法正确的是( )
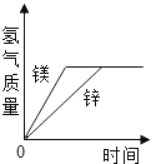
A. 锌一定没有剩余
B. 消耗的稀盐酸和稀硫酸质量之比为73:98
C. 最终产生氢气的质量相等
D. 消耗镁的质量与消耗锌的质量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示为X、Y、Z三种固体物质(不含结晶体水)的溶解度曲线,下列说法不正确的是
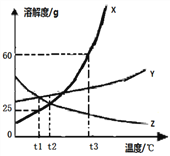
A. X中含有少量Y,应采用降温结晶的方法提纯X
B. t2℃时,三种物质的溶解度的大小关系是Y>X=Z
C. t3℃时,将X溶液降温到t1℃,X溶液的溶质质量分数变小
D. t3℃时,将等质量X、Y、Z的饱和溶液分别降温到到t1℃,所得溶液质量大小关系是Z>Y>X
查看答案和解析>>
科目: 来源: 题型:
【题目】20℃时,将等质量的甲、乙两种不与水反应的固体物质(不含结晶水),分别加入到盛有100g 水的烧杯中,充分搅拌后现象如图1,加热到 50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.则下列说法中错误的是( )
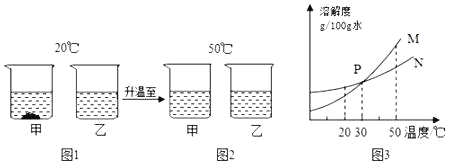
A. 图1中乙的溶液可能是不饱和溶液
B. 图2中两溶液溶质质量分数一定相等
C. 图3中 M表示的是甲的溶解度曲线
D. 图2中两溶液降温至30℃都会析出晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象中,能正确反应对应变化关系的是( )
A.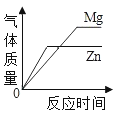 向等质量的镁和锌中分别加入足量等体积等质量分数的稀硫酸
向等质量的镁和锌中分别加入足量等体积等质量分数的稀硫酸
B.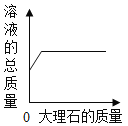 向一定量的稀盐酸中加入大理石
向一定量的稀盐酸中加入大理石
C.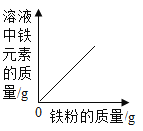 向一定量的稀盐酸中加入铁粉
向一定量的稀盐酸中加入铁粉
D.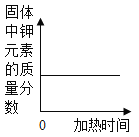 加热一定量的高锰酸钾固体
加热一定量的高锰酸钾固体
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸镁水合物是制备镁产品的中间体。
(制取MgCO33H2O)工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO33H2O的方法如图:
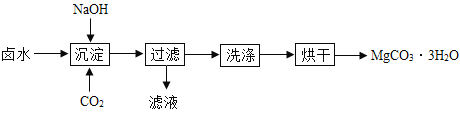
(1)沉淀过程的化学方程式为:MgCl2+CO2+2NaOH+2H2O═MgCO33H2O↓+2___。
(2)沉淀过程的pH随时间的变化如图所示,沉淀过程的操作为____(填标号)。
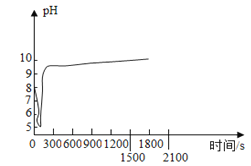
a 向卤水中滴加NaOH溶液,同时通入CO2
b 向NaOH溶液中滴加卤水,同时通入CO2
c 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
d 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
(3)沉淀过程的溶液中镁离子含量随时间的变化如图所示,不同温度下所得到沉淀产物如下表所示。
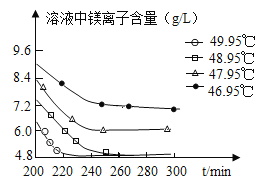
温度(℃) | 产物 |
46.95 | MgCO33H2O |
47.95 | MgCO33H2O |
48.95 | MgCO33H2O |
49.95 | Mg5(OH)2(CO3)44H2O |
则沉淀过程选择的温度为____℃,理由是此温度下,Mg2+沉淀的速率较快,沉淀效率较高,且不会生成其它沉淀。
(测定MgCO33H2O的纯度)
(查阅资料)
1.碱石灰是CaO与NaOH的固体混合物。
2.MgCO33H2O+H2SO4=MgSO4+CO2↑+4H2O。
3.Mg5(OH)2(CO3)44H2O也可以表示为Mg(OH)24MgCO34H2O,其相对分子质量为466,能与硫酸反应生成CO2。
4.Ba(OH)2能溶于水
(实验步骤)
利用如下图所示装置(图中夹持仪器略去)进行实验,以确定MgCO33H2O的纯度。
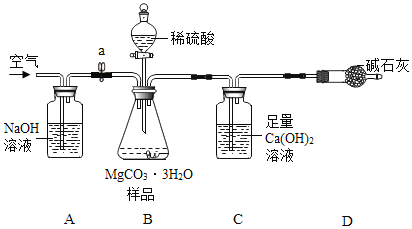
依据实验过程回答下列问题:
(1)A中NaOH溶液的作用是________。
(2)C装置中反应生成CaCO3的化学方程式为_____;D中碱石灰的作用为___。
(3)下列各项措施中,不能提高测定准确度的是____(填标号)。
a 在加入硫酸之前,应排净装置内的CO2气体
b 为了缩短实验时间,快速滴加硫酸
c 在A~B之间增添盛有浓硫酸的洗气装置
d 在C装置左侧导管末端增添多孔球泡
(4)小明认为应将C装置中澄清石灰水换成Ba(OH)2溶液,理由一:___,使CO2被吸收的更完全;理由二: BaCO3的相对分子质量比CaCO3大,等质量的MgCO33H2O生成的BaCO3质量大于CaCO
(5)实验中准确称取15.0g样品三份,进行三次测定,测得生成CaCO3沉淀的平均质量为10.0g。请计算样品中MgCO33H2O的纯度(写出计算过程)____。
(6)若获取MgCO33H2O的样品中含有少量Mg5(OH)2(CO3)44H2O,则样品中MgCO33H2O的纯度____(填“偏大”“不变”或“偏小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com