
科目: 来源: 题型:
【题目】如图是氢分子(H2)和氧分子(O2)运动的示意图。根据图回答:
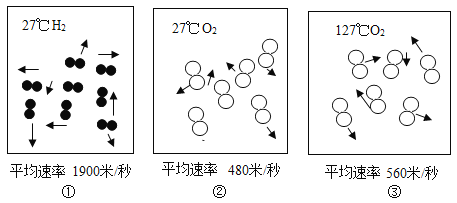
(1)仔细观察上述粒子运动的示意图,分子运动速率最快的是_____(填序号)。
(2)在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是_____(填序号)。
(3)从图中可见,影响分子运动速率的因素除温度外,还与_____有关。
(4)举一个能说明“温度升高,分子运动速率加快”的生活实例_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种有趣的钟表式元素周期表如图所示,关于时针所对应的元素说法中不正确的是
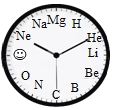
A.12:00 对应的元素为金属元素
B.10:00 对应的元素不易形成化合物
C.9:00 对应![]() 元素的离子符号为 F+
元素的离子符号为 F+
D.该钟表的整点时间与原子结构中的质子数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】铝合金是汽车制造中的重要材料之一,查阅资料可知:氢氧化铝沉淀可与氢氧化钠溶液反应,产生可溶性的偏铝酸钠,反应如下: ![]() 。某学习小组取7.8 g该合金粉末加入200.0g过量的盐酸中(假设合金中的其他成分不参与反应),向充分反应后的物质中加入过量20.0%的氢氧化钠溶液。整个实验过程的数据如图所示:
。某学习小组取7.8 g该合金粉末加入200.0g过量的盐酸中(假设合金中的其他成分不参与反应),向充分反应后的物质中加入过量20.0%的氢氧化钠溶液。整个实验过程的数据如图所示:
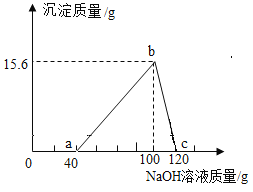
根据图示回答以下问题:
(1)b点时,溶液中的溶质为____________(写化学式)。
(2)该合金中铝的质量为____________g。
(3)加入盐酸的溶质质量分数为____________? (请写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇俗称酒精,是一种有机物,分子式为C2H5OH,在汽油中加入适量乙醇作为汽车燃料,可以节省石油资源并适当减少汽车的尾气污染。某同学为了探究一定量乙醇在空气中燃烧的产物进行了如下探究:
[提出问题]乙醇燃烧的产物是什么? .
[猜想假设]猜想1:含有H2O、CO2;猜想2:含有 H2O、CO;猜想3:含有________________。
[设计实验](1)小明同学点燃刚加入纯净酒精的酒精灯,将干冷的烧杯罩在酒精的火焰上方,观察到_____________,证明有水生成。
(2)小明再将涂有饱和石灰水的小烧杯罩在火焰上方,观察到石灰水变浑浊,证明猜想2不成立。
[交流讨论]小芳同学认为[设计实验](2)中石灰水变浑浊不一定生成碳酸钙,还可能的原因是_______________。
[继续探究]小芳为探究乙醇燃烧的生成物除了水之外,还有什么物质,她将4.6g乙醇和8 g氧气置于完全密闭的容器中引燃,恰好完全反应后依次通入如图所示装置中(假设装置气密性良好,各装置的吸收剂足量) ,并称得反应前后各装置的质量,如下表:
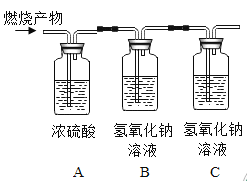
装置 | A装置 | B装置 | C装置 |
通入前的质量/g | 30 | 30 | 30 |
通入后的质量/g | 35.4 | 34.4 | 30.2 |
(1)C装置的作用是______________。
(2)根据以上数据可推测出猜想_____________成立。
查看答案和解析>>
科目: 来源: 题型:
【题目】兴趣小组的同学为探究碳酸钠的性质做了如下实验,请你一起完成。
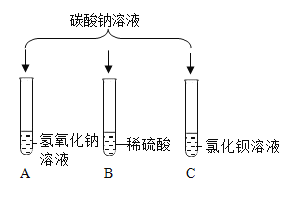
(1)试管A中没有发生反应,原因是__________________。
(2)试管B中的现象是_________________;试管C中发生反应的化学方程式为________________。
(3)上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同--烧杯中,然后过滤得到滤液①,为确定滤液①的成分,同学们做了如下实验探究:
实验操作 | 实验现象 | 实验分析 | |
(4) | 取少量滤液①于试管中,向其中加入足量的氯化钡溶液,过滤,得到沉淀和滤液②, 向沉淀中加入足量稀硝酸 | 产生白 色沉淀; 加入稀硝酸后白色沉淀部分消失 | 根据实验现象可知,滤液②中一定含有_______________(填写溶质的化学式) |
(5) | 取少量滤液②于试管中,________________。 | ____________。 | 根据实验现象可知,滤液①中一定含有氢氧化钠 |
[实验结论](6)同学们通过分析推理,得出结论:滤液①中共含有_______________种溶质。
[实验反思](7)向滤液①中加入足量的氯化钡溶液的目的是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验室制取和收集气体的装置图,据图回答问题。

(1)写出仪器①的名称_______________。
(2)实验室用氯酸钾和二氧化锰制取并收集一瓶干燥的氧气, 选择的发生及收集装置是______________(填字母序号) ;若实验室利用图中装置制取并收集二氧化碳,请写出检验二氧化碳已收集满的方法______________。
(3)制取气体前应先检查装置的气密性,若按F图示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是________________________(填字母序号)。
a将烧杯换成水槽
b装置气密性不好
c先用手捂住试管壁,再将导管另一端插入水中
(4)实验室常用碳化钙(块状固体,化学式为CaC2 )与水反应制取乙炔( C2H2)气体,同时生成一种白 色固体。
①已知碳化钙与水的反应非常剧烈。欲制取乙炔气体,要求做到节约、安全、可控制反应速率,你选择的发生装置是__________(填序号)。
②同学们想确定生成乙炔气体的反应原理,于是对生成的白色固体的成分进行了以下探究:
[提出猜想]甲同学:白色固体是氧化钙;
乙同学:白色固体是氢氧化钙;
丙同学:白色固体是碳酸钙。
[讨论交流]同学们讨论后认为甲同学的猜想错误,原因是_____________。
[实验过程及结论]同学们取该一定量白色固体加入试管中,向其中加人足量稀硫酸,观察不到明显现象,由此可知实验室中制取乙炔的反应原理为_____________(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~H是初中化学常见的八种物质,它们之间的关系如图所示(图中 “→”表示转化关系,“一 ”表示相互能反应;部分反应物、生成物及反应条件未标出)。A、F 、G、H属于不同类别的物质,F可以用于改良酸性土壤,D、E是元素组成相同的物质,B、C、G均为常见气体。
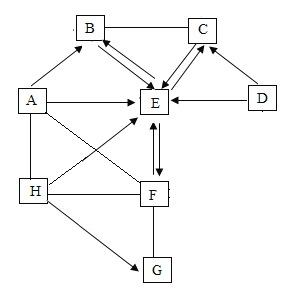
(1)E、G的化学式分别为_________________、________________。
(2)写出H与F反应的化学方程式__________________;从微观的角度分析,A与F反应的实质是_____________。
(3)B转化为E的过程中,体现出B物质的___________性。
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体可能含有铁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探究其组成成分,某化学兴趣小组进行了如下实验:取一定量该固体样品,加入足量的水溶解,经过滤后可得到滤液A和滤渣甲。现对滤液A和滤渣甲进行如下操作:
①向滤液A中加入过量的硝酸铜溶液得到溶液B,此过程中观察不到明显现象。再向溶液B中加入一定量硝酸银溶液,观察到有白色沉淀生成,过滤后可得到白色滤渣乙和滤液C。
②向滤渣甲中加入过量的稀盐酸,经过滤后可得到滤液D和滤渣丙,将滤渣丙在空气中充分灼烧,发现仍有固体物质残留。
请回答下列问题:
(1)该实验中生成白色沉淀滤渣乙的化学方程式为_________________。
(2)滤液D中一定含有_________________。
(3)原固体中一定不含有的物质是_______________,证据是__________________;原固体中一定含有的物质是_______________。
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,已知上层清液E中不含氯离子,则E中一定含有的溶质是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】烟台有漫长的海岸线,海洋蕴藏着丰富的资源,请按要求回答问题。
(1)海洋为我们提供了营养丰富的食材。鱼虾富含的______________是机体生长及修补受损组织的主要原料;海带富含的______________可以预防甲状腺肿大。
(2)海水碳储存可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减小,同时软体生物的贝壳也在逐渐软化、变薄和缩小。“海洋酸化”的原因可用化学方程式表示为__________________。
(3)从海水可制备纯碱,其流程如图1所示:

①粗盐水中主要含有的可溶性杂质是CaCl2、MgSO4,可加入下列物质:a.适量的盐酸;b. 过量的Na2CO3溶液;c.过量的Ba(OH)2溶液,利用过滤等操作进行除杂,则加入这三种物质的先后顺序为________________________(填字母)。
②向饱和氯化钠溶液中先后通入________________________,再经过一系列变化,最终可制得纯碱。请写出步骤Ⅲ发生反应的化学方程式________________________。
(4)利用如图2所示的流程从海水中提取金属镁:
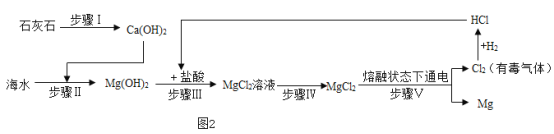
根据流程图判断,下列说法正确的是______________(填字母)。
A步骤I通过-步反应即可实现
B步骤Ⅱ、Ⅲ、IV的目的是从海水中提取氯化镁
C步骤Ⅲ发生了中和反应
D步骤V中化学能转化为电能
查看答案和解析>>
科目: 来源: 题型:
【题目】歼-20、大飞机、钻井平台等国之重器,向世界展示了中国制造的强大力量!
(1)我国生产的歼-20隐形战斗机发动机喷口、喷管的金属材料中加入了稀土金属铼(Re),可用KReO4来冶炼金属铼,请注明KReO4中铼元素的化合价________________________。
(2)由烟台中集来福士建造的钻井平台“蓝鲸1号”已成为可燃冰的开采神器。下列关于可燃冰的说法正确的是______________(填序号)。
①可燃冰储量巨大,是一种可再生能源
②可燃冰充分燃烧后几乎不产生任何残渣和废气
③可燃冰的热值大于汽油的热值
④甲烷无毒,因此不必关注开采造成的环境问题
(3)大飞机的燃料是航空煤油,是石油液化炼制的产品,是根据石油中各成分______________不同分离得到的;铝合金和碳纤维复合材料是制造飞机、火箭的常用材料,这主要利用了它们具有的共同性能是____________(填序号)。
①密度小、强度高
②密度大硬度大
③强度低 、硬度小
(4)载人航天器工作舱中的氧气可通过电解水产生。电解水时,氧气在电极的______________极产生。宇航员呼出的CO2用氢氧化锂(LiOH)吸收,已知氢氧化锂具有碱的通性,试用化学方程式表示出其吸收CO2的反应原理___________。航天器返回地面后,再利用Ca(OH)2与上述反应的产物之一作用,发生复分解反应,使_____________,再生。
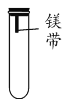
(5)镁被称为国防元素,镁带久置于空气中,表面会发生锈蚀而变暗,生成碱式碳酸镁 [ Mg2 (OH)2CO3,即带结晶水的碳酸镁和氢氧化镁的混合物]。欲通过实验探究镁带在空气中锈蚀是否与氧气有关,用如图所示装置,试管内可选用的物质如下:①O2和CO2;②CO2和水;③O2和水;④O2、CO2和水,需要选用_____________(填序号)才能完成实验。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com