
【题目】Fe2O3+2Al![]() Al2O3+2Fe所属基本反应类型是 。在该反应中 元素的化合价升高,该元素的原子 电子,被 。该反应中,Fe2O3发生了 反应,Al发生了 反应, 是氧化剂, 是还原剂, 是氧化产物, 是还原产物。
Al2O3+2Fe所属基本反应类型是 。在该反应中 元素的化合价升高,该元素的原子 电子,被 。该反应中,Fe2O3发生了 反应,Al发生了 反应, 是氧化剂, 是还原剂, 是氧化产物, 是还原产物。
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中地理 来源: 题型:
【题目】下图是元素周期表的简略框架图。
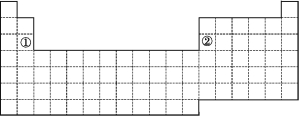
(1)请在上图所示的元素周期表中画出金属元素与非金属元素的分界线。按电子排布,可把元素划分成5个区,不全是金属元素的区为 。
(2)根据氢元素最高正化合价与最低负化合价的绝对值相等,你认为还可把氢元素放在元素周期表中的第 族;有人建议将氢元素排在元素周期表的第ⅦA族,请你写出支持这一观点的一个化学事实: 。
(3)上图中元素①②原子的价电子排布式分别为 、 。
比较元素①与元素②的下列性质(填“>”或“<”)。
原子半径:① ②;电负性:① ②;
金属性:① ②;第一电离能:① ②。
(4)某短周期元素最高正化合价为+7,其原子结构示意图为 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在稀硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、生石灰、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应。
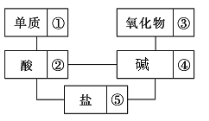
(1)请推断出它们的化学式分别为:
①_______; ②_______; ③________;④________; ⑤_______。
(2)写出下列序号之间反应的化学方程式:
①和②: ____________________________________________;
②和④: ____________________________________________;
②和⑤: ____________________________________________;
④和⑤: ____________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(1)常温时向水中加入少量固体MgCl2,________(填“促进”或“抑制”)了水的电离;与纯水相比,所得溶液中KW________(填“变大”“变小”或“不变”)。
(2)现有下列溶液:①20 mL 0.1 mol·L-1 H2SO4溶液;②40 mL 0.1 mol·L-1 CH3COOH溶液;③40 mL 0.1 mol·L-1 HCl溶液;④40 mL 0.1 mol·L-1 NaOH溶液;⑤20 mL 0.1 mol·L-1 Ba(OH)2溶液,其中:
A.c(H+)最小的是________(填序号)
B.任取2份溶液混合,混合溶液的pH为7,有________种取法。
C.②④混合后,溶液的pH________7(填“大于”“小于”或“等于”)。
D.混合后出现白色沉淀的两种溶液是________。(填序号)
(3)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。则:
①B是________溶液,C是________。
②常温下若B溶液中c(OH-)与C溶液中的c(H+)相同,B溶液的pH用pHb表示,C溶液的pH用pHc表示,则pHb+pHc=________(填数据)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC=![]() vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,vA=________,vB=________。
(2)化学方程式中,x=________,y=__________,p=__________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH________0。(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:
①反应速率________(填“增大”“减小”或“不变”),理由是____________________________。
②平衡时反应物的转化率________(填“增大”“减小”或“不变”),理由是_________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】和下列离子反应方程式相对应的化学方程式正确的是
A.Cu2++2OH===Cu(OH)2——CuCO3+2NaOH===Cu(OH)2↓+Na2CO3
B.Ba2++![]() ===BaSO4↓——Ba(OH)2+H2SO4===BaSO4↓+2H2O
===BaSO4↓——Ba(OH)2+H2SO4===BaSO4↓+2H2O
C.Ag++Cl===AgCl↓——AgNO3+NaCl===AgCl↓+NaNO3
D.Cu+2Ag+===Cu2++2Ag↓——Cu+2AgCl===2Ag+CuCl2
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】已知在相同条件下电离常数有如下关系:Ka1(H2CO3)>Ka(HBrO)>Ka2(H2CO3)。下列离子方程式或化学方程式中不正确的是
A.向NaHCO3溶液中滴加少量溴水:![]() +Br2
+Br2![]() HBrO+Br+CO2↑
HBrO+Br+CO2↑
B.向Na2CO3溶液中滴加少量溴水:2![]() +Br2+H2O
+Br2+H2O![]() BrO-+Br-+2
BrO-+Br-+2![]()
C.向NaBrO溶液中通入少量的CO2:CO2+NaBrO+H2O![]() NaHCO3+HBrO
NaHCO3+HBrO
D.向NaBrO溶液中通入足量的CO2:CO2+2NaBrO+H2O![]() Na2CO3+2HBrO
Na2CO3+2HBrO
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(OH)2被氧化的化学方程式为:________________________________。
为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时你觉得还需加入________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_________________________________。
(4)检验Fe3+存在的最佳试剂是____________,现象是______________________________________。
(5)写出Fe与H2O(g)在一定条件下反应的化学方程式:________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下图甲表示家族中某遗传病的发病情况,图乙是对致病基因(用A或a表示)的测定,已知控制性状的基因位于人类性染色体的同源部分,则Ⅱ-4的有关基因组成应是图乙中的
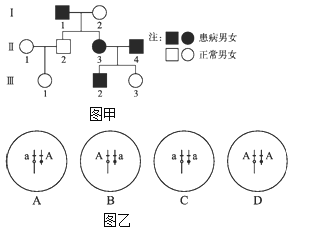
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com