
����Ŀ����1����Ҫ������������⣺
�� ���ĵ���ʽ_________��
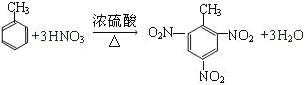
�� д���Ʊ�TNT�Ļ�ѧ����ʽ__________��
�� д��ʵ��������Ȳ�Ļ�ѧ����ʽ__________��
��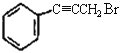 ���еĹ����ŵ�����Ϊ__________��
���еĹ����ŵ�����Ϊ__________��
��2��ij�л���Ľṹ��ʽΪ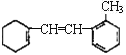 ���ݴ���д���пո�
���ݴ���д���пո�
�� �����ʱ�����һ�ȴ�����__________�֣�
�� lmol�����ʺ���ˮ��ϣ�����Br2�����ʵ���Ϊ__________mol��
�� lmol�����ʺ�H2�ӳ���H2__________mol��
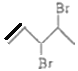
��3��![]() ��һ������Br2�����ӳɷ�Ӧ�����ɵIJ��������_______��
��һ������Br2�����ӳɷ�Ӧ�����ɵIJ��������_______��
A��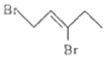 B��
B��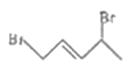
C��![]() D��
D��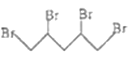
��4��ʵ��֤ʵ��ϩ�������Ը��������Һ����ʱ�����¹��ɣ�

��֪ij����ͨ������£�ֻ�ܸ������ʵ������巴Ӧ���������Ը��������Һ��Ӧʱ��������������ֻ��һ����û��֧������֪������ȫȼ��ʱ�����������������ͬ״������������8.5�����Է��������Ľṹ��ʽ________��
���𰸡�![]()
 CaC2+2H2O��Ca(OH)2+CH=CH�� ̼̼���� ����ԭ�� 4 2 5 B
CaC2+2H2O��Ca(OH)2+CH=CH�� ̼̼���� ����ԭ�� 4 2 5 B ![]()
��������
(1)�ټ���C��Χ��7�����ӣ���1�������ӣ��ڼױ���Ũ���ᡢŨ���ᷢ��ȡ����Ӧ����TNT����̼������ˮ��Ӧ�����������ƺ���Ȳ���ܸ��ݳ��������ŵĽṹ�������
(2)�ٸ����ʱ�������4����ԭ�ӣ��������м�����ԭ���䱽����һ�ȴ�����м��֣���̼̼˫�������ܷ����ӳɷ�Ӧ���۱�����̼̼˫���ܺ����������ӳɷ�Ӧ��
(3)![]() ��һ������Br2�����ӳɷ�Ӧ���ɷ���1��2�ӳɡ�1��4�ӳɻ���ȫ�ӳɷ�Ӧ��
��һ������Br2�����ӳɷ�Ӧ���ɷ���1��2�ӳɡ�1��4�ӳɻ���ȫ�ӳɷ�Ӧ��
(4)ij����ͨ�������ֻ�ܸ������ʵ������巴Ӧ������1��C=C˫����������ȫȼ��ʱ�����������������ͬ�������������8.5�������������ΪCxHy������ȼ�յ�ͨʽ��������x��y���������������������Һ��Ӧʱ�����õ�����������ֻ��һ����û��ȡ����ȷ���ṹ��ʽ��
(1)�ټ��ĵ���ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
�ڼױ���Ũ���ᡢŨ���ᷢ��ȡ����Ӧ����TNT����Ӧ�ķ���ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��̼����(CaC2)��ˮ��Ӧ������������[Ca(OH)2]����Ȳ���÷�Ӧ�ķ���ʽΪ��CaC2+2H2O��Ca(OH)2+CH��CH�����ʴ�Ϊ��CaC2+2H2O��Ca(OH)2+CH��CH����
�� 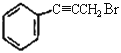 ���еĹ�������̼̼���� ����ԭ�ӣ��ʴ�Ϊ��̼̼���� ����ԭ�ӣ�
���еĹ�������̼̼���� ����ԭ�ӣ��ʴ�Ϊ��̼̼���� ����ԭ�ӣ�
(2)��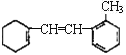 ��������4����ԭ�ӣ��������м�����ԭ���䱽����һ�ȴ�����м��֣������䱽����һ�ȴ�����4�֣��ʴ�Ϊ��4��
��������4����ԭ�ӣ��������м�����ԭ���䱽����һ�ȴ�����м��֣������䱽����һ�ȴ�����4�֣��ʴ�Ϊ��4��
��̼̼˫�������ܷ����ӳɷ�Ӧ��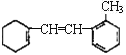 �к���2��̼̼˫��������1mol�����ʺ���ˮ��ϣ�����Br2�����ʵ���Ϊ2mol���ʴ�Ϊ��2��
�к���2��̼̼˫��������1mol�����ʺ���ˮ��ϣ�����Br2�����ʵ���Ϊ2mol���ʴ�Ϊ��2��
�۱�����̼̼˫�����ܺ����������ӳɷ�Ӧ���÷����к���һ������������̼̼˫��������1mol��������ȫ�ӳ���Ҫ5mol�������ʴ�Ϊ��5��
(3)![]() ��һ������Br2�����ӳɷ�Ӧ���ɷ���1��2�ӳɵõ�
��һ������Br2�����ӳɷ�Ӧ���ɷ���1��2�ӳɵõ�![]() ��
�� ��1��4�ӳɵõ�
��1��4�ӳɵõ� ������ȫ�ӳɵõ�
������ȫ�ӳɵõ�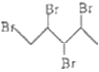 ��ֻ��B���ϣ��ʴ�Ϊ��B��
��ֻ��B���ϣ��ʴ�Ϊ��B��
(4)ij����ͨ�������ֻ�ܸ������ʵ������巴Ӧ������1��C=C˫�������������ΪCxHy��������ȫȼ��ʱ�����������������ͬ�������������8.5������x+![]() =8.5������������������Һ��Ӧʱ�����õ�����������ֻ��һ����û��ȡ���������ۿ�֪x=6��y=10�������ķ���ʽΪC6H10�����IJ����Ͷ�Ϊ2��������1�����������Ľṹ��ʽΪ
=8.5������������������Һ��Ӧʱ�����õ�����������ֻ��һ����û��ȡ���������ۿ�֪x=6��y=10�������ķ���ʽΪC6H10�����IJ����Ͷ�Ϊ2��������1�����������Ľṹ��ʽΪ![]() ����������Ľṹ��ʽΪHOOC(CH2)4COOH���ʴ�Ϊ��
����������Ľṹ��ʽΪHOOC(CH2)4COOH���ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W ��Ϊ���������ڷǽ���Ԫ�أ������£�������⻯��ˮ��Һ(Ũ�Ⱦ�Ϊ0.01 mol/L)�� pH ��ԭ�Ӱ뾶�Ĺ�ϵ��ͼ��ʾ������ X Ϊ��Ԫ�ء������й�˵����ȷ����
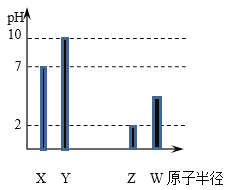
A.Y ����Ԫ��
B.ͼ�� Y ���⻯�ﲻ����X ���⻯�ﷴӦ
C.Z ������������Ӧˮ����Ļ�ѧʽΪ HClO4
D.W ������������Ӧˮ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
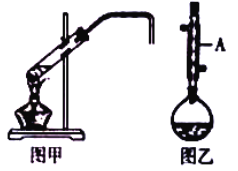
����Ŀ����ѧʵ��С������ʵ�����Ʊ������飨ͼ�ף���1���嶡�飨ͼ�ң����漰��ѧ��Ӧ���£�
NaBr+H2SO4�THBr+NaHSO4 ��
C2H5��OH+HBrC2H5��Br+H2O ��
CH3CH2CH2CH2��OH+HBrCH3CH2CH2CH2��Br+H2O ��
���ܴ��ڵĸ���Ӧ�У�����Ũ����Ĵ�������ˮ����ϩ���ѣ�Br����Ũ��������ΪBr2�ȡ��й������б����£�
�Ҵ� | ������ | ������ | 1���嶡�� | |
�ܶ�/gcm��3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
�е�/�� | 78.5 | 38.4 | 117.2 | 111.6 |
��ش��������⣺
��1��ͼ��������A������Ϊ_____��
��2���Ҵ��ķе����������ķе㣬��ԭ����_____��
��3����1���嶡��ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�������_____����ϲ㡱�����²㡱���ֲ㡱����
��4���Ʊ������У������Ũ����������ϡ�ͣ���Ŀ����_____��������ĸ��
A�����ٸ�����ϩ���ѵ�����
B������Br2������
C������HBr�Ļӷ�
D��ˮ�Ƿ�Ӧ�Ĵ���
��5������ȥ������е���������Br2���������������ʺϵ���_____��������ĸ��
A��NaIB��NaOHC��NaHSO3D��KCl
��6���Ʊ������飨ͼ�ף�ʱ�����ñ߷�Ӧ����������ķ�������������_____�����Ʊ�1���嶡�飨ͼ�ң�ʱȴ���ܱ߷�Ӧ�����������ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����þ�ڶ�����̼�е�ȼ�շ�Ӧ����Ϊ�ƺͶ�����̼Ҳ���Է�����Ӧ�����Ƕ�����CO2������ȼ�ս���������ʵ�飺
��1��������ͼװ���Ʊ�CO2������װ���з�Ӧ�����ӷ���ʽΪ_________��
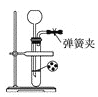
��2�����Ƶõ�CO2�������������a�ڻ���ͨ����ͼװ�ã���װ���еĿ����ž����ȼ�ƾ��ƣ��۲쵽����ֱ���е���ȼ�գ�����Ϊ��ɫ������ȴ�ܱڸ��к�ɫ�����Ͱ�ɫ���ʡ�
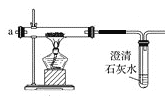
����˵��װ���п����Ѿ��ž���������_________��
����δ�ž������Ϳ�ʼ���ȣ�����ܷ����Ļ�ѧ��Ӧ����ʽ��ҪΪ_________��
��3�������Ż𣬿���ѡ�õ����������_________��
A��ˮ B����ĭ���� C����ɳ�� D��������̼
��4����С��ͬѧ�Թܱڵİ�ɫ���ʵijɷֽ������۲�������裺
������ɫ���ʿ�����Na2O�� ������ɫ���ʿ�����Na2CO3�� ������ɫ���ʻ�������_________��
��5��Ϊȷ���ð�ɫ���ʵijɷ֣���С�����������ʵ�飺
ʵ�鲽�� | ʵ������ |
��ȡ������ɫ�������Թ��У���������ˮ������Ʒȫ������ˮ�������мӹ�����CaCl2��Һ | ���ְ�ɫ���� |
������Ƭ�̣�ȡ�ϲ���Һ���Թ��У��μ���ɫ��̪��Һ | ���������� |
��ͨ��������ʵ��ķ���������Ϊ�������������У�___����������ţ���
����ʵ��ó�������CO2��ȼ�յĻ�ѧ����ʽΪ_____��ÿ����1mol�������ת�Ƶĵ�����Ϊ____��
��6����ʵ�飨2���л����ܲ�����һ��β����������Ϊ________��������β���ķ���Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D ���ֿ��������ʣ����ǵ������ӿ��ֱܷ���Ba2+��Ag+��Na+��Cu2+�е�ijһ�֣������ӿ��ֱܷ���NO3����SO42����OH����CO32���е�ijһ�֡�
������4�����ʷֱ��ܽ���ʢ������ˮ��4֧�Թ��У����ó�����Һ��ֻ��B��Һ����ɫ��
����������4֧�Թ��зֱ�����ᣬC��Һ���г���������A��Һ������ɫ��ζ�����ݳ���
��1�������٢�����ʵ�ƶ�B��C�Ļ�ѧʽ�ֱ�Ϊ_________��_________��
��2��д������ʵ����C������ķ�Ӧ��ѧ����ʽ��_________��
��3����A��Һ��D��Һ���ʹ֮ǡ����ȫ��Ӧ������Ӧ���������������ʷ���ķ�����_________����������Һ�м�����Ƭ�����������ӷ�Ӧ����ʽΪ��_________��
��4��A��ϡ���ᷴӦ���ɵ�����x���ſշ��ռ���������Ϊ8.96 L����״���£�������Ϊ15.2 g���û������ƽ��Ħ������Ϊ_________�����������x������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ⱦ�ϵ���Ҫԭ�ϣ�ijͬѧ��ʵ����������ͼ��ʾװ����ȡ����������Ҫ�������£�

���ڴ��Թ��ォ2 mLŨ�����1.5 mLŨ�����ϣ�ҡ�ȣ���ȴ��50��60 �����£�Ȼ����μ���1 mL�����ߵα����Թܡ�
�ڰ�ͼ���Ӻ�װ�ã������Թܷ���60 ���ˮԡ�м���10���ӡ�
���������գ�
(1)ָ����ͼ�еĴ���__________��____________��
(2)�������м��뱽ʱ������μ��롱���ߵα����Թܡ���Ŀ����__________________________��
(3)��Ӧһ��ʱ����Һ���Է�Ϊ���㣬�ϲ���Ҫ������________(����������)���ѷ�Ӧ��Ļ��Һ����ʢ����ˮ���ձ�����裬���Կ���________(����ĸ)��
a��ˮ�����Ǻ������ʵ�������
b��ˮ���п�����ζ��Һ��
c���ձ��е�Һ̬�л���ֻ��������
d������ɫ����״Һ�帡��ˮ��
(4)Ϊ�˻�ô���������ʵ�鲽�裺��ˮϴ����Һ���ڽ���������ת�Ƶ�ʢ��__________���ձ���ϴ�ӡ���__________(����������)���з��룻��__________���ܸ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��֬�ĽṹƬ����ͼ��ʾ�����й��ڸ���֬��˵������ȷ���ǣ� ����ͼ��~~~��ʾ���ӳ���
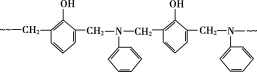
A.�ϳɸ���֬�ķ�ӦΪ���۷�Ӧ
B.�����Ϻϳɸ���֬��ԭ�ϱ�����ͬ
C.�ϳɸ���֬�ĵ���֮һ��ȩ���ɼ״������õ�
D.����֬������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�A�ǿ�����������ˮ���������Ļ���ɫ�������壬A��B��C��D��E����XԪ�أ���ת����ϵ��ͼ��ʾ��
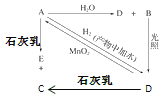
��1����ֱ�д���������ʵĻ�ѧʽ����Ϊ��Һ�������ʵĻ�ѧʽ����
A________��B________��D________��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ����ע����Ӧ��������
A��H2O�����ӷ���ʽ����_____________��
A��ʯ���飨��ѧ����ʽ����______________��
E¶���ڿ����еĵ�1����ѧ����ʽ��___________��
��3��Ư�۵���Ч�ɷ���________����ѧ���ƣ�������Ư�۵ķ���__________��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��������ʵ��ϵͳ�ⶨһ��Ũ��̼������Һ��pH���¶ȵĹ�ϵ���õ���ͼ��ʾ���ߡ����з�������ȷ����
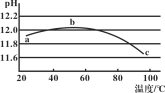
A.b����Һ��OH-Ũ�����������������
B.ˮ�ĵ���ƽ��Ҳ�����Һ��pH����Ӱ��
C.a��b��ˮ��ƽ�������ƶ�
D.a����Һ�Լ��ԣ�������Ũ�ȴӴ�СΪ��Na+>CO32->OH->HCO3-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com