
����Ŀ���縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ����ˮ������������������ˮ��pH��5.0~6.0֮�䣬ͨ���������Fe(OH)3���壬Fe(OH)3��������������ã�������ˮ�е������ʹ�������������ˮ�����ã���ԭ����ͼ��ʾ������˵����ȷ����

A. ʯī�缫�Ϸ���������Ӧ B. ͨ����ĵ缫��Ӧʽ��CH4+4CO32--8e-=5CO2+2H2O
C. ͨ�����ĵ缫��ӦʽΪO2+4e-=2O2- D. ����ȼ�ϵ����CO32-�����һ���ƶ�
���𰸡�B
��������
��װ�����Լ���ȼ�ϵ��Ϊ��Դ������ˮ���е��������ݼ���ȼ�յ�ԭ����ͨ�����һ��Ϊ������ͨ������һ��Ϊ�������������缫Ϊ������ʯīΪ���������ݵ缫�Ϸ����ķ�Ӧ�������Һ���������ӵ��ƶ�������н��
A�����ݼ���ȼ��ʱ���ϼ۵ı仯�������֪�����е�CԪ�ػ��ϼ����ߣ�ʧȥ���ӣ������ڸ�������������Ӧ����֮�����ӵ�ʯīΪ������������ԭ��Ӧ������A����
B�������ڵ�̼����Ϊ����ʣ���ͨ����ĸ�����ӦΪCH4+4CO32--8e-=5CO2+2H2O������B��ȷ��
C����װ��ͼ������Ϣ��֪��ͨ������������ӦʽΪO2+2CO2+4e-=2CO32-������C����
D���ڵ���ڲ������������ƶ������Լ���ȼ�ϵ����CO32-��ͨ����ĸ����ƶ�����D�������ΪB��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ�������ĵ��������ֶ�����Ԫ�أ�����ĸX��ʾ��ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯������ͼ��ʾ�������жϳ���Ԫ�ػش����⣺

�� f��Ԫ�����ڱ���λ����__________��
�� �Ƚ�d��e�������ӵİ뾶��С���û�ѧʽ��ʾ����ͬ��_______��__________�Ƚ�g��h������������Ӧ��ˮ���������ǿ���ǣ�_______��__________
�� ��ѡ����Ԫ�����һ����ԭ�ӹ��ۻ����д�������ʽ____________________
�� ��֪1mole�ĵ���������d2��ȼ�գ��ָ������£��ų�255.5kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ____________
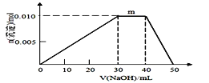
�� ����Ԫ�ؿ������R��zx4f(gd4)2����ʢ��10mL1mol��L-1R��Һ���ձ��еμ�1mol��L-1NaOH��Һ���������ʵ�����NaOH��Һ����仯ʾ��ͼ������ͼ��ʾ��
�� R��Һ������Ũ���ɴ�С��˳����________________
�� д��m�㷴Ӧ�Ķ����ӷ���ʽ________________________________
�� ��R��Һ�ļ�20mL1.2 mol��L-1Ba(OH)2��Һ������в������������ʵ���Ϊ_______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ������˵����ȷ����
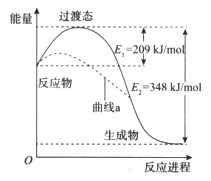
A. �÷�Ӧ�ų���348 kJ������
B. ����a�����Ƿ�Ӧʹ���˴���
C. �ϼ���������֮�ʹ��ڳɼ��ͷ�����֮��
D. N2O��g����NO��g����N2��g����NO2��g�� ![]() ����139kJ/mol
����139kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������;�㷺����ҵ����������������Ҫ�ɷ���Al2O3���Ʊ���������
��1�����Ȼ�ô�����Al2O3���乤���������£�
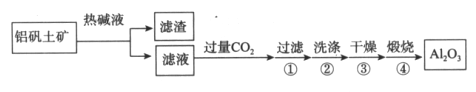
����Һ��ͨ�����CO2�ķ�Ӧ���ӷ���ʽ��________________��
�����������������Ļ�ѧ����ʽ��______________��
��2����Al2O3�ܽ������ڵı���ʯ�����ۼ����У���ʯī����Ϊ������ʯī��Ϊ���������е�⡣
�ٵ��Al2O3���Ʊ���������ԭ����__________������ţ���
a. Al2O3���ڵ����
b. Al2O3�������ӻ�����
c. Al2O3��������������
d. Al2O3������״̬ʱ�ܵ���
��Al������_________��������
������ʯī����Ҫ���ϲ��䣬��ϵ缫��Ӧʽ��������ԭ����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Cl2����ijЩ�����л���ʱ�����������HCl���������·�Ӧ����ʵ���ȵ�ѭ�����ã�4HCl��g��+O2��g��![]() 2Cl2��g��+2H2O��g����H=��115.6kJ/mol
2Cl2��g��+2H2O��g����H=��115.6kJ/mol

����˵����ȷ����
A. �÷�Ӧ�Ļ��Ϊ115.6kJ/mol
B. �����������ʹ�÷�Ӧ���ʱ�����
C. �÷�Ӧ������Ӧ��ܱ��淴Ӧ��ܴ�
D. ����H2O(g)��1molH-O���ȶ���HCl(g)��1molH-Cl������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.ij��ȤѧϰС�������ͼװ����ȡSO2���о������ʡ�
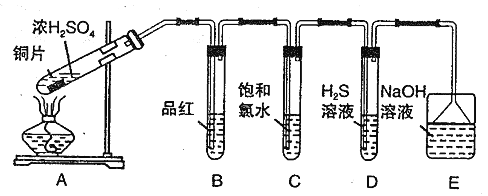
��ش���������:
��1��B��C��D�ֱ����ڼ���SO2 �����ʣ�д��C�з�Ӧ�����ӷ���ʽ_______��
��2��ʵ���й۲쵽D ���л��dz��֣���ͬѧ�����������֤��SO2 ���������������������________________________��
��3��Eװ�õ�����Ϊ______________��
II.ijѧϰС���һ��̽����ͬŨ�ȵ����������Բ�ͬ����Ʋ��������ʵ��:
��ȡһ������ԭ���۷���һ�����Ũ�����У����ȣ���ַ�Ӧ��õ���ҺX���ռ�������Y��������������Y �к���SO2��H2��
��4����ҺX�к��еĽ�����������(�ѧʽ)_________��������μ��������______��
��5��Ϊ�˲ⶨ����Y ��SO2 �ĺ�������2.24 L( ��״��)����Y ͨ�뵽200.00mL0.2000mol/L ���Ը��������Һ�У���ַ�Ӧ��ȡ��20.00mL��Һת����ƿ�н��еζ�������0.1000mol/L��KHC2O4��Һ10.00mL (������ر���ԭ������Mn2+ )��
����֪��������0.1000mol/L KHC2O4 ����Һ�У�c(C2O42-) > c(H2C2O4)���ζ����������б�ҺӦ��_______(����������)ʢװ���ζ��յ������Ϊ____________��
����������Y ��SO2 �����ʵ�������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ���![]() ��W�������еIJ��ֽṹ����һ����Ҫ�Ĺ��ܸ߷��Ӳ��ϣ��ۺ��������е�һ�֣�ת��·�����£�
��W�������еIJ��ֽṹ����һ����Ҫ�Ĺ��ܸ߷��Ӳ��ϣ��ۺ��������е�һ�֣�ת��·�����£�

��֪����A�й����Ų���ͬһ��̼ԭ���ϡ�
��![]()
��R1CH=CHR2+R3CH=CHR4![]() R1CH=CHR4+R2CH=CHR3(R��ʾ��������ԭ��)��
R1CH=CHR4+R2CH=CHR3(R��ʾ��������ԭ��)��
(1)B����������������__________��
(2)E��������__________��G����H�ķ�Ӧ������__________��
(3)д��D����E�Ļ�ѧ����ʽ��______________________��
(4)X�Ľṹ��ʽ_______________��
(5)E���ڶ���ͬ���칹��,��E������ͬ�������Ҳ��ܷ���������Ӧ��ͬ���칹����__________��(����������ṹ,����E)�����з��Ϻ˴Ź��������з����֮��3��3��2 �Ľṹ��ʽ________________________��
(6)��CH3CH2OHΪԭ��(���Լ���ѡ)�ϳɻ���ϩ,��д���ϳ�����ͼ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���ı�0.1mol/LRCOOH��Һ��pH����Һ��RCOOH��RCOO-�����ֲ�����a(X)= c(X)/[c(RCOOH)+c(RCOO-)]������(HCOOH)�����(CH3CH2COOH)������ӵķֲ�������pH�Ĺ�ϵ��ͼ��ʾ��
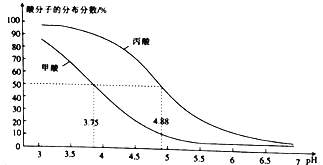
����˵����ȷ����
A. ��������Աȼ���ǿ
B. CH3CH2COOH![]() CH3CH2COO-+H+��lgK=-4.88
CH3CH2COO-+H+��lgK=-4.88
C. ��0.1mol/L������Һ��pH=2.33����0.01mol/L������Һ��pH=3.33
D. ��0.1mol/L��HCOOH��Һ��0.1mol/L��HCOONa��Һ�������ϣ�������Һ��:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ˮ��Һ�д��ڸ�����Ϊ������롢ˮ�⡢�����ܽ�ȣ�����ѧ֪ʶ�ش��������⣺
��1��t��ʱ����ˮ��c(H+)��1��10-6 mol��L-1������¶���ˮ�����ӻ�����KW��_______�����¶��£�pH��10��Ba(OH)2��Һ�����ʵ���Ũ��Ϊ_________��
��2��25��ʱ����ͬ���ʵ���Ũ�ȵ�������Һ�У���NaCl ��NaOH ��H2SO4 ��(NH4)2SO4������ˮ�ĵ���̶��ɴ�С˳��Ϊ______������Żش𣩡�
��3��25��ʱ���� a mol��L-1 �Ĵ���� b mol��L-1 ������������Һ�������Ϻ���Һ��pH=7������Һ��c(CH3COO-)+c(CH3COOH)=__________����a_______ b�����������������=������
��4����AgCl�ֱ���룺��5 mLˮ ��10 mL 0.1 mol��L-1 MgCl2��Һ ��20 mL 0.5 mol��L-1 NaCl��Һ ��40 mL 0.3mol��L-1 ������Һ���ܽ�����Һ���ͣ�����Һ��Ag+��Ũ�ȷֱ�Ϊa��b�� c��d�������ɴ�С������˳����_____������ĸ��ʾ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com