
����Ŀ��I.ij��ȤѧϰС�������ͼװ����ȡSO2���о������ʡ�
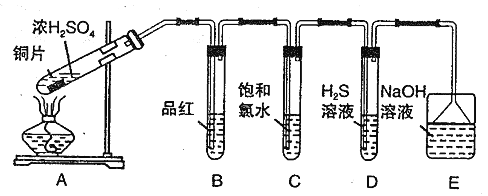
��ش���������:
��1��B��C��D�ֱ����ڼ���SO2 �����ʣ�д��C�з�Ӧ�����ӷ���ʽ_______��
��2��ʵ���й۲쵽D ���л��dz��֣���ͬѧ�����������֤��SO2 ���������������������________________________��
��3��Eװ�õ�����Ϊ______________��
II.ijѧϰС���һ��̽����ͬŨ�ȵ����������Բ�ͬ����Ʋ��������ʵ��:
��ȡһ������ԭ���۷���һ�����Ũ�����У����ȣ���ַ�Ӧ��õ���ҺX���ռ�������Y��������������Y �к���SO2��H2��
��4����ҺX�к��еĽ�����������(�ѧʽ)_________��������μ��������______��
��5��Ϊ�˲ⶨ����Y ��SO2 �ĺ�������2.24 L( ��״��)����Y ͨ�뵽200.00mL0.2000mol/L ���Ը��������Һ�У���ַ�Ӧ��ȡ��20.00mL��Һת����ƿ�н��еζ�������0.1000mol/L��KHC2O4��Һ10.00mL (������ر���ԭ������Mn2+ )��
����֪��������0.1000mol/L KHC2O4 ����Һ�У�c(C2O42-) > c(H2C2O4)���ζ����������б�ҺӦ��_______(����������)ʢװ���ζ��յ������Ϊ____________��
����������Y ��SO2 �����ʵ�������Ϊ__________��
���𰸡� SO2+Cl2+2H2O=4H++ SO42��+2 Cl�� װ��C�ӷ���������Ҳ����ʹDװ���г��ֻ��� β�������������� Fe2+ ȡ������Һ�������еμ�K3[Fe(CN)3]��Һ����������ɫ��������֤��ԭ��Һ�к���Fe2+�����������𰸾����֣� ��ʽ�ζ��� �������һ��KHC2O4��Һ����ƿ����Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ָ� 90%
��������(1)ͭ��Ũ���ᷴӦ�ķ���ʽΪ2H2SO4(Ũ) + Cu![]() CuSO4 + 2H2O +SO2�������������ܹ�ʹƷ����ɫ������������л�ԭ�ԣ��ܹ������͵���ˮ����������������������ԣ��ܹ�������������C�з�Ӧ�����ӷ���ʽΪSO2+Cl2+2H2O=4H++ SO42��+2 Cl�����ʴ�Ϊ��SO2+Cl2+2H2O=4H++ SO42��+2 Cl����
CuSO4 + 2H2O +SO2�������������ܹ�ʹƷ����ɫ������������л�ԭ�ԣ��ܹ������͵���ˮ����������������������ԣ��ܹ�������������C�з�Ӧ�����ӷ���ʽΪSO2+Cl2+2H2O=4H++ SO42��+2 Cl�����ʴ�Ϊ��SO2+Cl2+2H2O=4H++ SO42��+2 Cl����
(2)������ˮ���лӷ��ԣ�C�лӷ���������Ҳ����ʹDװ���г��ֻ��ǣ����D���л��dz��֣�����֤��SO2���������ԣ��ʴ�Ϊ��װ��C�ӷ���������Ҳ����ʹDװ���г��ֻ��ǣ�
(3)���������ܹ���Ⱦ������Eװ���е����������ܹ�����β������ֹ��Ⱦ��ͬʱ���۵�©�����Է��������ʴ�Ϊ��β����������������
(4)��ԭ������Ũ���ᷴӦ�IJ����к��ж��������������˵����Ӧһ��ʱ���Ũ��������ϡ���ᣬ����������ϡ����ķ�Ӧ�������ҺX�к��еĽ���������ΪFe2+�������������ӿ���ȡ������Һ�������еμ�K3[Fe(CN)3]��Һ����������ɫ��������֤��ԭ��Һ�к���Fe2+���ʴ�Ϊ��Fe2+��ȡ������Һ�������еμ�K3[Fe(CN)3]��Һ����������ɫ��������֤��ԭ��Һ�к���Fe2+��
(5)����֪�����£�0.1000mol/L KHC2O4����Һ�У�c(C2O42-)>c(H2C2O4)��˵������̶ȴ���ˮ��̶ȣ���Һ�����ԣ�Ӧ��ѡ����ʽ�ζ���ʢװKHC2O4��Һ��KHC2O4��Һ�ܹ������Ը��������Һ�������������һ��KHC2O4��Һ����ƿ����Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ָ���֤���ﵽ�˵ζ��յ㣬�ʴ�Ϊ����ʽ�ζ��ܣ��������һ��KHC2O4��Һ����ƿ����Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ָ���
������Y�еĶ���������������գ�ʣ��ĸ��������KHC2O4��Һ�ζ������ĵ�KHC2O4�����ʵ���=0.1000mol/L��0.01L=0.001mol������2MnO4-+5HC2O4-+11H+=2Mn2++10CO2��+8H2O��5SO2+ 2 MnO4- + 2 H2O = 2 Mn2+ + 4 H+ + 5 SO42-����֪������������ʵ���=![]() ��(0.2000mol/L��0.2L-0.001mol��
��(0.2000mol/L��0.2L-0.001mol��![]() ��
��![]() )=0.09mol��
)=0.09mol��
������Y��SO2�����ʵ�������=![]() ��100%=90%���ʴ�Ϊ��90%��
��100%=90%���ʴ�Ϊ��90%��


 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д� ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2O2�ڴ��������·ֽ����ʼӿ죬�������淴Ӧ���̵ı仯����ͼ��ʾ������˵����ȷ���ǣ������� 
A.�����������С�˷�Ӧ����ЧӦ
B.��������������H2O2��ƽ��ת����
C.H2O2�ֽ���Ȼ�ѧ����ʽ��H2O2=H2O+ ![]() O2+Q
O2+Q
D.��Ӧ��������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ����Ȳ���ױ�������ϩ�� ![]() ��4���л���ֱ���һ����������H2��ַ�Ӧ�� ��������H2��ȫ�ӳɷ�Ӧʱ�����ʵ���֮��Ϊ1��3������ ��
��4���л���ֱ���һ����������H2��ַ�Ӧ�� ��������H2��ȫ�ӳɷ�Ӧʱ�����ʵ���֮��Ϊ1��3������ ��
��������H2��ȫ�ӳɷ�Ӧʱ�����ʵ���֮��Ϊ1��2������ ��
�۱���ϩ��H2��ȫ�ӳɵ����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ����������������ͼ��ʾ�����ʽ���������Ԫ����ɣ���ת����ϵ��ͼ��ʾ������b��dΪ�����������Ϊ�����b��ˮ��Һ�������Ҿ���Ư������d��������Ӧ�ɵõ���Ư��ֽ���Ļ�������������0.01mol/L f��Һ��pH>2������˵����ȷ����

A. Ԫ�صķǽ�����:X>W>Z B. X���⻯����ֻ���ڼ��Թ��ۼ�
C. �����̬�⻯����ȶ���:Y>Z D. Y�ĺ��������ε�ˮ��Һ���ܳʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ڵ��볣��ΪKa��ijһԪ����ζ������У�pHͻ������Ũ�ȵ������������Ũ����ҪӰ��ζ��յ�͵ζ��յ�֮������߲��֡������£��ò�ͬŨ�ȵ�NaOH��Һ�ֱ�ζ�20mL����ͬŨ�ȵ�ij����HA��Һ���ζ�������ͼ��ʾ������˵������ȷ����

A. ��ͼ��֪��c1>c2>c3
B. M����Һ�д���:c(H+)+c(HA)=c(OH-)+c(A-)
C. ǡ���к�ʱ����Һ������Ũ�ȵĴ�С��ϵ: c(Na+)>c(A-��>c(OH-)>c(H+)
D. ��pH=7��Һ�����: ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ����һ���������ォ��ˮ�е�����CO(NH2)2]ת��Ϊ�����Ѻ����ʵ�ԭ��Ҳװ��ʾ��ͼ�����øõ����ͼ��װ���е����϶�ͭ������˵����ȷ����
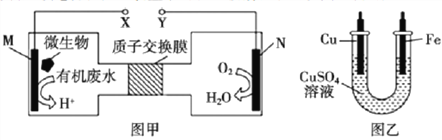
A. ͼ����Fe�缫Ӧ��ͼ����Y������
B. ͼ����H+�����ӽ���Ĥ���������ƶ�
C. ͼ����M�缫��Ӧʽ��CO(NH2)2+5H2O-14e=CO2+2NO2+14H+
D. ��ͼ����M�缫����0.5mol����ʱ��ͼ�������缫����96g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ںϳɻ��ʣ���ũҵ��Ӧ�ù㷺�����й��ڰ������ʵ���������ȷ����
A. ��ɫ B. ������ C. �ܶȱȿ���С D. ��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����м׳ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH=2K2CO3+6H2O������˵����ȷ����

A. �׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҡ������ǻ�ѧ��ת�����ܵ�װ��
B. �׳�ͨ��CH3OH�ĵ缫��ӦΪCH3OH��6e��+2H2O=CO32��+8H+
C. ��Ӧһ��ʱ������ҳ��м���һ����Cu��OH��2���壬��ʹCuSO4��Һ�ָ���ԭŨ��
D. �׳�������280 mL����״���£�O2����ʱ������������������1.45g����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com