
����Ŀ��
������Ҫ�ɷ�Ϊ NaAlSi2O6���������������ֽ��������ӣ�����Cr3+�ĺ�����������ɫ����dz��
(1) NaAlSi2O6����Ԫ���У���һ��������С��Ԫ�غ͵縺������Ԫ����ɵĺ������ֻ�ѧ���Ļ�������___________(д��ѧʽ)
(2)��̬Cr3+�ĺ�������Ų�ʽΪ_____________________��
(3)�����K[Cr(C2O4)2(H2O)�е�������___________��C2O42����̼ԭ�ӵ��ӻ����������___________����H2O��Ϊ�ȵ������������___________(��дһ��)
(4)һ�������Ͻ�ľ����ṹ��ͼ��ʾ������ṹ���ƵĻ�������___________(����)��

a.������ b.���ʯ c.�� d.�Ȼ��
(5)Ca��O��Gr�����γ�һ�־���������Եĸ�������������ṹ��ͼ��ʾ������Ca2+��O2�����������������ܶѻ���ʽ��
�ٸþ���Ļ�ѧʽΪ___________��
����֪�����ӡ������Ӱ뾶�ֱ�Ϊ100pm��140pm���þ����IJ���(�߳�)Ϊ___________pm��
�۰����ӵ�������ֵΪNA���þ����ܶȵļ������ʽΪ___________g��cm��3��������Cr4+λ��O2�����γɵ�������������ģ�����������ı߳�Ϊ___________pm��
���𰸡�Na2O2 [Ar]3d3��1s22s22p63s23p63d3 C2O42-��H2O sp2�ӻ� NH2- d CaCrO3 240![]() pm
pm ![]() g��cm��3 120
g��cm��3 120![]() pm
pm
��������
(1)Ԫ�طǽ�����Խǿ���縺��Խ������Խǿ���縺��ԽС��
(2)Cr3+�Ļ�̬���������Ϊ24-3=21�������Ų�ʽΪ��[Ar]3d3��1s22s22p63s23p63d3��
��3��ԭ������ͬ���۵�������ͬ�ķ���Ϊ�ȵ�������
��4����ͼ��֪�����Ͻ�ľ����ṹ�У�Niԭ����ĿΪ1��Alԭ����ĿΪ8��![]() =1��ΪAlNi��ÿ��Niԭ����Χ��8��Alԭ�ӣ�ÿ��Alԭ����Χ��8��Niԭ�ӣ��ݴ˽��ѡ���и����ʵľ����ṹ�жϣ�
=1��ΪAlNi��ÿ��Niԭ����Χ��8��Alԭ�ӣ�ÿ��Alԭ����Χ��8��Niԭ�ӣ��ݴ˽��ѡ���и����ʵľ����ṹ�жϣ�
��5���ٸ��ݾ����ṹͼ�;�̯�����㣻
�۸����ܶȹ�ʽ���м��㡣
(1)Ԫ�طǽ�����Խǿ���縺��Խ������Խǿ���縺��ԽС������Na��Al��Si��O����Ԫ�ص縺���ɴ�С��˳��Ϊ��O��Si��Al��Na����NaAlSi2O6����Ԫ���У���һ��������С��Ԫ�غ͵縺������Ԫ����ɵĺ������ֻ�ѧ���Ļ�������Na2O2��
(2)Cr3+�Ļ�̬���������Ϊ24-3=21�������Ų�ʽΪ��[Ar]3d3��1s22s22p63s23p63d3��
��3��K[Cr��C2O4��2��H2O��2]������ΪC2O42-��H2O�������������ÿ��Cԭ���γ�һ��C=O��C-C��C-O����Cԭ���γɵĦҼ���ĿΪ3�����۲���Ӷ���Ϊ3������Ϊsp2�ӻ���ԭ������ͬ���۵�������ͬ�ķ���Ϊ�ȵ����壬����H2O��Ϊ�ȵ����������Ӧ����3��ԭ�ӡ��ҵ�����Ϊ10����NH2-��
��4����ͼ��֪�����Ͻ�ľ����ṹ�У�Niԭ����ĿΪ1��Alԭ����ĿΪ8��![]() =1��ΪAlNi��ÿ��Niԭ����Χ��8��Alԭ�ӣ�ÿ��Alԭ����Χ��8��Niԭ�ӣ�
=1��ΪAlNi��ÿ��Niԭ����Χ��8��Alԭ�ӣ�ÿ��Alԭ����Χ��8��Niԭ�ӣ�
a����������ÿ����������Χ��8�������ӣ�ÿ����������Χ��4�������ӣ������ϣ�
b�����ʯΪ�ռ�������״�ṹ��ÿCԭ����Χ��4��Cԭ�ӣ������ϣ�
c�������������������ѻ����Ƶ���λ��Ϊ8����ÿ����ԭ����Χ������������ԭ����8���������ϣ�
d���Ȼ����ÿ���������Χ��8�������ӣ�ÿ����������Χ��8������ӣ����ϣ�
�ʴ�Ϊd��
��5���ٸ��ݾ����ṹͼ�;�̯����֪��������Oԭ����Ϊ![]() ��6=3��Caԭ����Ϊ
��6=3��Caԭ����Ϊ![]() ��8=1��Crԭ����Ϊ1����ѧʽΪCaCrO3��
��8=1��Crԭ����Ϊ1����ѧʽΪCaCrO3��
����֪�����ӡ������Ӱ뾶�ֱ�Ϊ100pm��140pm��������Խ�����480 pm�����Ըþ����IJ���(�߳�)Ϊ240![]() pm��
pm��
�۰����ӵ�������ֵΪNA���þ����ܶȵļ������ʽΪ =
=![]() g��cm��3��������Cr4+λ��O2�����γɵ�������������ģ���������߳�Ϊ������
g��cm��3��������Cr4+λ��O2�����γɵ�������������ģ���������߳�Ϊ������![]() ��Խ��߳��ȣ������������ı߳�Ϊ
��Խ��߳��ȣ������������ı߳�Ϊ![]() ��240
��240![]() pm=120
pm=120![]() pm��
pm��


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ�����̼����ﴦ����Cu2+��ˮ��ý���ͭ����������м�ͻ���̿����������ʱ����÷�ˮ��Cu2+Ũ���ڲ�ͬ��̼������(x)��������ʱ��仯����������ͼ��ʾ��

������������������
A. ����̿��Cu2+����һ������������
B. ��м�ͻ���̿������Һ���γ���أ���Ϊ����
C. ������̼���������̼��(x)��һ������߷�ˮ��Cu2+��ȥ������
D. ������̼�������պ�Cu2+��ˮ��ͭ�ķ�Ӧԭ����Fe+Cu2+��Fe2++Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ʊ��屽��ʵ��װ����ͼ��ʾ����ش��������⣺

(1)�÷�Ӧװ��������A������Ϊ__________����Ӧ��ʼǰ��������A�м���Ĺ���ҩƷ�����ۣ���װ������Һ©���е�Һ��ҩƷ��_______��
(2)������B���ϡ������ڣ���ȴˮӦ��_____�ڽ��롣
(3)���ܿڲ��ܲ�����ƿ�е�Һ��֮�£���ԭ����____________��
(4)�Ҳ��Һ©���е������ڷ�Ӧ_______ʱ����A��(��д��Ӧǰ����Ӧ�л��߷�Ӧ��)�������ӷ���ʽ�����������ǣ�_________________��
(5)��Ӧ��������ƿ�е�Һ���м��������ữ����������Һ���ɼ���������________________��
(6)�÷�Ӧ���̿������±�����3Br2+2Fe=2FeBr3��Br2+FeBr3=FeBr4��+Br+(���ȶ�)��![]() + Br+ + FeBr4����
+ Br+ + FeBr4����![]() + HBr + FeBr3�����Ϸ�Ӧ��֪��
+ HBr + FeBr3�����Ϸ�Ӧ��֪��![]() +Br2 ��
+Br2 �� ![]() +HBr�еĴ���Ϊ_________��
+HBr�еĴ���Ϊ_________��
A��Fe B��FeBr3 C��Br+ D��FeBr4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֽ�����ɵĺϽ�A���ں��ʵ������¿ɰ���ͼ���з�Ӧ(���ֲ����ˮʡ��)����֪FΪ���ɫ��������ش�
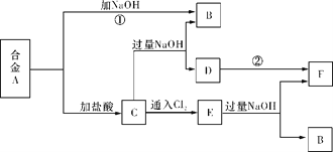
(1)��ҺC��������Ҫ��____________________(�ѧʽ)��
(2)д����Ӧ�ڵĻ�ѧ����ʽ_______________________________________________������D��F��ʵ������_______________________________________________��
(3)д����ӦC��E�����ӷ���ʽ________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йط�Ӧ�����仯ͼ����жϴ�����ǣ� ��

A. I�ɱ�ʾ����ȵķ��ȷ�Ӧ
B. II�ɱ�ʾ����ȵķ��ȷ�Ӧ
C. III��ʾ��ը��Ӧ
D. IV��ʾ����ͼ�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ��Q1��Q2�Ĵ�С��ϵ��
A(g)+B(g)��C(g)+Q1 A(g)+B(g)��C(l)+Q2
A. Q1��Q2 B. Q1��Q2 C. Q1��Q2 D. ���Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������250 mL 0.10 mol��L-1��NaOH��Һʱ������ʵ�������ʹ���Ƶ���ҺŨ��ƫ�ߵ���(����)
A. ����ƿ����ˮδ�������ﴦ��
B. ����ʱ���ӿ̶���
C. ����Ͳ��ȡŨNaOH��Һʱ����ˮϴ����Ͳ2��3�Σ�ϴ��Һ�����ձ���
D. ���ݺ�ת����ƿ���Σ�����Һ����͵���ڿ̶��ߣ��ٲ��Ӽ���ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ü״�ȼ�ϵ������Դ���������缫��⺬Cr2O72�������Է�ˮ�����տɽ�Cr2O72��ת����Cr(OH)3��������ȥ��װ������ͼ������˵����ȷ����

A. Fe(II)����
B. M�缫�ĵ缫��ӦʽΪCH3OH+8OH����6e��= CO32��+6H2O
C. ���һ��ʱ�����Fe(��)�������г�������
D. ��·��ÿת��6mol���ӣ������1 mol Cr2O72������ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����̿���Ҫ�ɷ�ΪMnO2���������Ʊ��̼��仯���
��1������ұ�������̵�һ�ַ��������������̿�����Mn3O4�����������ȷ�Ӧԭ���Ƶ��̣������ȷ�Ӧ�Ļ�ѧ����ʽΪ ��
��2���ִ�ұ�������̵�һ�ֹ�����������ͼ��ʾ��

�±�Ϊt��ʱ���й����ʵ�pKsp��ע��pKsp =��lgKsp����
���� | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
���̿�ԭ�����ķ�ӦΪ��12MnO2+ C6H12O6+ 12H2SO4��12MnSO4+ CO2��+18H2O
���÷�Ӧ�У���ԭ��Ϊ__________��д��һ�������ԭ�������ʵĴ�ʩ�� ��
����Һ1��pH ����������������������������MnSO4����Һ��pH��
������MnF2����ҪĿ���dz�ȥ ����Ca2+��Fe3+��Cu2+��
��3����MnSO4��ȡMnCO3
��MnSO4��Һ�м������NH4HCO3��Һ�����÷�Ӧ�����ӷ���ʽΪ_____________________������MnSO4��Һ�м���(NH4)2CO3��Һ���������Mn(OH)2�����ܵ�ԭ���У�MnCO3(s) + 2OH��(aq)![]() Mn(OH)2(s) + CO32-(aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K�� ������ֵ����
Mn(OH)2(s) + CO32-(aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K�� ������ֵ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com