
【题目】某化学兴趣小组对铜、铁与硝酸的反应进行实验探究。回答下列问题:
(1)验证铜与硝酸的反应(实验装置如图所示)。已知仪器a中盛有足量的一定浓度的硝酸溶液,试管b中盛有6.4g铜片。
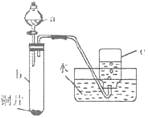
①仪器a的名称是___。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有___。
③待试管b中铜片完全消失。如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是___ g。
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3molHNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为___。
②Fe粉与稀硝酸反应生成硝酸亚铁的离子方程式为___。
③反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=___。
④标准状况下,生成NO气体的体积为___L(保留两位小数)。
【答案】分液漏斗 酸性和强氧化性 9.8 Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O 1:3 1.68
【解析】
(1)①根据装置图可知仪器的名称;
②反应中N元素的化合价部分未变化生成硝酸铜,部分降低生成氮的氧化物;
③铜完全反应生成硝酸铜,向b中液体里加入足量氢氧化钠溶液,铜离子完全转化为氢氧化铜沉淀,根据n=![]() 计算铜的物质的量,根据铜原子守恒计算氢氧化铜的物质的量,再根据m=nM计算;
计算铜的物质的量,根据铜原子守恒计算氢氧化铜的物质的量,再根据m=nM计算;
(2)①铁粉与稀硝酸反应生成硝酸铁、NO和水,结合原子守恒和电子守恒写出反应的化学方程式;
②Fe粉与稀硝酸反应生成硝酸亚铁、NO和水,结合原子守恒和电子守恒写出反应的离子方程式;
③5.6g Fe粉的物质的量为![]() =0.1mol,根据得失电子守恒和物料守恒分析解答;
=0.1mol,根据得失电子守恒和物料守恒分析解答;
④一氧化氮的物质的量为:0.3-3n(Fe3+)-2n(Fe2+)。
(1)①根据装置图可知仪器a的名称是分液漏斗;
②反应中N元素的化合价部分未变化生成硝酸铜,硝酸表现酸,性部分降低生成氮的氧化物,硝酸表现强氧化性;
③6.4g铜的物质的量为![]() =0.1mol,向b中液体里加入足量氢氧化钠溶液,铜离子完全转化为氢氧化铜沉淀,根据铜原子守恒可知n[Cu(OH)2]=n(Cu)=0.1mol,故m[Cu(OH)2]=0.1mol×98g/mol=9.8g;
=0.1mol,向b中液体里加入足量氢氧化钠溶液,铜离子完全转化为氢氧化铜沉淀,根据铜原子守恒可知n[Cu(OH)2]=n(Cu)=0.1mol,故m[Cu(OH)2]=0.1mol×98g/mol=9.8g;
(2)①铁粉与稀硝酸反应生成硝酸铁、NO和水,发生反应的化学方程式为Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O;
②Fe粉与稀硝酸反应生成硝酸亚铁、NO和水,发生反应的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
③根据得失电子守恒和物料守恒可知:n(Fe3+)+n(Fe2+)=0.1mol;3n(Fe3+)+2n(Fe2+)=3[0.3-3n(Fe3+)-2n(Fe2+)],解之得:n(Fe3+)=0.025mol;n(Fe2+)=0.075mol,所以溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)为1:3;
④一氧化氮的物质的量为:0.3-3n(Fe3+)-2n(Fe2+)=0.3-3×0.025mol-2×0.075mol=0.075mol,所以生成NO气体的体积为:0.075mol×22.4L/mol=1.68L。


科目:高中化学 来源: 题型:
【题目】已知Fe2O3 (s)+3CO(g) ![]() 2Fe(s) +3CO2 (g),则反应达平衡后甲、乙两容器中说法不正确的是( )
2Fe(s) +3CO2 (g),则反应达平衡后甲、乙两容器中说法不正确的是( )
起 始 量 | 温度T℃ 平衡常数K=64 恒容且V=1L | ||||
Fe2O3 | CO | Fe | CO2 | ||
甲 | 1 mol | 1 mol | 1 mol | 1 mol | |
乙 | 1 mol | 2 mol | 1 mol | 1mol | |
A.容器中混合气体的平均相对分子质量不变时反应达平衡
B.乙中CO2的体积分数为50%
C.甲中CO的转化率为60%
D.甲、乙两容器中 CO的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示装置回答以下问题。已知:①KMnO4常温下与浓盐酸反应可制得Cl2。②H2SiO3不溶于水。
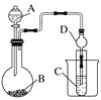
(1)利用如图装置可以验证元素非金属性的变化规律。图中A装置的名称是________________。干燥管D的作用是____________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为____________________________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_____________________。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀HNO3 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2。试剂A与C分别为________(填序号);试管中发生反应的离子方程式为__________________。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ能量,根据能量变化示意图,下列说法不正确的是
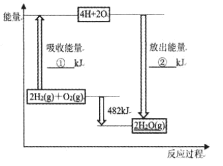
A.①、②的数值分别为1370、1852
B.拆开H2O(g)中的1 molH-O键吸收463kJ的能量
C.2H2(g)+O2(g)=2H2O(g) △H=-482kJ·mol-1
D.已知H2O(1)=H2O(g) △H>0,说明lmolH2O(1)的能量比1molH2O(g)高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol·L-1NaOH溶液,得到沉淀的物质的量与加入NaOH溶液的体积如图所示。原溶液中Cl-与SO42-的物质的量之比为( )
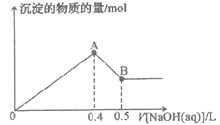
A.6:1B.1:3C.2:3D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是

A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。试回答下列问题:
(1)Ni2+电子排布中,电子填充的能量最高的能级符号为______。
(2)金属Ni能与CO形成配合物Ni(CO)4.与CO互为等电子体的一种分子为______(写化学式,下同),与CO互为等电子体的一种离子为______。
(3)丁二酮肟(![]() )是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为______,2mol丁二酮肟分子中所含σ键的数目为______。
)是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为______,2mol丁二酮肟分子中所含σ键的数目为______。
(4)丁二酮肟常与NI2+形成图A所示的配合物,图B是硫代氧的结果:
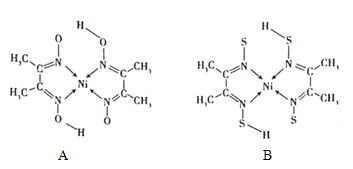
①A的熔、沸点高于B的原因为______。
②B晶体含有化学键的类型为______(填选项字母)。
A.σ键B.金属键C.配位键D.π键
(5)人工合成的氧化镍往往存在缺陷,某缺陷氧化银的组成为Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为______。
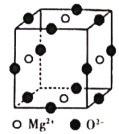
(6)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种有机烯醚,可以用烃A通过下列路线制得:
是一种有机烯醚,可以用烃A通过下列路线制得:
![]()
则下列说法正确的是( )
A.![]() 的分子式为C4H4O
的分子式为C4H4O
B.①、②、③的反应类型分别为卤代、水解、消去
C.A能使高锰酸钾酸性溶液褪色
D.A的结构简式是CH2=CHCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com