
【题目】用HCl滴定NaOH:c(NaOH)=![]() (填“偏大”或“偏小”或“无影响”)。
(填“偏大”或“偏小”或“无影响”)。
(1)酸式滴定管未润洗__________;
(2)碱式滴定管未润洗__________;
(3)锥形瓶用NaOH润洗__________;
(4)锥形瓶洗净后未干燥__________;
(5)酸式滴定管滴定前有气泡,滴定结束后无气泡__________;
(6)滴定时不小心滴到锥形瓶外__________;
(7)振荡锥形瓶时溶液溅出__________;
(8)滴定前仰视,滴定后俯视__________;
(9)滴定前平视,后仰视__________。
【答案】偏大 偏小 偏大 无影响 偏大 偏大 偏小 偏小 偏大
【解析】
根据滴定原理:c(NaOH)=![]() ,通过分析各个操作对消耗标准溶液的体积大小判断滴定误差。
,通过分析各个操作对消耗标准溶液的体积大小判断滴定误差。
(1)酸式滴定管未润洗,会使标准溶液浓度减小,导致消耗标准溶液体积偏大,以此为标准计算的待测碱溶液的浓度偏大;
(2)碱式滴定管未润洗导致等体积的溶液中含有碱的物质的量减少,则消耗标准溶液体积偏少,以此为标准计算的待测碱溶液的浓度偏小;
(3)锥形瓶用NaOH润洗会使NaOH增多,导致消耗标准溶液体积偏大,以此为标准计算的待测碱溶液的浓度偏大;
(4)锥形瓶洗净后未干燥,由于没有改变NaOH的物质的量,因此消耗标准溶液体积不变,对待测碱溶液的浓度无影响;
(5)酸式滴定管滴定前有气泡,滴定结束后无气泡,消耗标准溶液体积偏大,以此为标准计算的待测碱溶液的浓度偏大;
(6)滴定时不小心滴到锥形瓶外,就会多消耗标准溶液,以此为标准计算的待测碱溶液的浓度偏大;
(7)振荡锥形瓶时溶液溅出,反应消耗标准溶液体积偏小,以此体积为标准计算待测溶液的浓度偏小;
(8)滴定前仰视后俯视,则标准溶液体积读数偏小,以此为溶液体积计算的待测碱溶液的浓度偏小;
(9)滴定前平视,后仰视,使标准溶液体积偏大,以此为溶液体积计算的待测碱溶液的浓度偏大。


科目:高中化学 来源: 题型:
【题目】让生态环境更秀美、人民生活更幸福!为此,天津冬季取暖许多家庭用上了清洁能源天然气。实际生产中天然气需要脱硫,在1200℃时,工艺中会发生下列反应:
①H2S(g)+![]() O2(g)=SO2(g)+H2O(g) ΔH1
O2(g)=SO2(g)+H2O(g) ΔH1
②2H2S(g)+SO2(g)=![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
③H2S(g)+![]() O2(g)=S(g)+H2O(g) ΔH3
O2(g)=S(g)+H2O(g) ΔH3
④2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为( )
A.ΔH4=![]() (ΔH1 +ΔH2-3ΔH3)
(ΔH1 +ΔH2-3ΔH3)
B.ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=![]() (ΔH1-ΔH2+3ΔH3)
(ΔH1-ΔH2+3ΔH3)
D.ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为_____。
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是_____(填元素符号)。
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为_____。
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力_____ (“减弱”或“不变”)。铁晶体中粒子之间作用力类型是_____。
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是_____;
②CH4和HCHO比较,键角较大的是_____,主要原因是_____。
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。
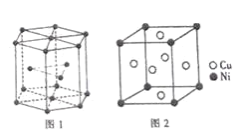
①钴晶胞堆积方式的名称为_____;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为_____ pm(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO2![]() 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是
①相同时间内,氧气的生成速率为n mol·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
A. ①③⑤⑥ B. ②③⑤
C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是( )
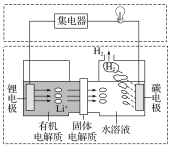
A.碳极发生的反应:2H2O+2e-=H2↑+2OH-
B.有机电解质和水溶液不可以互换区域
C.理论上外电路中每转移1 mol电子,负极消耗的质量为7 g
D.若该电池可以充电,充电时碳极接外加电源的负极,锂极接外加电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按系统命名法命名下列各物质。
①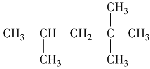 _____________________
_____________________
②(CH3)2CH—CH2—CH2—CH2—CH3_____________________
③![]() ____________________
____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质硼是冶金、建材、化工、核工业等部门的重要原料,而金属镁也广泛应用于航空航天等国防军事工业。以铁硼矿为原料,利用碳碱法工艺生产硼和镁,其工艺流程图如下:
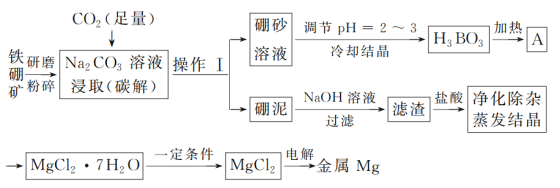
已知:铁硼矿的主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Al2O3和SiO2杂质;硼砂的化学式为Na2B4O7·10H2O。
(1)铁硼矿研磨粉碎的目的是____________;操作Ⅰ的名称为___;硼泥中除杂质SiO2和Al2O3外,其他成分的化学式为_______。
(2)写出流程图中碳解过程的化学方程式:__________;在高温条件下金属Mg与A反应制备单质硼的化学方程式为:__________。
(3)碳碱工艺需两次调节pH:①常用H2SO4调节硼砂溶液pH=2~3制取H3BO3,其离子方程式为B4O72-+2H++5H2O=4H3BO3;②制取MgCl2·7H2O时,在净化除杂过程中,需先加H2O2溶液,其作用是_______,然后用MgO调节pH约为5,其目的是_____。
(4)用MgCl2·7H2O制取MgCl2时,为防止MgCl2水解,反应需在“一定条件下”进行,则该条件是指_____。
(5)实验时不小心触碰到NaOH溶液,可用大量清水冲洗,再涂抹H3BO3溶液中和,其化学方程式为:NaOH+H3BO3=Na[B(OH)4],下列关于Na[B(OH)4]溶液中微粒浓度关系正确的是___。
A c(Na+)+c(H+)=c([B(OH)4]-)+c(OH-)
B c(Na+)>c([B(OH)4]-)>c(H+)>c(OH-)
C c(Na+)=c([B(OH)4]-)+c(H3BO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示。下列说法不正确的是

A.该反应的化学方程式为5A+4B![]() 4C
4C
B.2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4
C.用B的浓度变化表示0-2min时间内的速率为2mol/(L·min)
D.2min前,正反应速率逐渐减小,逆反应速率逐渐增大,但是正反应速率大于逆反应速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为标定一种烧碱样品的物质的量浓度,称取该烧碱样品4.0g配成1L溶液,取出20.00mL置于锥形瓶中,以甲基橙为指示剂,用0.10mol·L-1HCl标准溶液滴定,恰好完全中和时消耗标准盐酸19.00mL,若烧碱中只含有一种杂质,则不可能是( )
A.NaClB.Ca(OH)2C.Na2CO3D.NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com