
【题目】用下列实验装置和方法进行相应实验,能达到实验目的的是
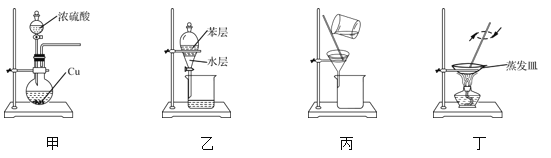
A. 用装置甲制备SO2
B. 用装置乙从碘水溶液中萃取碘
C. 用装置丙除去粗盐溶液中混有的KCl杂质
D. 用装置丁蒸干溶液获得(NH4)2CO3晶体
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将 0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ·mol-1 ,则H2SO4和Ba(OH)2反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在101kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1) △H =-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 1molOH-的质量为17g
B. 二氧化碳的摩尔质量为44g
C. 铁原子的摩尔质量等于它的相对原子质量
D. 标准状况下,1mol 任何物质的体积均为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷及其化合物在工农业生产中都有重要用逾。
(1)基态磷原子价电子排布的轨道表示式为_____。
(2)元素B、N、O的第一电离能由大到小的顺序为_____。
(3)一种食品添加剂NaNO2中NO2﹣中心原子的杂化类型是_____,与NO2﹣互为等电子体的分子的化学式为_____(写1种)
(4)N2H4是火箭的燃料,与氧气的相对分子质量相同,它在常温常压下是液态,而氧气是气态,造成这种差异的主要原因是_____。
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层,磷化硼可由三溴化硼和三溴化磷于高温下在氢气中反应合成。
①三溴化磷分子的空间构型是_____,三溴化硼键角是_____。
②磷化硼晶体晶胞如图所示,其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为_____,磷原子的配位数为是_____,该结构中有一个配位健,提供空轨道的原子是_____;已知该晶胞边长apm,阿伏加德罗常数为NA,则磷化硼晶体的密度为_____gcm﹣3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用含碳、氢、氧三种元素的有机物A和B为原料合成有机化合物H(C11H12O2)的路线示意图如下:

已知: 两个醛分子间能发生如下反应:
 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)
(1)经质谱法测定,有机物A的相对分子质量为46,经元素分析知A分子中C、H和O原子个数比为2:6:1 。则有机物A的分子式为______________
(2)芳香族化合物B的分子式为C7H8O,C能与钠反应,但不与NaOH反应。则C的结构简式为 ____________________________。
(3)写出A转化为C的化学方程式:__________________________________________________________
(4)检验C中含有的官能团的化学实验方法是_____________________________________________________________________________________________________________________________________
(5)写出E的结构简式:____________________;H的结构简式:________________________________
(6)上述合成过程中没有涉及到的反应类型是:_________________(填写序号)
A.取代反应; b . 加成反应; c. 消去反应; d. 氧化反应; e. 还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向盛有1 L 0.1 mol·L-1NaHSO4溶液的烧杯中不断滴加0.05 mol·L-1的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如下图所示,下列说法不正确的是

A. A点时pH=1
B. 恰好完全沉淀时Ba(OH)2的体积为2 L
C. B点时,溶液中的离子浓度关系为c(Na+)>c(SO![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
D. C点时pH=14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,错误的是( )
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.不能用酒精萃取碘水溶液中的碘
C.蒸馏时,应使温度计水银球位于蒸馏烧瓶支管处
D.可以用pH试纸测定氯水的酸碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化二氯(C12O)是次氯酸的酸酐,用作氯化剂其部分性质如下:
物理性质 | 化学性质 |
常温下,C12O是棕黄色刺激性气体。 熔点:-120.6℃;沸点2.0℃ | C12O不稳定接触一般有机物易爆炸;它易溶于水,同时反应生成次氯酸。 |
实验室制备原理2Na2CO3+H2O+2Cl2![]() 2NaCl +2NaHCO3+ C12O, 现用下列装置设计实验制备少量C12O,并探究相关物质的性质。
2NaCl +2NaHCO3+ C12O, 现用下列装置设计实验制备少量C12O,并探究相关物质的性质。

(1)装置A中仪器X的名称为___________。
(2)若气体从左至右流动装置连接顺序是A、___________(每个装置限用一次)。
(3)装置F中盛装试剂的名称为___________。
(4)A中反应的离子方程式为___________。
(5)当D中收集适量液态物质时停止反应,设计简单实验证明B中残留固体中含有NaHCO3:___________。
(6)实验完成后取E中烧杯内溶液滴加品红溶液发现溶液褪色。该课题组设计实验探究溶液褪色的原因。
序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.1mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
I | 5.0 | 0 | 0 | 5.0 | 3滴 | 较快褪色 |
II | 0 | 5.0 | a | 0 | 3滴 | 不褪色 |
III | 5.0 | 0 | 0 | 3滴 | 缓慢褪色 |
①a=___________。
②由上述实验得出的结论是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com