
����Ŀ�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH �����ڸõ�ص�˵����ȷ����( )
3Zn(OH)2+2Fe(OH)3+4KOH �����ڸõ�ص�˵����ȷ����( )
A. �ŵ�ʱ��Zn��������������ԭ��Ӧ
B. �ŵ�ʱ��K2FeO4������ҺpH��С
C. ���ʱ��п��������ҺpH��С
D. ���ʱ�������缫��ӦΪ��Fe(OH)3-3e-+5OH-==FeO42-+4H2O
���𰸡�D
��������
A���ŵ�ʱ��пʧ���ӷ���������Ӧ����������A����
B���ŵ�ʱ��������صõ������������缫��ӦʽΪFeO42-+4H2O+3e-=Fe��OH��3+5OH-��pH����B����
C�����ʱ��п�����������缫��ӦʽΪ��Zn��OH��2+2e-=Zn+2OH-����ҺpH����C����
D����������ʧ���ӷ���������Ӧ���ɸ���������ӣ��缫��ӦʽΪ��Fe��OH��3-3e-+5OH-�TFeO42-+4H2O����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
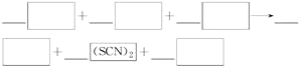
����Ŀ����֪����(SCN)2Ϊ��±�أ�����Ӽ������ӵ�������±���������ơ����������գ������軯����Һ���Ȼ�����Һ��ϣ���Һ��Ϊ��ɫ��
(1)д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________��
(2)�����ɵĺ�ɫ��Һ��Ϊ���ȷݣ���������ʵ��(�������Ƕ���)��
�ٵ�һ���еμӵ⻯����Һ���������ټ������Ȼ�̼�����������ˮ��ӽ���ɫ�����Ȼ�̼���__________ɫ��д���ù��̵����ӷ���ʽ��________________________�������Һ�еμ�������ˮ��ˮ��Һ�ֱ�Ϊ��ɫ����������Br2________(������������С����������ȷ����) (SCN)2��
�ڵڶ����м����������Ը��������Һ��Ѫ��ɫ��ȥ����ɲ���ƽ�÷�Ӧ�����ӷ���ʽ_________________������________mol������ص���Һ��ȫ��Ӧ��ת�Ƶ���2 mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У�����3mol A��1mol B��һ�������·�����Ӧ3A��g����B��g��![]() 2C��g����D��g������ƽ��ʱ�����C��Ũ��Ϊw mol/L��������������¶Ȳ��䣬���°������������ʼ���ʣ��ﵽƽ��ʱ��C��Ũ����ȻΪw mol/L���ǣ� ��
2C��g����D��g������ƽ��ʱ�����C��Ũ��Ϊw mol/L��������������¶Ȳ��䣬���°������������ʼ���ʣ��ﵽƽ��ʱ��C��Ũ����ȻΪw mol/L���ǣ� ��
A. 6mol A��2mol B
B. 1.5mol A��0.5mol B��1mol C��0.5mol D
C. 3mol A��1mol B��2mol C��1mol D
D. 4mol C��1mol D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ��Ϊ0.100 0 mol��L1��NaOH��Һ�ζ�20.00 mLŨ�Ⱦ�Ϊ0.100 0 mol��L1��������HX��HY��HZ���ζ�������ͼ��ʾ������˵����ȷ����
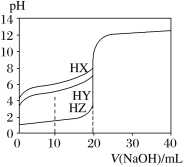
A.����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��HZ��HY��HX
B.���ݵζ����߿ɵ�Ka(HX)����������107
C.HX��HY��HZ��Һ�о���������ƽ��
D.HY��HZ��ϣ��ﵽƽ��ʱc(H��)��![]() ��c(Z)��c(OH)
��c(Z)��c(OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������[CO��NH2��2��H2O2]��һ��������ζ�İ�ɫ�ᾧ��ĩ���������غ�������˫�����ʣ���һ�����͵������������������㷺Ӧ����Ư�ס���֯��ҽҩ��ũҵ����ֳҵ��������ϳ���ͼ��
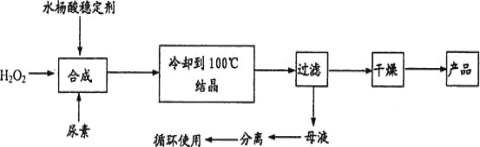
�Իش��������⣺
��1��ʵ�������������n��H2O2����n��CO��NH2��2��]=1.2:1������Ҫԭ����____��
��2����ĸҺ�з����H2O2�����أ����õIJ�����____��
a.���������� b.��Һ������ c.��ѹ���ᾧ d.��ѹ������ȡ
��3��Ϊ�ⶨ��Ʒ�л������ĺ�����������16�����൱��H2O2 34��������ȡ������Ʒ12.000g���ܽ⣬��250mL����ƿ�ж��ݡ�ȷ��ȡ25.00mL����ƿ�У�����1mL 6mol/L�����ᣬȻ����0.2000 mol/LKMnO4����Һ�ζ������εζ�ƽ������KMnO4��Һ20.00mL��KMnO4��Һ�����ز���Ӧ����
�ٵζ��յ�������ǣ��������һ��KMnO4��Һ��____��
������ƿ��ʹ��ǰ������еIJ�����____��
����ɲ���ƽ����ʽ��__MnO4��+___H2O2+___H+=___Mn2++____H2O+____,__
�����ζ�ǰ�ζ��ܼ��촦�����ݣ��ζ�����ʧ����ʹ��õĻ���������___��ѡ���ƫ�ߡ�����ƫ�͡����䡱����
�ݸ��ݵζ������ȷ����Ʒ�л���������������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��CO(g)��CuO(s)![]() CO2(g)��Cu(s)�ͷ�Ӧ��H2(g)��CuO(s)
CO2(g)��Cu(s)�ͷ�Ӧ��H2(g)��CuO(s)![]() Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ��CO(g)��H2O(g)
Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ��CO(g)��H2O(g)![]() CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(����)
CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(����)
A. ��Ӧ�ٵ�ƽ�ⳣ��K1��c(CO2).c(Cu)/c(CO).c(CuO)
B. ��Ӧ�۵�ƽ�ⳣ��K��K1/K2
C. ���ڷ�Ӧ�ۣ�����ʱ���¶����ߣ�H2Ũ�ȼ�С����÷�Ӧ���ʱ�Ϊ��ֵ
D. ���ڷ�Ӧ�ۣ����º����£�����ѹǿ��H2Ũ��һ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���淴Ӧ��X(s)��aY(g)![]() bZ(g)����H����Ӧ�ﵽƽ��ʱ���¶ȡ�ѹǿ�Կ��淴Ӧ��Ӱ������ͼ��ʾ(ͼ��pΪѹǿ������p1>p2)�������й��ж���ȷ����(����)
bZ(g)����H����Ӧ�ﵽƽ��ʱ���¶ȡ�ѹǿ�Կ��淴Ӧ��Ӱ������ͼ��ʾ(ͼ��pΪѹǿ������p1>p2)�������й��ж���ȷ����(����)
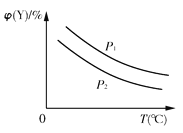
A. ���淴Ӧ���ʱ���H<0
B. ��Ӧ�Ļ�ѧ������a<b
C. �ÿ��淴Ӧ��ƽ�ⳣ��K��![]()
D. �¶ȡ�ѹǿ���䣬��ʹ�ú��ʵĴ������������Y��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ϊ��Ч��������Ҫ�ɷ�Ԫ�أ��Ӹ�����[��Ҫ��Ag2S��Cu2(OH)2CO3��FeO��Cr2O3��SiO2]����ȡCr��Ag�Ĺ���������ͼ��
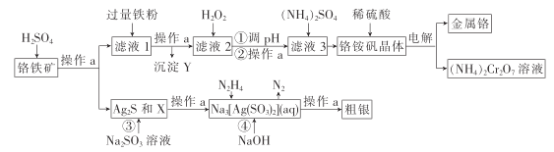
��֪���ٲ������������������↑ʼ��������ȫ������pH���±�(��������Ũ��Ϊ0.01mol��L-1)
������ | Fe(OH)2 | Fe(OH)3 | Cr(OH)3 |
��ʼ������pH | 7.6 | 2.7 | 4.9 |
��ʼ������pH | 9.6 | 3.7 | 6.8 |
�ڸ�立����壺[NH4Cr(SO4)2��12H2O]
��1������aΪ___��X��Y�ֱ�Ϊ____��___��
��2��д������H2O2������Ӧ�����ӷ���ʽ��___��
��3������pHֵ���õ����ʵĻ�ѧʽΪ___��pHֵӦ�����Ƶķ�ΧΪ__������Һ3��ø���茶������ȷ����������___�����ˡ�ϴ�ӡ����
��4������立������������������ֱ������ˮ����Ҫԭ����___��
��5������ܷ�����Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������̼����ȼ�ϵ����Li2CO3��K2CO3Ϊ����ʡ���CH4Ϊȼ��ʱ���õ�ع���ԭ����ͼ������˵����ȷ���� (����)��

A. aΪCH4��bΪCO2
B. ![]() ���ƶ�
���ƶ�
C. �˵���ڳ���ʱҲ�ܹ���
D. �����缫��ӦʽΪO2��2CO2��4e��===2![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com