
【题目】25℃时,用浓度为0.100 0 mol·L1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
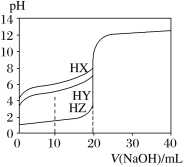
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线可得Ka(HX)的数量级是107
C.HX、HY与HZ溶液中均存在两种平衡
D.HY与HZ混合,达到平衡时c(H+)=![]() +c(Z)+c(OH)
+c(Z)+c(OH)
【答案】B
【解析】
A项、在相同温度下,溶液中离子浓度越大,溶液的导电性越强,由图像起点可知,三种酸溶液的酸性大小顺序为HZ>HY>HX,在相同温度下,同浓度的三种酸溶液中离子浓度得大小顺序为HZ>HY>HX,则三种酸溶液的导电能力顺序为HZ>HY>HX,故A错误;
B项、由图像起点可知,0.100 0 mol·L1 HX溶液的pH为4,溶液中c(H+)=c(X)=10—4mol/L,c(HX)= 0.100 0 mol/L—10—4mol/L≈0.100 0 mol/L,则Ka(HX)=![]() =
=![]() = 107,故B正确;
= 107,故B正确;
C项、由图像起点可知,0.100 0 mol·L1 HZ溶液的pH为1,说明HZ为强酸,在溶液中完全电离,只存在水的电离平衡,故C错误;
D项、由Ka(HY)=![]() 可知
可知![]() = c(H+),若HY与HZ混合,达到平衡时c(H+)=
= c(H+),若HY与HZ混合,达到平衡时c(H+)=![]() +c(Z)+c(OH)成立,得到c(Z)+c(OH)=0,与HZ为强酸溶液中一定存在Z不相符,故D错误;
+c(Z)+c(OH)成立,得到c(Z)+c(OH)=0,与HZ为强酸溶液中一定存在Z不相符,故D错误;
故选B。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
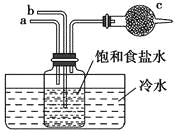
A. a通入CO2,然后b通入NH3,c中放碱石灰
B. b通入NH3,然后a通入CO2,c中放碱石灰
C. a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写中,正确的是( )
A.NaHCO3溶液中加入少量NaOH溶液:![]()
B.铁跟稀硫酸反应:![]()
C.少量金属钠加到冷水中:![]()
D.氧化铁与稀硫酸反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl36H2O晶体。(图中夹持及尾气处理装置均已略去)

(1)装置B中发生反应的化学方程式是______。
(2)装置E中的现象是______。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:______。
(4)该小组学生利用上述滤液制取FeCl36H2O晶体,设计流程如图所示:
![]()
①步骤I中通入Cl2的作用是________。
②简述检验滤液中Fe3+的操作方法_______。
③步骤Ⅱ从FeCl3稀溶液中得到FeCl36H2O晶体的主要操作包括:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2,发生反应:2CO2(g)===2CO(g)+O2(g),该反应的ΔH________(填“>”“<”或“=”)0,ΔS________(填“>”“<”或“=”)0,在低温下,该反应________(填“能”或“不能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式为2NO+2CO![]() 2CO2+N2。反应在常温下能够自发进行,则反应的ΔH________(填“>”“<”或“=”)0。
2CO2+N2。反应在常温下能够自发进行,则反应的ΔH________(填“>”“<”或“=”)0。
(3)已知在100 kPa、298 K时石灰石分解反应CaCO3(s)===CaO(s)+CO2(g)的ΔH>0,ΔS>0,则:
①该反应常温下________(填“能”或“不能”)自发进行。
②据本题反应数据分析,温度________(填“能”或“不能”)成为反应方向的决定因素。
(4)已知CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g),ΔH=+218 kJ·mol-1,该反应能够自发进行的反应条件是________。
CaO(s)+SO2(g)+CO2(g),ΔH=+218 kJ·mol-1,该反应能够自发进行的反应条件是________。
(5)某吸热反应能自发进行,则该反应的ΔS________(填“>”或“<”)0。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×101 | 1.7×105 | 6.2×1010 | K1=4.3×107 K2=5.6×1011 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为________(填字母)。
(3)常温下,0.1 mol·L1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________(填序号)
A.[H+] B.[H+]/[CH3COOH]
C.[H+]·[OH] D.[OH]/[H+]
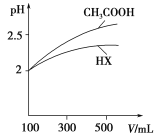
(4)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)写出少量CO2通入次氯酸钠溶液中的离子方程式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH 。关于该电池的说法正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH 。关于该电池的说法正确的是( )
A. 放电时,Zn作负极,发生还原反应
B. 放电时,K2FeO4附近溶液pH减小
C. 充电时,锌极附近溶液pH减小
D. 充电时,阳极电极反应为:Fe(OH)3-3e-+5OH-==FeO42-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁是冶炼铁的主要方法。
(1)从炼铁高炉口排出的尾气中含有一定量的有毒气体___(填化学式),会污染空气。100多年前,人们曾耗巨资改建高炉,结果尾气中的该物质含量并未减少。高炉炼铁的主要反应方程式为(设铁矿石用磁铁矿)____。
(2)已知:①4Fe(s) + 3O2=2Fe2O3(s) ΔH1
②4Fe3O4(s)+O2(g)=6Fe2O3(s) ΔH2
③3Fe(s)+2O2(g)=Fe3O4(s) ΔH3
则ΔH2=___(用含上述ΔH的代数式表示)。
(3)高铁酸钠(Na2FeO4)是铁的一种重要化合物,可用电解法制备,阳极材料为铁,其电解质溶液应选用___(填H2SO4、HNO3、KOH、NaOH、Na2SO4)溶液,阳极反应式为___。
(4)某温度下,HX的电离平衡常数K=1×10-5。则该温度下0.100mol/L的HX溶液中c(H+)=___(平衡时HX的浓度以0.100mol/L计,水的电离忽略不计。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物杜瓦苯(![]() )的说法中错误的是
)的说法中错误的是
A.杜瓦苯与苯互为同分异构体
B.杜瓦苯的二氯代物共有六种(不含立体异构)
C.杜瓦苯中所有的碳原子可能共平面
D.杜瓦苯可使酸性高锰酸钾溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com