
【题目】在密闭容器中,加入3mol A和1mol B,一定条件下发生反应3A(g)+B(g)![]() 2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持体积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )
2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持体积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )
A. 6mol A+2mol B
B. 1.5mol A+0.5mol B+1mol C+0.5mol D
C. 3mol A+1mol B+2mol C+1mol D
D. 4mol C+1mol D
【答案】B
【解析】
该反应在恒温恒容条件下进行,达到平衡后,C的浓度仍为w mol/L,说明两反应为等效平衡,只要按化学计量数将各物质的量转化到左边,满足n(A)=3mol,n(B)=1mol即可。
A、开始加入6molA+2molB,假如容器的容积为原容器容积的2倍,则达到平衡时各组分的浓度与原平衡相等,C的浓度为w mol/L;然后将容器的容积缩小一半,相当于增大了压强,平衡向着正向移动,则C的浓度大于2w mol/L,故A错误;
B、开始加入1.5molA+0.5molB+1molC+0.5molD,将1molC+0.5molD按化学计量数转化到左边可得1.5molA、0.5molB,故等效为开始加入3molA+1mol B所到达的平衡,平衡时C的浓度为w mol/L,故B正确;
C、开始加入3molA+1molB+2mol C+1molD,将2molC、1molD按化学计量数转化到左边可得3molA、1molB,故等效为开始加入6molA、2molB所到达的平衡,根据B可知,达到平衡时C的浓度大于2w mol/L,故C错误;
D、开始加入4molC、1molD,假设D完全反应,则消耗2molC,还剩余2molC,相当于加入3mol A和1molB、2molC,所以达到平衡时C的浓度一定大于w mol/L,故D错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

(1)B装置中的干燥剂是_____(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1--2滴浓盐酸,可观察到E装置中的现象是产生______(填”烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____(填“a”“b”或“c”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写中,正确的是( )
A.NaHCO3溶液中加入少量NaOH溶液:![]()
B.铁跟稀硫酸反应:![]()
C.少量金属钠加到冷水中:![]()
D.氧化铁与稀硫酸反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H具有似龙延香、琥珀香气息,香气淡而持久,广泛用作香精的稀释剂和定香剂.合成它的一种路线如图:
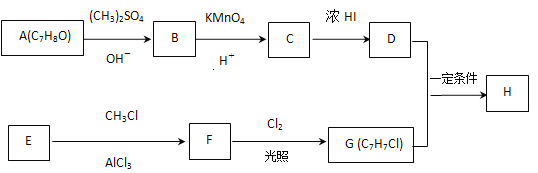
已知以信息:
①![]() ;
;
②核磁共振氢谱显示A的苯环上有四种化学环境不同的氢原子,且取代基的位置相邻;
③在D中滴加几滴FeCl3溶液,溶液呈紫色;
④芳香烃 F的相对分子质量介于90~100之间,0.1 mol F充分燃烧可生成7.2 g水;
⑤R1COOH+RCH2Cl![]() R1COOCH2R+HCl。
R1COOCH2R+HCl。
回答下列问题:
(1)A的化学名称是____,由C生成D的反应的化学方程式为______________。
(2)由F生成G的反应的化学方程式为____________,反应类型为____。
(3)H的结构简式为_________。
(4)苯环上有三个取代基且其中两个与A中所含的官能团相同,同时又能发生银镜反应的C的同分异构体有 (不考虑立体异构)_____种,其中核磁共振氢谱中有5组峰,且峰面积之比为1∶2∶2∶2∶1的同分异构体的结构简式是________(任写一种即可)。
(5)由苯酚和已有的信息经以下步骤可以合成化合物
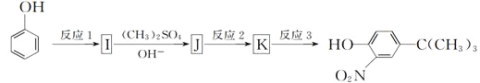
反应1所用的试剂为___,K的结构简式为____,反应3所用的试剂为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl36H2O晶体。(图中夹持及尾气处理装置均已略去)

(1)装置B中发生反应的化学方程式是______。
(2)装置E中的现象是______。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:______。
(4)该小组学生利用上述滤液制取FeCl36H2O晶体,设计流程如图所示:
![]()
①步骤I中通入Cl2的作用是________。
②简述检验滤液中Fe3+的操作方法_______。
③步骤Ⅱ从FeCl3稀溶液中得到FeCl36H2O晶体的主要操作包括:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2,发生反应:2CO2(g)===2CO(g)+O2(g),该反应的ΔH________(填“>”“<”或“=”)0,ΔS________(填“>”“<”或“=”)0,在低温下,该反应________(填“能”或“不能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式为2NO+2CO![]() 2CO2+N2。反应在常温下能够自发进行,则反应的ΔH________(填“>”“<”或“=”)0。
2CO2+N2。反应在常温下能够自发进行,则反应的ΔH________(填“>”“<”或“=”)0。
(3)已知在100 kPa、298 K时石灰石分解反应CaCO3(s)===CaO(s)+CO2(g)的ΔH>0,ΔS>0,则:
①该反应常温下________(填“能”或“不能”)自发进行。
②据本题反应数据分析,温度________(填“能”或“不能”)成为反应方向的决定因素。
(4)已知CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g),ΔH=+218 kJ·mol-1,该反应能够自发进行的反应条件是________。
CaO(s)+SO2(g)+CO2(g),ΔH=+218 kJ·mol-1,该反应能够自发进行的反应条件是________。
(5)某吸热反应能自发进行,则该反应的ΔS________(填“>”或“<”)0。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH 。关于该电池的说法正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH 。关于该电池的说法正确的是( )
A. 放电时,Zn作负极,发生还原反应
B. 放电时,K2FeO4附近溶液pH减小
C. 充电时,锌极附近溶液pH减小
D. 充电时,阳极电极反应为:Fe(OH)3-3e-+5OH-==FeO42-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组性质比较中,正确的是()
①沸点:![]()
②离子还原性:![]()
③酸性:![]()
④金属性:![]()
⑤气态氢化物稳定性:![]()
⑥半径:![]()
A.①②③B.③④⑤⑥C.②③④D.①③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com