
【题目】用锌片与1 mol·L-1稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是
A. 对该反应体系加热
B. 用浓硫酸代替稀盐酸
C. 不用锌片,改用锌粉
D. 加入少量1 mol·L-1硫酸
科目:高中化学 来源: 题型:
【题目】在标准状况下,1L水中溶解700LNH3,所得溶液的密度为0.9g·cm-3,则氨水的浓度为
A. 18.4mol·L-1 B. 20.4mol·L-1 C. 37.7% D. 38.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能的存储是氢能应用的主要瓶颈,2008年,Yoon等人发现Ca与C60生成的Ca32C60能大量吸附H2分子.
(1)C60晶体易溶于苯、CS2 , 说明C60是 分子(选填:“极性”、“非极性”);
(2)1mol C60分子中,含有σ键数目为 .
(3)MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度agcm﹣3 , 则晶胞的体积为 cm3[用a、NA表示阿伏加德罗常数].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是SO2和H2S)的转化对环境保护具有重要意义.
(1)SO2的大量排放会引起严重的环境问题是 , 潮湿条件下,写出大气中SO2转化为HSO3﹣的方程式 .
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42﹣ , 两步反应的能量变化示意图1如下:
1mol H2S(g)全部氧化成SO42﹣(aq)的热化学方程式为
(3)SO2是工业制硫酸的原料气体之一,一定温度下,向容积为2L的密闭容器中充入一定量的SO2和O2 , 发生反应:2SO2(g)+O2(g)2SO3(g),过程中测定的部分数据见表:
时间/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.050 |
4 | 0.050 | 0.025 |
5 | 0.040 | |
8 | 0.020 |
①反应在0~4min内的平均速率为v(SO2)=;
②此温度下该反应的化学平衡常数K= ,
③8min时,维持温度不变,往反应容器中再通入0.020mol SO2(g),0.010mol O2(g),重新达到平衡时混合气体中SO2的百分含量将(填“减小”,“增大”或“不变”).(4)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示:
①在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌.欲使生成的硫单质中不含CuS,可采取的措施有 .
②一般来说,如果一个反应的平衡常数大于105 , 通常认为反应进行得较完全;相反,如果一个反应的平衡常数小于10﹣5 , 则认为这个反应很难进行.已知常温下各物质的溶度积及电离平衡常数:
CuS:Ksp=6.3×10﹣36;H2S:K a1=1.3×10﹣7 , K a2=7.1×10﹣15 ,
通过计算说明反应CuS(s)+2H+ (aq)=Cu2+(aq)+H2S(aq)进行的程度 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极.该电池的电解质为6mol/LKOH溶液,下列说法正确的是( )
A.放电时镍电极反应为:NiO(OH)+H2O+e﹣=Ni(OH)2+OH﹣
B.放电时OH﹣移向镍电极
C.充电时碳电极反应为H2﹣2e﹣+2OH﹣=2H2O
D.充电时将碳电极与电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系,该元素(用R)表示)的单质能与NaOH溶液反应生成盐(Na2RO3)和氢气.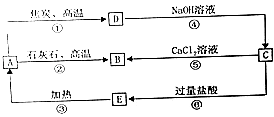
(1)写出各物质的化学式:A;C .
(2)写出反应①的化学方程式该反应中氧化剂与还原剂的物质的量之比为 .
(3)写出反应④的离子方程式: .
(4)写出反应⑤的离子方程式 .
(5)H2CO3的酸性强于E的酸性,请用离子方程式予以证明: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个电化学过程的示意图. 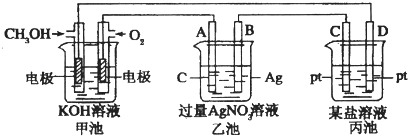
请回答下列问题:
(1)图中甲池是(填“原电池”“电解池”或“电镀池”).
(2)A(石墨)电极的名称是(填“正极”“负极”“阴极”或“阳极”).
(3)写出通入CH3OH的电极的电极反应式
(4)乙池中反应的化学方程式为当乙池中B(Ag)极质量增加5.4g,甲池中理论上消耗O2的体积为L(标准状况),此时丙池中某电极析出1.6g某金属,则丙池中的某盐溶液可能是 A.MgSO4B.CuSO4 C.NaCl D.AgNO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.硫离子的结构示意图为 
B.核外电子排布相同的微粒化学性质也相同
C.氢弹中用到的2H,3H互为同位素
D.同种元素的原子均有相同的质子数和中子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述,正确的是( )
A.新制氯水中只含Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后pH值将变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com