
【题目】结合元素周期律,结合下列事实推测不合理的是()
事实 | 推测 | |
A | IVA族 | 同族 |
B | HI在230℃时分解,HCl在1500℃时分解 | HF分解温度大于1500℃ |
C | H3PO4是中强酸,H2SO4是强酸 | HClO4是强酸 |
D | Na、Al通常用电解法冶炼 | Mg可用电解法冶炼 |
A.AB.BC.CD.D
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A.![]() 为V形的极性分子
为V形的极性分子
B.ClO3-的空间构型为平面三角形
C.SF6中有7对完全相同的成键电子对
D.SiF4和SO32-的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
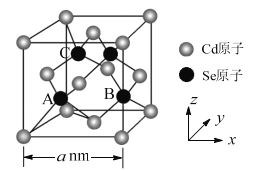
【题目】(CdSe)n小团簇(CdnSen,n=1~16)为Ⅱ-Ⅵ族化合物半导体材料,具有独特的光学和电学性质,常应用于发光二极管、生物系统成像与诊断等方面。
回答下列问题:
(1)基态Se原子的价层电子排布式为___。
(2)Cd的第一电离能大于同周期相邻元素,原因是___。
(3)CdS、CdSe、CdTe均为重要的Ⅱ-Ⅵ族化合物半导体材料,熔点分别为1750℃、1350℃、1041℃,上述熔点呈规律性变化的原因是___。
(4)利用有机配体PH3、N(CH3)3等修饰(CdSe)2可改善其光致发光效率。其中PH3的空间构型是___。N(CH3)3中参与形成配位键的孤电子对占据的轨道是___。
(5)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。其中原子坐标参数A为(![]() ,
,![]() ,
,![]() ),则B、C的原子坐标参数分别为___。该晶胞中CdSe键的键长为___。已知Cd和Se的原子半径分别为rCdnm和rSenm,则该晶胞中原子的体积占晶胞体积的百分率为___。
),则B、C的原子坐标参数分别为___。该晶胞中CdSe键的键长为___。已知Cd和Se的原子半径分别为rCdnm和rSenm,则该晶胞中原子的体积占晶胞体积的百分率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:
3A(g)+B(g)![]() xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol/(L·min),且此时A、B的物质的量浓度之比为3∶5。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol/(L·min),且此时A、B的物质的量浓度之比为3∶5。求:
(1)此时A的浓度及反应开始前放入容器中A、B的物质的量。
(2)B的平均反应速率。
(3)x的值是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叶蝉散(isoprocard)对水稻叶蝉和飞虱具有较强的触杀作用,防效迅速,但残效不长.工业上用邻异丙基苯酚合成叶蝉散的过程如下:

下列有关说法正确的是( )
A.叶蝉散的分子式是C11H16NO2
B.邻异丙基苯酚发生了取代反应
C.叶蝉散在强酸、强碱性环境中能稳定存在
D.可用FeCl3检验叶蝉散中是否含邻异丙基苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食用香料A分子中无支链,B分子中无甲基,B能使Br2的CCl4溶液褪色,1mol B与足量Na反应生成0.5mol H2,各物质间有如图1转化。
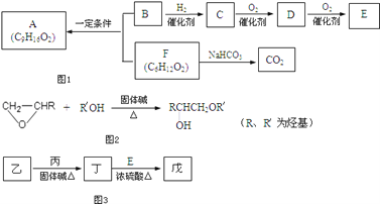
回答下列问题:
(1)在一定条件下能与C发生反应的是____;
a.Na b.Na2CO3 c.Br2/CCl4 d.CH3COOH
(2)D分子中的官能团名称是____,E的结构简式是____;
(3)B与F反应生成A的化学方程式是____;
(4)F的某种同分异构体甲能发生水解反应,其中的一种产物能发生银镜反应;另一产物在光照条件下的一氯取代物只有两种,且催化氧化后的产物也能发生银镜反应。则甲的结构简式是____;
(5)已知醇与某类环醚类之间在和固体碱共热的环境下会有如图2反应:从反应机理分析,该反应类型可称为____;
(6)工业上由乙出发可以合成有机溶剂戊(C7H14O3),流程图示见图3,
已知:①乙是C的同系物,其催化氧化产物在常温下为气态;②丁分子中有2个甲基,推测戊的结构简式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、Cu2O 广泛应用于太阳能电池领域。以 CuSO4、NaOH 和抗坏血酸为原料,可制备 Cu2O。
(1)Cu2+基态核外电子排布式为________。
(2)SO4 2﹣的空间构型为_________(用文字描述),Cu2+与 OH-反应能生成[Cu(OH)4 ]2-, [Cu(OH)4]2-中的配位原子为_______(填元素符号)。
(3)抗坏血酸的分子结构如图 1 所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
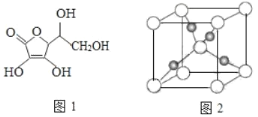
(4)一个 Cu2O 晶胞(如图 2)中,Cu 原子的数目为_________。
Ⅱ、磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 FeCl3、NH4H2PO4、LiCl 和苯胺等作为原料制备。回答下列问题:
(5)在周期表中,与 Li 的化学性质最相似的邻族元素是___,该元素基态原子核外 M层电子的自旋状态_______(填“相同”或“相反”)。
(6)苯胺(![]() )的晶体类型是_________。苯胺与甲苯(
)的晶体类型是_________。苯胺与甲苯( ![]() )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡均属于溶液中的离子平衡。根据要求回答问題。
(1)常温下0.1mol·L-1的HA溶液中pH=3,则HA是______(填“强电解质”或“弱电解质”),其电离方程式____________________________________。
(2)已知:常温下0.1mol·L-1 BOH溶液pH=13,将V1L0.1mol·L-1HA溶液和V2L 0.1 mol·L-1BOH溶液混合,回答下列问题:
①当V1:V2=1:1时,溶液呈____性,请用离子方程式解释原因________________。
②当混合溶液pH=7时,溶液中离子浓度大小关系是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苦杏仁酸在医药工业可用于合成头孢羟唑、羟苄唑、匹莫林等的中间体,下列路线是合成苦杏仁酸及其衍生物的一种方法:
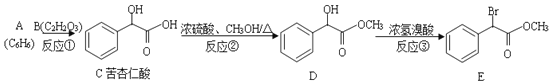
(1)苦杏仁酸中含有的官能团名称__________。
(2)生成C的反应类型_________。B的结构简式____________。
(3)1molE最多可以与___________NaOH反应。
(4)反应③的化学方程式为_______。
(5) 两个C分子可以反应生成具有三个六元环的化合物F,则F的结构简式为______。
(6)写出满足下列条件的C的同分异构体,既能发生银镜反应,又能发生水解反应,遇到FeCl3溶液显紫色,其中苯环上只有两个位于对位取代基,其结构简式为________。
(7)已知:RCH2COOH![]() RCHClCOOH,请以冰醋酸为原料(无机试剂任选)设计制备聚乙醇酸(
RCHClCOOH,请以冰醋酸为原料(无机试剂任选)设计制备聚乙醇酸(![]() )的合成路线______。
)的合成路线______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com