
【题目】Ⅰ、Cu2O 广泛应用于太阳能电池领域。以 CuSO4、NaOH 和抗坏血酸为原料,可制备 Cu2O。
(1)Cu2+基态核外电子排布式为________。
(2)SO4 2﹣的空间构型为_________(用文字描述),Cu2+与 OH-反应能生成[Cu(OH)4 ]2-, [Cu(OH)4]2-中的配位原子为_______(填元素符号)。
(3)抗坏血酸的分子结构如图 1 所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
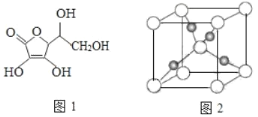
(4)一个 Cu2O 晶胞(如图 2)中,Cu 原子的数目为_________。
Ⅱ、磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 FeCl3、NH4H2PO4、LiCl 和苯胺等作为原料制备。回答下列问题:
(5)在周期表中,与 Li 的化学性质最相似的邻族元素是___,该元素基态原子核外 M层电子的自旋状态_______(填“相同”或“相反”)。
(6)苯胺(![]() )的晶体类型是_________。苯胺与甲苯(
)的晶体类型是_________。苯胺与甲苯( ![]() )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是________。
【答案】1s22s22p63s23p63d9或[Ar]3d9 正四面体形 O sp3、sp2 易溶于水 4 Mg 相反 分子晶体 苯胺中存在电负性较强的N所以可以形成氢键,因此比甲苯的熔沸点高。
【解析】
(1)Cu原子失去4s能级上1个电子、3d能级上1个电子生成铜离子,据此书写该基态离子核外电子排布式;
(2)SO42-中S原子价层电子对个数![]() 且不含孤电子对,根据价层电子对互斥理论判断该微粒空间构型;该配离子中Cu2+提供空轨道、O原子提供孤电子对形成配位键;
且不含孤电子对,根据价层电子对互斥理论判断该微粒空间构型;该配离子中Cu2+提供空轨道、O原子提供孤电子对形成配位键;
(3)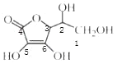 中1、2、3号C原子价层电子对个数是4,4、5、6号碳原子价层电子对个数是3,根据价层电子对互斥理论判断该分子中C原子轨道杂化类型;抗坏血酸中羟基属于亲水基,增大其水解性;
中1、2、3号C原子价层电子对个数是4,4、5、6号碳原子价层电子对个数是3,根据价层电子对互斥理论判断该分子中C原子轨道杂化类型;抗坏血酸中羟基属于亲水基,增大其水解性;
(4)该晶胞中白色球个数![]() 、黑色球个数为4,则白色球和黑色球个数之比=2:4=1:2,根据其化学式知,白色球表示O原子、黑色球表示Cu原子;
、黑色球个数为4,则白色球和黑色球个数之比=2:4=1:2,根据其化学式知,白色球表示O原子、黑色球表示Cu原子;
(5)根据元素周期表和对角线原则可知与锂化学性质相似的是镁,镁的M层电子数是2,占据s轨道,s轨道最多容纳2个电子,所以自旋方向相反;
(6)大多数有机物都是分子晶体,除了一部分有机酸盐和有机碱盐是离子晶体。苯胺比甲苯的熔沸点都高,同一种晶体类型熔沸点不同首先要考虑的就是是否有氢键,苯胺中存在电负性较强的N所以可以形成氢键,因此比甲苯的熔沸点高。
(1)Cu原子失去4s能级上1个电子、3d能级上1个电子生成铜离子,该基态离子核外电子排布式为1s22s22p63s23p63d9或[Ar]3d9;
(2)SO42中S原子价层电子对个数![]() 且不含孤电子对,根据价层电子对互斥理论判断该微粒空间构型为正四面体形;该配离子中Cu2+提供空轨道、O原子提供孤电子对形成配位键,所以配原子为O;
且不含孤电子对,根据价层电子对互斥理论判断该微粒空间构型为正四面体形;该配离子中Cu2+提供空轨道、O原子提供孤电子对形成配位键,所以配原子为O;
(3)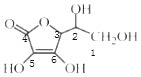 中1、2、3号C原子价层电子对个数是4,4、5、6号碳原子价层电子对个数是3,根据价层电子对互斥理论判断该分子中C原子轨道杂化类型,1、2、3号C原子采用sp3杂化,4、5、6号C原子采用sp2杂化;抗坏血酸中羟基属于亲水基,增大其水解性,所以抗坏血酸易溶于水;
中1、2、3号C原子价层电子对个数是4,4、5、6号碳原子价层电子对个数是3,根据价层电子对互斥理论判断该分子中C原子轨道杂化类型,1、2、3号C原子采用sp3杂化,4、5、6号C原子采用sp2杂化;抗坏血酸中羟基属于亲水基,增大其水解性,所以抗坏血酸易溶于水;
(4)该晶胞中白色球个数![]() 、黑色球个数为4,则白色球和黑色球个数之比=2:4=1:2,根据其化学式知,白色球表示O原子、黑色球表示Cu原子,则该晶胞中Cu原子数目为4;
、黑色球个数为4,则白色球和黑色球个数之比=2:4=1:2,根据其化学式知,白色球表示O原子、黑色球表示Cu原子,则该晶胞中Cu原子数目为4;
(5)根据元素周期表和对角线原则可知与锂化学性质相似的是镁,镁的M层电子数是2,占据s轨道,s轨道最多容纳2个电子,所以自旋方向相反;
(6)大多数有机物都是分子晶体,除了一部分有机酸盐和有机碱盐是离子晶体。苯胺比甲苯的熔沸点都高,同一种晶体类型熔沸点不同首先要考虑的就是是否有氢键,苯胺中存在电负性较强的N所以可以形成氢键,因此比甲苯的熔沸点高。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】某强酸性溶液 X 中可能含有 Ba2+、A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-、NO2-中的一种或几种,现取 X 溶液进行连续实验,实验过程及产物如下:
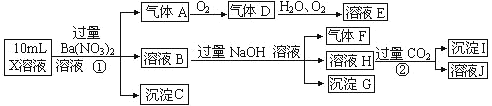
根据以上信息,下列判断正确的是
A.X 溶液中一定存在 A13+、NH4 + 、Fe3+、SO42-
B.X 溶液中可能存在 SO32-、C1-、NO2-
C.向溶液 J 中加入过量的溶液 E,最终溶液中可能含有两种溶质
D.沉淀 I 一定是 Al (OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

(1)反应开始到10s,用Z表示的反应速率___________________
(2)反应开始到10s时,Y的转化率为__________________
(3)反应的化学方程式为:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期律,结合下列事实推测不合理的是()
事实 | 推测 | |
A | IVA族 | 同族 |
B | HI在230℃时分解,HCl在1500℃时分解 | HF分解温度大于1500℃ |
C | H3PO4是中强酸,H2SO4是强酸 | HClO4是强酸 |
D | Na、Al通常用电解法冶炼 | Mg可用电解法冶炼 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3A(g)+B(g)![]() 2C(g)+3D(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g)+3D(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.9 mol·L-1·min-1B.v(B)=0.2mol·L-1·min-1
C.v(C)=0.5mol·L-1·min-1D.v(D)=1.0mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海冰是海水冻结而成的咸水冰。海水冻结时,部分来不及流走的盐分以卤汁的形式被包围在冰晶之间,形成“盐泡”![]() 假设盐分以一个NaCl计
假设盐分以一个NaCl计![]() ,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )
,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )

A.海冰内层“盐泡”越多,密度越小
B.海冰冰龄越长,内层的“盐泡”越多
C.海冰内层“盐泡”内的盐分主要以NaCl分子的形式存在
D.海冰内层NaCl的浓度约为![]() 设冰的密度为
设冰的密度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向NaX溶液和YCl溶液中加入盐酸和氢氧化钠溶液,混合溶液的pH与离子浓度变化关系如图所示,下列说法不正确的是

A.L1表示![]() 与pH的变化关系
与pH的变化关系
B.Kb(YOH)=10-10.5
C.a点时两溶液中水的电离程度不相同
D.0.1mol·L-1的YX溶液中离子浓度关系为:c(Y+)>c(X-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH(OH)CH2CH![]() CH3CH=CHCH3+H2O,下列有关说法正确的是
CH3CH=CHCH3+H2O,下列有关说法正确的是
A.CH3CH=CHCH3分子中所有碳原子不可能处于同一平面
B.CH3CH=CHCH3和HBr加成产物的同分异构体有4种(不考虑立体异构)
C.CH3CH(OH)CH2CH3与乙二醇、丙三醇互为同系物
D.CH3CH(OH)CH2CH3、CH3CH=CHCH3均能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 1L水中溶解了40.0 g NaOH,该溶液的物质的量浓度为1 mol/L
B. 从1L2mol/L的NaCl液中取出0.5L,取出的该溶液的浓度为1mol/L
C. 中和100 mL 1mol/L的H2SO4溶液,需NaOH8.0g
D. 配制500mL0.5mol/L的CuSO4溶液,需40.0g胆矾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com