
【题目】某实验小组人员用质量分数为98%,密度为1.84g·cm-3的浓硫酸配制1L2.3mol·L-1的稀硫酸。
(1)所配制的稀硫酸中,H+的物质的量浓度与____mol·L-1的NaHSO4溶液中H+的物质的量浓度相同,NaHSO4与氢氧化钡在溶液中反应使溶液呈中性的离子方程式为_____。
(2)需量取浓硫酸的体积为_____mL。
(3)容量瓶使用前应_____。
【答案】4.6 Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O 125.0 查漏
【解析】
由电离方程式可知硫酸中H+的物质的量浓度是硫酸物质的量浓度的两倍,NaHSO4溶液中H+的物质的量浓度与NaHSO4物质的量浓度相同;通过配制前后溶质质量不变可得公式:![]() ,以此答题。
,以此答题。
(1)由电离方程式可知硫酸中H+的物质的量浓度是硫酸物质的量浓度的两倍,NaHSO4溶液中H+的物质的量浓度与NaHSO4物质的量浓度相同,故2.3mol·L-1的稀硫酸中H+的物质的量浓度为4.6mol/L,与4.6mol/L的NaHSO4溶液中H+的物质的量浓度相同;NaHSO4与氢氧化钡在溶液中反应使溶液呈中性的离子方程式为:![]() ;
;
故答案为:4.6;![]() ;
;
(2)配制前后溶质质量不变可得公式:![]() ,则浓硫酸的体积
,则浓硫酸的体积![]() ;容量瓶使用前应查漏。
;容量瓶使用前应查漏。
故答案为:125.0;查漏。


科目:高中化学 来源: 题型:
【题目】化合物F是合成一种增强记忆力药物的重要中间体,其合成路线如下:
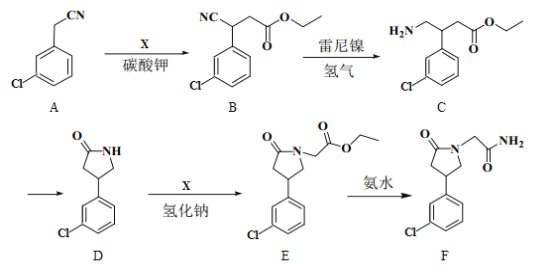
(1)E中的含氧官能团名称为__________。(写一种)
(2)A→B的反应类型为__________。
(3)写出同时满足下列条件的B的一种同分异构体的结构简式:__________。
①为α-氨基酸;②苯环上有4个取代基;③有6种不同化学环境的氢。
(4)C转为D生成的另一种产物的结构简式为__________。
(5)已知:R—Br→R—CN,请写出以苯甲醇(![]() )和
)和![]() 为原料制备有机物X
为原料制备有机物X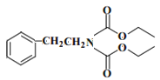 (结构如图)的合成路线流程图__________________(无机试剂任用,合成路线流程图示例见本题题干)。
(结构如图)的合成路线流程图__________________(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼制石油能得到许多有机化合物,相关物质的转化关系如下图所示,其中A的产量是衡量一个国家石油化工发展水平的重要标志,标况下,B气体的密度为0.71gL-1,C是一种红色固体单质,D是一种混合气体。

请回答:
(1)A的结构简式为______,A与溴的四氯化碳溶液的反应类型为______。
(2)B与CuO反应的化学方程式______。
(3)下列说法不正确是______。
A.A中所有原子共平面
B.A与溴的四氯化碳溶液反应现象,和A与溴水反应的现象完全相同
C.等物质的量A与B混合物在足量氧气中完全燃烧,生成水的物质的量相等
D.B是引起温室效应的气体之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.水杨酸和阿司匹林互为同系物
B.H2 和 D2 互为同素异形体
C.甲苯分子中所有碳原子均共平面
D.分子式为 C3H6BrCl 和C3H6Br2的有机物的同分异构体个数相同(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.将0.1 mol·L-1 CH3COOH溶液从20 ℃升温至30 ℃,溶液中c(H+)/c(CH3COOH)减小
B.若NH4Cl溶液与NH4HSO4溶液的pH相等,则c(NH![]() )也相等
)也相等
C.向盐酸中加入氨水至中性,溶液中![]() >1
>1
D.常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中放出的热量为______kJ。
(2)肼(N2H4)-空气燃料电池(产物为N2和H2O)是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式:_______,负极的电极反应式:_______。
(3)如图是一个电解过程示意图。
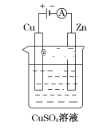
①锌片上发生的电极反应式是:____________
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气______L.(假设空气中氧气体积分数为20%;Cu相对原子质量:64)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧层中臭氧分解过程如图所示,下列说法正确的是
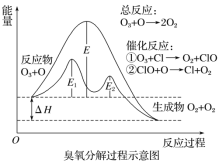
A.催化反应①②均为放热反应
B.E1是催化反应①对应的正反应的活化能,(E2+ΔH)是催化反应②对应的逆反应的活化能。
C.决定O3分解反应速率的是催化反应②。
D.温度升高,总反应的正反应速率的增加幅度小于逆反应速率的增加幅度,且平衡常数增大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.标准状况下3.6gH2O含有的电子数为2NA
B.2.8g乙烯与聚乙烯的混合物含有的极性键为0.4NA
C.0.lmolCl2与足量的铁粉充分反应转移的电子数为0.2NA
D.1L0.2mol/l的K2SO3溶液中SO![]() 的数目为0.2NA
的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4mo1A和2molB进行如下反应:3A(g)+2B(g)![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应前后的压强之比为5:4(相同的温度下测量),则下列说法正确的是
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应前后的压强之比为5:4(相同的温度下测量),则下列说法正确的是
A.该反应的化学平衡常数表达式是K=![]()
B.此时,B的平衡转化率是35%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加C的量,B的平衡转化率不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com