
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是
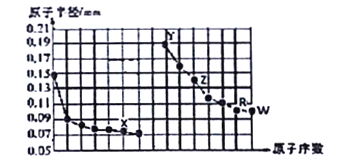
A. X所在主族中,X的简单氢化物分子间存在氢键,所以其氢化物稳定性最强
B. R简单氢化物的酸性弱于W简单氢化物,故元素非金属性R小于W
C. 在同周期中,W的含氧酸酸性最强
D. 已知Z的一种金属储氢材料LiZH4(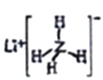 )遇水剧烈反应放出H2,则反应方程式为:LiZH4+2H2O=LiZO2+4H2↑
)遇水剧烈反应放出H2,则反应方程式为:LiZH4+2H2O=LiZO2+4H2↑
【答案】D
【解析】由图可知,为第二周期和第三周期元素的原子半径的变化,根据原子序数关系可知X为O元素,Y为Na元素,Z为Al元素,R为S元素,W为Cl元素,A.X 为氧元素,所在主族中非金属性最强,所以其氢化物稳定性最强,选项A错误;B.简单氢化物的酸性强弱不能用于判断元素非金属性强弱,应该是R的最高价氧化物的水化物H2SO4性弱于W最高价氧化物的水化物HClO4,故元素非金属性R小于W,选项B错误;C.在同周期中,W的最高价含氧酸HClO4酸性最强,选项C错误;D.已知Z的一种金属储氢材料LiZH4(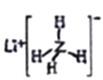 )遇水剧烈反应放出H2,则反应方程式为:LiAlH4+2H2O=LiAlO2+4H2↑,选项D正确。答案选D。
)遇水剧烈反应放出H2,则反应方程式为:LiAlH4+2H2O=LiAlO2+4H2↑,选项D正确。答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铋(Bi)与氮同族,氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、生产金属铋等。一种用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下:
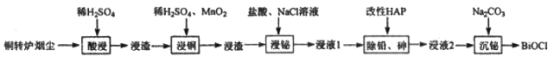
请回答:
(1)Bi位于第六周期,其原子结构示意图为__________________________________。
(2)向“酸浸”所得浸液中加入Zn粉,充分反应后过滤,从溶液中获得ZnSO4·7H2O的操作为__________、过滤、洗涤、干燥。
(3)“浸铜”时,有单质硫生成,其离子方程式为____________________________。
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为____________________________。
(5)“除铅、砷”时,可以采用以下两种方法。
①加入改性HAP。浸液1与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
L/S | 125:1 | 50:1 | 25:1 | 15:1 |
Pb2+去除率/% | 84.86 | 94.15 | 95.40 | 96.83 |
As3+去除率/% | 98.79 | 98.92 | 98.34 | 99.05 |
m(沉铋)/g | 2.34 | 2.33 | 2.05 | 1.98 |
实验中应采用的L/S=_________________________。
②铁盐氧化法,向浸液1中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。欲使溶液中c(AsO42-)<10-9mol/L且不产生Fe(OH)3沉淀,应控制pH的范围为__________。
已知:1g2=0.3:;FeAsO4、Fe(OH)3的Ksp分别为5×10-23、4×10-38。
(6)“沉铋“时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列说法正确的有( )
A.1molNa2O2晶体中共含有4NA个离子
B.0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒
C.常温常压下16gO2和O3混合气体含有NA个氧原子
D.1mol/LNa2CO3溶液中含有NA个CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡(NO2浓度约为0.0125mol/L).图中的曲线表示二氧化氮分解反应在前25s内的反应进程.
(1)前20秒内O2的平均生成速率:mol/(Ls)
(2)在某温度下达到平衡后,不改变其他条件,向该容器中再加入少量的NO2 , 平衡移动的方向是 , NO2的平衡转化率 68.75%(填“>”、“<”或“=”),NO的体积百分含量 (填“增大”、“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2+3H2![]() 2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A. 达到平衡时,反应速率:v(正)=v(逆)=0
B. 恒温恒压下,充入少量He,反应速率减慢
C. 升温正反应速率加快,逆反应速率减慢
D. 若在反应的密闭容器加入1 mol N2和过量的H2,最后能生成2 mol NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是由乙烯合成乙酸乙酯的几种可能的合成路线:

(1)乙烯中官能团的结构简式是___,乙醇中含氧官能团的名称是____。
(2)请写出上述几种路线中涉及到的有机化学反应基本类型,反应①:____,反应②:____。
(3)请写出④、⑤反应的化学方程式:
④__________________________;
⑤____________________________。
(4)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用下列装置来制备。完成下列填空:

①实验时,加入药品的顺序是____,该反应进行的比较缓慢,为了提高反应速率,一般要加入浓硫酸做催化剂,并____。
②反应结束后,将试管中收集到的产品倒入分液漏斗中,____、静置,然后分液。
③若用b装置制备乙酸乙酯,其缺点有____(答一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物 {[(CH3COO)2Cr]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒。已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
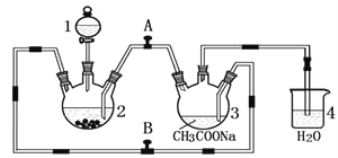
Zn(s)+ 2HCl(aq)=ZnCl2(aq)+ H2(g);
2CrCl3(aq)+Zn(s)= 2CrCl2(aq)+ ZnCl2(aq)
2Cr2+(aq)+ 4CH3COO—(aq)+ 2H2O(l)=[(CH3COO)2Cr]2·2H2O(s)
请回答下列问题:
(1)仪器1的名称是______________________________________。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是____________(填序号);目的是_________________________。
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液,一段时间后再加盐酸
C.先加盐酸,一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与醋酸钠溶液顺利混合,应关闭阀门_____(填“A”或“B",下同),打开阀门____。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与醋酸钠溶液反应外,另一个作用是_____________________________________________。
(5)已知其他反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[(CH3COO)2Cr]2·2H2O 9.4g,则该实验所得产品的产率为____________(不考虑溶解的醋酸亚铬水合物)。
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的_______,再加入碱液,调节pH至少为_______才能是铬的离子沉淀完全(铬的离子浓度应小于10-5mol/L)。【已知Cr(OH)3的溶度积为6.3×10-31,![]() ≈4,lg2≈0.3】
≈4,lg2≈0.3】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
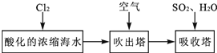
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)
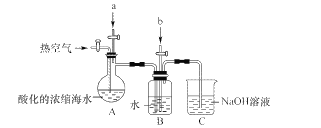
(1)A装置中通入a气体的目的是(用离子方程式表示)____。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是____。
(3)B装置中通入的b气体是____,目的是使溴蒸气转化为氢溴酸以达到富集的目的,试写出该反应的化学方程式____。
(4)C装置的作用是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料.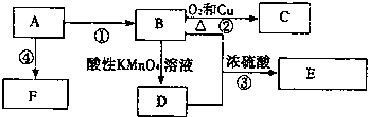
(1)A的电子式为 , F的结构简式 .
(2)D分子中的官能团名称是 , 请设计一种实验来验证D物质存在该官能团的方法是
(3)写出下列反应的化学方程式并指出反应类型:③ , 反应类型 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com