
| A、原混合物中n(Fe):n(Fe2O3)=2:1 |
| B、向溶液中滴入KSCN溶液,显红色 |
| C、无法计算原混合物的质量a |
| D、此时溶液中Fe2+和Fe3+的物质的量之比为3:1 |
| 0.224L |
| 22.4L/mol |
| 2 |
| 6 |
| 1 |
| 2 |
| 1 |
| 2 |


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
| A、同一物质的固、液、气三种状态的熵相同 |
| B、0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移 |
| C、等物质的量的钠分别在足量的氧气和氯气中燃烧,转移电子数相等 |
| D、1.5 mol NO2与足量H2O反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg和Al |
| B、Mg和Fe |
| C、Fe和Zn |
| D、Al和Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3++3H2O═Fe(OH)3+3H+ |
| B、HSO3-+H2O?H2SO3+OH- |
| C、CH3COO-+H2O?CH3COOH+OH- |
| D、A13++3HCO3-═Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
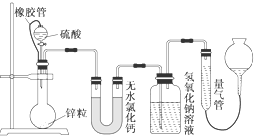 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.| n(H2) |
| n(SO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com