
【题目】PET是世界上产量最大的合成纤维,其结构简式为:
![]()
现以煤的干馏产品A 与F 为原料制备PET,生产的工艺流程如图所示。
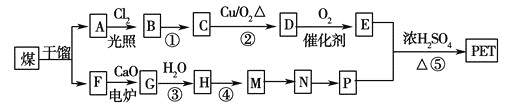
①A的分子式为C8H10,且能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。
②M分子里所有原子共平面。
③G 为CaC2,其与H2O 反应时元素化合价不变。
请回答下列问题:
(1)A的名称为__________。M→N 的反应类型为__________;
(2)反应①的反应条件为:__________;
(3)写出有机物A 所有一氯代物的结构简式:__________。
(4)写出下列反应的化学方程式:
①D与足量的氢氧化铜悬浊液煮佛:__________;
②反应⑤:__________。
(5)P的一种同系物X的分子式为C3H8O2 ,在核磁共振氢谱图中出现三种信号峰,其峰的强度之比为2∶1∶1。则X 的结构简式为__________。
【答案】 对二甲苯 加成反应 NaOH的水溶液,加热 ![]() 或
或
![]() +4Cu(OH)2+2NaO
+4Cu(OH)2+2NaO![]()
![]() +2Cu2O↓+4H2O n
+2Cu2O↓+4H2O n![]() +nHOCH2CH2OH
+nHOCH2CH2OH![]()
![]() +(2n-1)H2O
+(2n-1)H2O ![]()
【解析】(1).能使酸性高锰酸钾溶液褪色,但不能使溴水褪色,说明A为苯的同系物,且含有对位取代基,所以A为对二甲苯;已知M分子里所有原子共平面,M为乙烯,由于P为乙二醇,则M→N的反应类型为加成反应,生成卤代烃;
(2).B为卤代烃,反应①为卤代烃的水解,其反应条件为NaOH的水溶液,加热;
(3).Cl取代甲基中任一H原子均为同一种物质,且取代苯环上剩余任一H为另一种物质,即CH3-苯环-CH2Cl, ;
;
(4).①E含有羧基,则D含有醛基,所以此反应为醛基被氢氧化铜氧化的反应,由于氢氧化铜悬浊液的制备为硫酸铜溶液滴入氢氧化钠溶液中,所以反应方程式为:
![]() +4Cu(OH)2+2NaO
+4Cu(OH)2+2NaO![]()
![]() +2Cu2O↓+4H2O ;
+2Cu2O↓+4H2O ;
②反应⑤为缩聚反应,E为对二苯甲酸,P为乙二醇,在浓硫酸加热条件下脱水聚合,方程式为:n![]() +nHOCH2CH2OH
+nHOCH2CH2OH![]()
![]() +(2n-1)H2O;
+(2n-1)H2O;
(5). C3H8O2在核磁共振氢谱图中出现三种信号峰,其峰的强度之比为2:1:1,说明有三种不同的H原子,其中有两个羟基,为饱和烷烃的取代物,故答案为:![]() 。
。


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】已知NaHSO3溶液显酸性,还原性:HSO3->I-,氧化性:IO3->I2。在含3mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图。下列说法正确的是 ( )
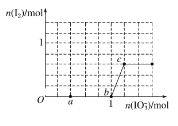
A. 反应过程中的氧化产物均为Na2SO4
B. a点时消耗NaHSO3的物质的量为1.0 mol
C. O~b间的反应可用如下离子方程式表示:3HSO3-+IO3-+3OH-===3SO42-+I-+3H2O
D. 当溶液中I-与I2的物质的量之比为5∶3时,加入的NaIO3为1.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组通过实验探究NO2的性质。已知:2NO2+2NaOH===NaNO3+NaNO2+H2O。
任务1:利用如图所示装置探究NO2能否被NH3还原(夹持固定装置已略去)。
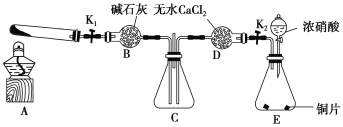
请回答下列问题:
(1)E装置中制取NO2的化学方程式是_____________________________。
(2)若NO2能被NH3还原,预期观察到C装置中的现象是________________。
(3)此实验装置存在的一个明显缺陷是_______________________________________。
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(4)实验前,该小组同学提出三种假设。
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3:________________________________________________。
(5)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。
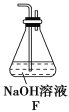
①装置的合理连接顺序是(某些装置可以重复使用)_________________。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中发生反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铟(In2O3)用作光谱纯试剂、光电显示半导体薄膜和电子元件的材料等,铟产业被称为“信息时代的朝阳产业”。利用水铟矿[主要成分为In(OH)3]制备In2O3的工艺流程如下:
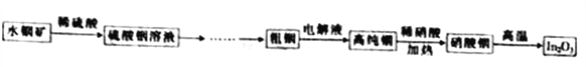
已知:常温下Ksp[In(OH)3]=1.41×10-33。
回答下列问题:
(1)In2O3中In的化合价为_________________。
(2)用硫酸酸浸水铟矿时发生反应的离子方程式为(杂质不参与反应)_________________。
(3)用硫酸从水铟矿中提取铟时,酸度与浸出率关系如图,则适宜硫酸的物质的量浓度为______。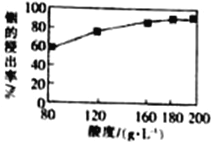
(4)高纯铟与稀硝酸反应的离子方程式为_________________。
(5)硝酸铟高温下生成氧化铟的同时又红棕色气体产生。写出该反应的化学方程式:________。
(6)粗铟电解精炼为高纯铟时、阳极的电极反应为_________________。
(7)水铟矿溶于硫酸中得到c(In3+)=1.41mol·L-1,要使In3+不产生沉淀,计算此时溶液的pH(写出必要的计算式)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气(CO+H2) 广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气,
(1)已知标况下,5.6LCH4与水蒸气完全反应时吸收51.5kJ的热量,请写出该反应的热化学方程式________________;
(2)在150℃时2L 的密闭容器中,将2molCH4和2mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=________。
②在该温度下,计算该反应的平衡常数K=________。
③下列选项中能表示该反应已达到平衡状态的是________。
A.V(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C(CH4)=C(CO)
(3)合成气中的氢气也用于合成氨气:N2+3H2![]() 2NH3。保持温度和体积不变,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是_______________;
2NH3。保持温度和体积不变,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是_______________;
容器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2 的体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | v甲 | P甲 |
乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | v乙 | P乙 |
丙 | 2L | 2molN2+6molH2 | n2 mol | φ丙 | v丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.v乙 >v>v甲 D.P乙>P甲=P丙
(4)合成气可以制取甲醚,绿色电源“二甲醚-氧气燃料电池”工作原理如下图所示
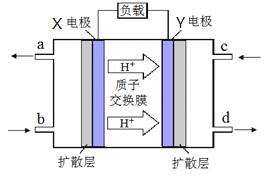
① 电极Y 上发生的反应式为__________ ;
②电池在放电过程中,电极X周围溶液的pH_______(填“增大、减小、不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.溶于水可以导电的化合物一定是离子化合物
B.在离子化合物中可能存在共价键
C.在共价化合物中可能存在离子键
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 若2.24L某气体中含有的分子数为0.1NA,则该气体所处的状态一定为标准状况
B. 一定条件下,密闭容器中1.4gN2与0.2molH2充分反应,转移的电子数为0.3NA
C. 0.1mol熔融状态下的NaHSO4中含有的阴离子数为0.2NA
D. 7.4g丁醇中存在的共价键总数为1.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com