
【题目】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动。
【探究一】
(1)甲同学将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________________。
【探究二】
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O===2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为________。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略):
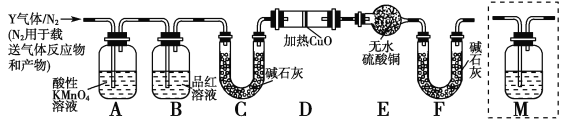
(3)装置B中试剂的作用是________。
(4)认为气体Y中还含有Q的理由是_____________________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于________(选填序号)。
a.A之前 b.A—B间 c.B—C间 d.C—D间
(6)如果气体Y中含有H2,预计实验现象应是_________________。
【答案】(1)铁钉表面被钝化(2)66.7%
(3)检验SO2是否除尽
(4)C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O(5)c
CO2↑+2SO2↑+2H2O(5)c
(6)D中固体由黑变红和E中固体由白变蓝
【解析】
试题分析:(1)铁钉放入冷硫酸中,浓硫酸有较强的氧化性能使铁钉钝化阻止反应进一步进行;
(2)①亚铁离子能使酸性高锰酸钾褪色,溶液中已经有三价铁离子,选择a会造成干扰,b能检验三价铁离子的存在,选c生成两种沉淀,受氢氧化铁沉淀颜色的影响无法分辨。
②SO2具有还原性,通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4,生成的硫酸遇到氯化钡会产生白色沉淀,则n(混合气体)=0.336L/22.4L/mol==0.015mol;

n=0.01mol
所以二氧化硫的体积分数为:0.01mol/0.015mol×100%=66.7%。、
(3)A除去二氧化硫,二氧化硫能使品红溶液褪色,所以B可以检验A中是否完全除去二氧化硫。
(4)在加热时,铁钉中不仅铁和浓硫酸反应,碳也和浓硫酸反应生成生成二氧化硫、二氧化碳和水,反应方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(5)Q为二氧化碳,二氧化碳和二氧化硫都能使澄清石灰水变浑浊,选择a或b受二氧化硫的影响无法判断二氧化碳的存在,选d时二氧化碳被碱石灰吸收。故选C;
(6)氢气还原氧化铜会生成水蒸气能使白色的硫酸铜粉末变蓝色,同时有红色的铜单质生成。


科目:高中化学 来源: 题型:
【题目】Ⅰ、工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产过程中会产生沉淀氢氧化铁,用来制取FeCO3的流程如下:
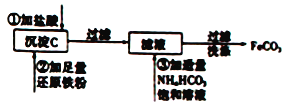
完成上述转化过程中的离子方程式
①____________________________。
②____________________________。
Ⅱ、有一瓶澄清溶液,其中可能含有可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、NO3-、CO32-、SO42-。取该溶液进行以下实验:
(1)填写表中开空白:
实验步骤 | 肯定不存在的离子 |
①用PH试纸检验,溶液呈强酸性 | |
②取出部分溶液,加入少量CCl4和数滴新制氯水,振荡,精置CCl4层呈紫红色 | |
③另取出部分溶液,向其加入NaOH溶液,使溶液从酸性变为碱性,在滴加过程中及滴加完毕后,均无沉淀产生 | |
④取③中的部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝 | |
⑤另取③中的部分碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成 |
(2)根据以上事实,该溶液中肯定存在的离子是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)===4C(g)+2D(g),在相同时间内,用不同物质表示的平均反应速率如下,则反应速率最快的是( )
A.v(A)=0.4 mol/(L·s) B.v(B)=0.8 mol/(L·s)
C.v(C)=1.2 mol/(L·s) D.v(D)=0.7 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)及其化合物可用于制半导体及除草剂等。回答下列问题:
(1)砷是氮的同族元素,比氮多2个电子层,砷在周期表中的位置为第__________周期___________族;AsH3的热稳定性比NH3___________(填“强”或“弱”)。砷在自然界中丰度最大的核素的中子数为40,该核素为______________(用元素符号表示)。
(2)砷化镓是常见的半导体材料,Ga与As同周期,镓最外层有3个电子,砷化镓的化学式为____________。
(3)某工业废水中含有少量的As2O3,向该废水中通入硫化氢可将其转化为更难溶的As2S3,该反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 石墨和C60互为同位素
B. CH4和CH3CH3互为同系物
C. 14CO2的摩尔质量为46
D. 3517Cl、3717Cl 为不同的核素,有不同的化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:

(1)溶液中一定含有的溶质是______________(填化学式)。
(2)溶液中一定不含有的溶质是____________(填化学式)。
(3)溶液中可能含有的溶质是__________(填名称),判断该物质是否存在的实验方法是________,现象是_____________。
(4)分别写出AB段、BC段发生的离子方程式:
①AB段为________________________________;
②BC段为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O![]() HCl+HClO K=4.5×10-4。次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
HCl+HClO K=4.5×10-4。次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为__________________________。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为________________________。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为____________________。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图)。

①下列溶液能吸收Cl2的是________(填字母序号)。
A.饱和食盐水
B.饱和Na2SO3溶液
C.饱和NaOH溶液
D.浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4LCCl4含有C—Cl键的数目为4NA
B.取50mL 14.0mol/L浓硝酸与足量铜片反应,生成气体分子的数目为0.35 NA
C.反应NH4N3![]() 2N2↑+2H2↑,标准状况下每生成22.4LN2,转移电子的数目为2 NA.
2N2↑+2H2↑,标准状况下每生成22.4LN2,转移电子的数目为2 NA.
D.电解精炼铜时,若转移的电子数为NA个,则阳极质量减小32g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com