
【题目】2019年10月9日诺贝尔化学奖颁给三位科学家,以表彰他们在锂离子电池领域的贡献。用镁代替锂可增加电池的能量密度,一种镁电池的总反应如下:![]() ,用该电池在碳棒上镀铜装置如图,下列说法正确的是
,用该电池在碳棒上镀铜装置如图,下列说法正确的是![]()
![]()
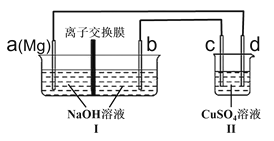
A.装置Ⅰ放电时的b电极反应式为:![]()
B.装置II中d极是碳棒,接通电路后,硫酸铜溶液浓度减小
C.装置I中最适合用阴离子交换膜,![]() 向b极移动
向b极移动
D.若用阴离子交换膜,有![]() 通过时,消耗镁12g
通过时,消耗镁12g
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钾(KIO3)是重要的食品添加剂。某化学兴趣小组设计下列步骤制取KIO3,并进行产品的纯度测定。
制取碘酸(HIO3)的实验装置示意图和有关资料如下:

HIO3 | ①白色固体,能溶于水,难溶于四氯化碳 ②Ka=0.169mol·L-1 |
KIO3 | ①白色固体,能溶于水,难溶于乙醇 ②碱性条件下易发生反应: ClO-+ IO3- =IO4 -+ Cl- |
回答下列问题:
步骤Ⅰ用 Cl2 氧化 I2 制取 HIO3
(1)装置 A 中发生反应的化学方程式_______。
(2)装置 B 中的 CCl4 可以加快反应速率,原因_______。
(3)反应结束后,获取 HIO3 溶液的操作中,所需玻璃仪器有烧杯、________和_______。
步骤Ⅱ用 KOH 中和 HIO3 制取 KIO3
(4)该中和反应的离子方程式为_______。中和之前,应将上述 HIO3溶液煮沸至接近无色,否则中和时易生成_______(填化学式)而降低 KIO3 的产量。
(5)往中和后的溶液中加入适量_______,经搅拌、静置、过滤等操作,得到白色固体。
(6)为验证产物,取少量上述固体溶于水,滴加适量 SO2 饱和溶液,摇匀,再加入几滴淀粉溶液,溶液变蓝。若实验时,所加的 SO2 饱和溶液过量,则无蓝色出现,原因是_______。
步骤Ⅲ纯度测定
(7)取 0.1000 g 产品于碘量瓶中,加入稀盐酸和足量 KI 溶液,用 0.1000 mol·L-1Na2S2O3溶液滴定,接近终点时,加入淀粉指示剂,继续滴定至终点,蓝色消失(I2+2S2O32-=2I-+S4O62-)。进行平行实验后,平均消耗 Na2S2O3 溶液的体积为 24.00 mL。则产品中 KIO3 的质量分数为_______。[M(KIO3)=214.0 g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:CH4+2O2+2KOU=K2CO3+3H2O,下列说法正确的是( )
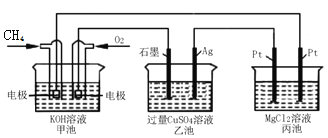
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池中正极的电极反应式是O2+4e-+4H+=2H2O
C. 反应过程中,乙池的pH逐渐减小
D. 甲池中消耗O2的体积与丙池生成气体的总体积在相同条件下的比值为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全固态锂硫电池是一种新型电池,其能量密度约为一般电子设备中广泛使用的锂离子电池的4倍,且成本更低廉。已知锂硫电池的总反应为![]() ,用此电池作电源电解足量的
,用此电池作电源电解足量的![]() 溶液,其工作原理如图所示。下列有关说法正确的是( )
溶液,其工作原理如图所示。下列有关说法正确的是( )
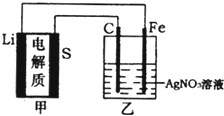
A.乙池溶液中的NO3![]() 移向铁电极
移向铁电极
B.乙池石墨电极反应式为![]()
C.甲池充电时,锂电极发生氧化反应
D.甲池中消耗14g锂,乙池中产生![]() 氧气
氧气![]() 标准状况下
标准状况下![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学知识在实际生产和生活中有广泛的用途,氢氧燃料电池![]() 乙池
乙池![]() 和电解的实验装置
和电解的实验装置![]() 甲池
甲池![]() 联合,把工业上有毒的废气
联合,把工业上有毒的废气![]() 含苯蒸汽
含苯蒸汽![]() 通过右图的装置一定条件下可实现有机物转化,实现废物的利用.从C出口为
通过右图的装置一定条件下可实现有机物转化,实现废物的利用.从C出口为![]() 气体
气体![]() 标准状况下
标准状况下![]() ,甲池中A为含苯蒸汽的物质的量分数为
,甲池中A为含苯蒸汽的物质的量分数为![]() 的混合气体,B为20mol混合气体,其中含苯蒸汽的物质的量分数为
的混合气体,B为20mol混合气体,其中含苯蒸汽的物质的量分数为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
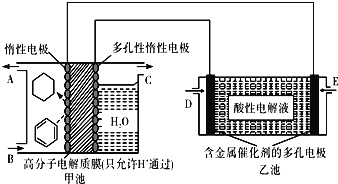
A.D极电极反应:![]()
B.E处通入![]() ,C处有
,C处有![]() 放出
放出
C.甲池中阴极区只有苯被还原
D.导线中共传导14mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷(C3H8)熔融盐燃料电池和锌蓄电池均为用途广泛的直流电源,放电时二者的总反应分别为C3H8+5O2=3CO2+4H2O,2Zn+O2=2ZnO。用丙烷(C3H8)燃料电池为锌蓄电池充电的装置如图所示,下列说法不正确的是

A. 物质M为CO2
B. 燃料电池消耗1mo1 O2时,理论上有4 mol OH-透过b膜向P电极移动
C. a膜、b膜均适宜选择阴离子交换膜
D. 该装置中,锌蓄电池的负极反应式为Zn+2OH--2e-=ZnO+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组设计如图所示装置,进行NO和![]() 假设二者物质的量之比为
假设二者物质的量之比为![]() 的处理并制取硝酸。下列说法正确的是
的处理并制取硝酸。下列说法正确的是![]()

A.ab适宜选用阴离子交换膜
B.该电池工作时,正极区溶液的pH减小
C.导线中流过![]() 电子的电量时,有
电子的电量时,有![]() 离子通过交换膜
离子通过交换膜
D.负极的电极反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲池的总反应式为2CH3OH+ 3O2+ 4KOH=2K2CO3+ 6H2O。试回答:
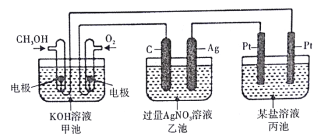
(1)图中甲池的装置是_________(填“原电池”或“电解池”),乙池中石墨电极是________极。
(2)写出通入CH3OH的电极的电极反应式:________________
(3)乙池中总反应的化学方程式为___________________
(4)当乙池中Ag极的质量增加5.40g时,甲池中理论上消耗O2________mL(标准状况);此时丙池某电极上析出1.60g某金属,则丙池中的盐溶液可能是________(填字母)
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com