
【题目】下列说法正确的是( )
A.反应2Mg+CO2![]() 2MgO+C ΔH<0从熵变角度看,可自发进行
2MgO+C ΔH<0从熵变角度看,可自发进行
B.在密闭容器发生可逆反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,ΔH变小
N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,ΔH变小
C.已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2.0×10-12,将等体积浓度为1.0×10-4mol/L的AgNO3溶液滴入到浓度均为1.0×10-4mol/L的KCl和K2CrO4的混合溶液中产生两种不同沉淀,且Ag2CrO4沉淀先产生
D.根据HClO的Ka=3.0×10-8,H2CO3的Ka1=4.3×10-7, Ka2=5.6×10-11,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,pH前者小于后者
【答案】D
【解析】
A.反应2Mg+CO2![]() 2MgO+C ΔH<0,从熵变角度看,该反应的混乱程度减小,因此不可自发进行,错误;
2MgO+C ΔH<0,从熵变角度看,该反应的混乱程度减小,因此不可自发进行,错误;
B.2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,即增大压强,化学平衡向正反应方向移动,重新达到平衡后,由于温度不变,所以ΔH不变,错误;
N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,即增大压强,化学平衡向正反应方向移动,重新达到平衡后,由于温度不变,所以ΔH不变,错误;
C.将等体积浓度为1.0×10-4mol/L的AgNO3溶液滴入到浓度均为1.0×10-4mol/L的KCl和K2CrO4的混合溶液中产生两种不同沉淀,反应产生AgCl沉淀需要的Ag+的浓度是c(Ag+)= 1.8×10-10÷1.0×10-4=1.8×10-6mol/L;反应产生Ag2CrO4沉淀需要的c(Ag+)=![]() ,可见先产生AgCl沉淀,错误;
,可见先产生AgCl沉淀,错误;
D.根据HClO的Ka=3.0×10-8,H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,CO32-水解程度大于ClO-,所以pH前者小于后者,正确。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】铁、铝是生活中重要的金属材料,铁铝及其化合物有非常重要的用途。
(1)下列说法不正确的是__________(填序号)。
①配制FeCl3、ACl3溶液时,均是先将固体FeCl3、ACl3溶于较浓的盐酸,再用蒸馏水稀释到所需浓度
②FeCl2、FeCl3、Fe(OH)3均可以通过化合反应生成
③利用氯水和KSCN溶液可以检验FeCl3溶液中有无Fe2+
④加热蒸干Al2(SO4)3溶液残留固体的成分为Al2O3
(2)以高碗铝土矿(主要成分为Al2O3、Fe2O3、SiO2、少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:

①流程中两次焙烧均会产生SO2,用NaOH溶液吸收处理SO2的离子方程式为___________。
②添加1%CaO和不添加CaO的矿粉焙烧其硫去除率随温度变化曲线如图所示。

已知:多数硫酸盐的分解温度都高于600℃
硫去除率=(1-![]() )×100%
)×100%
I.不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于__________。
Ⅱ.700℃时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是___________________。
③“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出该反应的化学方程式___________________。
(3)已知25℃时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33。
①在25℃下,向浓度均为0.1mo·L-1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成__________(填化学式)沉淀。
②溶液中某离子浓度低于1.0×10-5ml·L-1时,可以认为已沉淀完全。现向一定浓度的AlCl3和FeCl3混合溶液中逐滴加入氨水,当Fe3+恰好沉淀完全时,测得c(Al3+)=0.2mol·L-1,所得沉淀中__________(选填“还含有”或“不含有”)Al(OH)3。理由是___________________(通过计算说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行实验能达到相应实验目的的是
A.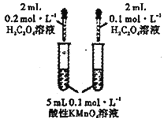 装置探究浓度对化学反应速率的影响
装置探究浓度对化学反应速率的影响
B. 装置探究催化剂对H2O2分解速率的影响
装置探究催化剂对H2O2分解速率的影响
C. 装置制取SO2气体并验证其还原性(可加热)
装置制取SO2气体并验证其还原性(可加热)
D. 装置防止铁钉生锈
装置防止铁钉生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0。某温度下,将 2 mol SO2 和 1 mol O2 置于 10L 密闭容器中,反应达平衡后,SO2 的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g)ΔH<0。某温度下,将 2 mol SO2 和 1 mol O2 置于 10L 密闭容器中,反应达平衡后,SO2 的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
甲 乙
乙 丙
丙
A.由图甲推断,B 点 SO3的平衡浓度为 0.3molL1
B.在图甲中,在此温度下,C 点 υ 正<υ 逆
C.达到平衡后,保持体积不变,充入氦气,压强增大,则反应速率变化图像可以用图乙表示
D.压强为 0.50 MPa 时,不同温度下 SO2 的平衡转化率与时间关系如图丙,则 T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.反应2NO2N2O4在室温下可自发进行,则该反应的△H<0
B.工业上电解熔融态氯化铝冶炼单质铝
C.CH3COOH溶液加水稀释后,溶液中![]() 的值增大
的值增大
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.1mol的四氧化二氮气体充入1 L抽空的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下数据:
浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/mol·L—1 | 0.1 | c1 | 0.05 | c3 | a | b |
c(NO2)/mol·L—1 | 0 | 0.06 | c2 | 0.12 | 0.12 | 0.12 |
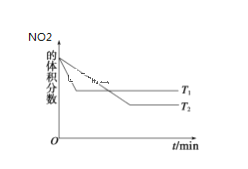
(1)该反应的化学方程式为______________________,表中c2_____c3_____a______b(选填“>”、“<”、“==”)。
(2)20 s时四氧化二氮的浓度c1=____________mol·l—1依据图象可以判断该反应的 ΔH___0(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
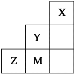
A.电负性:Y>Z>M
B.离子半径:M->Z2->Y-
C.ZM2分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子最外层电子轨道表示式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,可以证明反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①1个N≡N键断裂的同时有3个H—H键形成
②N2、H2、NH3的分子数之比为1∶3∶2
③1个N≡N键断裂的同时有6个N—H键形成
④N2、H2、NH3的浓度不再变化
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com