
����Ŀ�������£���1.000 mol/L�������20.00 mL1.000mol/L��ˮ�У���ҺpH���¶��������������仯������ͼ��ʾ�������й�˵����ȷ����

A. a����ˮ�������c(H��)=1.0��10-14 mol/L
B. b�㣺c(NH4+)+c(NH3��H2O)=c(Cl-)
C. c�㣺c(Cl-)=c(NH4+)
D. d��ǰ����Һ�¶���������Ҫԭ����NH3��H2O�������
���𰸡�C
��������
A.��ˮ�е���������ˮ����ģ����ݰ�ˮ��������Ũ�ȴ�С�����жϣ�
B.b��ʱpH>7������Ͱ�ˮ��Ӧ��ˮ��������Ӧ��Ϊ�Ȼ�狀Ͱ�ˮ�Ļ��Һ��
C.c����Һ��pH=7��Ϊ������Һ����c(H+)=c(OH-)�����ݵ���غ�����жϣ�
D.d��ǰ�����кͷ�Ӧ���кͷ�ӦΪ���ȷ�Ӧ��d�������백ˮǡ����ȫ�кͣ��¶ȴ���ߡ�
A.a��Ϊ��ˮ��Һ����ˮ�е�������Ϊˮ����ģ�����a����Һ��pH<14������Һ��������Ũ�ȴ���1.0��10-14mol/L������ˮ�������c(H+)>1.0��10-14mol/L��A����
B.������20.00mL����ʱ������Ͱ�ˮǡ����ȫ��Ӧ�õ�NH4Cl��Һ��NH4Cl��Һ�������Ҵ�ʱ��Һ�е������غ�Ϊc(NH4+)+c(NH3��H2O)=c(Cl-)��b����Һ��pH>7���������백ˮ��Ӧ��ˮ��������Ӧ��Ϊ�Ȼ�狀Ͱ�ˮ�Ļ��Һ�����������غ�֪c(NH4+)+c(NH3��H2O)>c(Cl-)��B����
C.c��pH=7����Һ�����ԣ���c(H+)=c(OH-)�����ݵ���غ��֪��c(Cl-)=c(NH4+)��C��ȷ��
D.�ᡢ���кͷ�Ӧ�Ƿ��ȷ�Ӧ����d��ǰ��������ļ��룬����кͷ�Ӧ�ų��������࣬ʹ��Һ���¶����ߣ�d��ʱ����Ͱ�ˮǡ����ȫ��Ӧ��������࣬d����ټ������¶Ƚ��ͣ������ڼ���������¶ȵ�����Һ�¶ȣ�D����
�ʺ���ѡ����C��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ƿ����һ�����ʵ���Ũ�ȵ�NaCl��Һ��ʵ���У���ʹ������ҺŨ��ƫ�ߵ���
A. ����NaCl����ʱ������������
B. û��ϴ���ܽ�NaCl������ձ��Ͳ�����
C. ����ʱ��ˮ�Ӷ��ˣ��õι�������Һ���̶���
D. ����ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨijK2SO4��Һ��Ũ�ȣ�ȡ25mL����Һ�������м������BaCl2��Һ����ַ�Ӧ����˲���õ�BaSO4����4.46g����K2SO4��Һ�����ʵ���Ũ���Ƕ��٣�(Ҫ��д������ļ�����̣��������һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������480mL0.2mol��L-1��NaOH��Һ��
(1)ͨ�������֪��Ӧ��������ƽ����_____��NaOH���塣
(2)��ʵ������Ҫ�IJ�����������Ͳ����ͷ�ιܡ��ձ����_____��
(3)������ѡ������IJ�����д����ȷ��˳��_____������ĸ����
A.ϴ�� B.��ȴ C.��ȡ D.���� E.���� F.ת����Һ G.ϡ�� H.�ܽ�
(4)��ʵ������г������������������Һ��Ũ���к�Ӱ��(����ƫ��������ƫ����������Ӱ����)��
�ٶ���ʱ������ˮ���������˿̶�_____��
������ƿ�������һ����ˮ��_____��
�۶���ʱ���ӹ۲쵽Һ��պõ���̶���_____��
(5)��NaOH��Һ��2.24L����(STP)��ǡ����ȫ��Ӧ��������������Һ_____mL��
(6)��18mol��L-1����������100mL1.0 mol��L-1���ᣬʵ��ʱӦѡ�õ�������_____�����ţ���
A.100mL��Ͳ B.������ƽ C.������ D.50mL����ƿ
E.10mL��Ͳ F.��ͷ�ι� G.50mL�ձ� H.100mL����ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ܱ������м��� 0.3 mol A��0.1 mol C ��һ������ B �������壬 һ�������·������·�Ӧ�� 3A(g) ![]() B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )
B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )
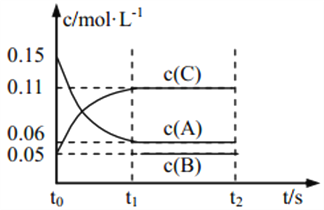
A. �� t1��15 s������ A ��Ũ�ȱ仯��ʾ t0��t1�ε�ƽ����Ӧ����Ϊ 0.004 mol��L��1��s��1
B. t1ʱ�÷�Ӧ�ﵽƽ�⣬ A ��ת����Ϊ 60%
C. ���������ݻ�Ϊ2 L��B����ʼ�����ʵ���Ϊ 0.02 mol
D. t0��t1 �Σ� �˹����������������Ƚ�������Ϊ a kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ 3A(g)![]() B(g)��2C(g) ��H����50a kJ��mol��1
B(g)��2C(g) ��H����50a kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�����Ϊ������ȱ�������涨��ʳ���б�����������ĵ���أ���ʵ������Ҫ����480mL 0.1mol/LKIO3��Һ��ʵ�ʲ��������У�
��1�����������ص�����Ϊ___g��
��2��������Һʱ���������У�
A.��ƿ B��������ƽ C.�ձ� D.��ͷ�ι� E.ҩ�� F.��Ͳ
����Ҫ�õ�����__������ţ�����ȱ�IJ���������___��___��д���ƣ���
��3�����dz������ƹ��̼���Ϊ���¸����裺
A����ȴ B������ C��ϴ�� D������ E���ܽ� F��ҡ�� G��ת�� H��װ���Լ�ƿ
����ȷ�IJ���˳��Ӧ��___(�����)��
��B E A G C G D F H ��B E G A C G F D H
��B E F G C G D H A ��B E A G C G D H F
��4���ڴ����ƹ����У����������ʹ���ƽ��ƫ�ߵ���____ (�����)��
��ת��ʱδϴ���ձ��Ͳ����� �ڶ���ʱ���ӿ̶��߹۲�Һ��
�۶���ʱ���ӿ̶��߹۲�Һ�� ������ƿ������ˮϴ�ɾ���δ����
��ҡ�Ⱥ��ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
��5������ʳ�����Ƿ�ӵ⣬���������·�Ӧ��KIO3+KI+H2SO4�� K2SO4+I2+H2O(δ��ƽ)
����ƽ�÷���ʽ��������˫���ŷ���ʾ�÷���ʽ����ת�Ƶķ������Ŀ��___��
�ڸ÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ___��
�������Ӧ��ת��0.5mol���ӣ�������I2�����ʵ���Ϊ____mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������ܱ������п��淴ӦH2(g)��I2(g) ![]() 2HI (g)�ﵽƽ��״̬�ı�־�� �� ��
2HI (g)�ﵽƽ��״̬�ı�־�� �� ��
A. ��������ѹǿ���ٱ仯
B. ��Ӧ����v(H2) =![]()
C. ����������ɫ���ٱ仯
D. c(H2)��c (I2)��c(HI)= 1��1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���CO��CO2��ɵĻ������Ϊ6.72 L������Ϊ12 g����:
��1�����������ܶ���_______�������������λС����
��2��CO��CO2�����ʵ���֮����________��
��3��CO�����������________��CO������������________��
��4�����������������ԭ�ӵ����ʵ�����_________������̼ԭ�ӵ����ʵ�����_________��
��5����������ƽ��Ħ��������_________��������������ܶ���__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ�������������װһ��װ�����ⶨ��������Ҫ�ɷ�FeS2���������������(����SO2��H2SO3�������ķ�Ӧ)��ʵ�����ȷ�����������£�
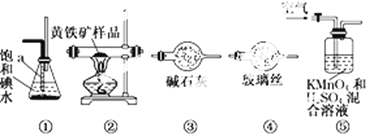
A�����Ӻ�װ�ã������װ�õ�������
B����ȡ��ϸ�Ļ�������Ʒ
C����2.0 g��ƷС�ĵط���Ӳ�ʲ�������
D����1 L/min�����ʹ������
E����Ӳ�ʲ������еĻ�������Ʒ���ȵ�800�桫850��
F����300 mL�ı��͵�ˮ����SO2�������ķ�Ӧ�ǣ�I2��SO2��2H2O = 2HI��H2SO4
G������Һ��CCl4��ȡ������
H��ȡ20.00mLG��������Һ����0.2000mol��L��1��NaOH����Һ�ζ����Իش�
��1������G��������Ҫ������______��Ӧȡ_______ (����������������)����Һ���к���ʵ�顣
��2��װ����ȷ������˳���� ![]()
![]()
![]() ��
�� ![]() (����)��______
(����)��______
��3��װ�â��и�����ص�������__________�������������������__________��
��4������H�еζ�ʱӦѡ��_____��ָʾ�������Ը���________�������жϵζ��Ѿ��ﵽ�յ㡣
��5���ٶ��������е����ڲ���E����ȫ��ת��ΪSO2�����ұ����͵�ˮ��ȫ���գ��ζ��õ����������±���ʾ��
�ζ����� | ����Һ�����/mL | NaOH����Һ�����/mL | |
�ζ�ǰ | �ζ��� | ||
��һ�� | 20.00 | 0.00 | 20.48 |
�ڶ��� | 20.00 | 0.22 | 20.20 |
������ | 20.00 | 0.36 | 20.38 |
���������Ʒ����Ԫ�ص���������Ϊ___________��
��6��Ҳ������������������������ⶨ�������к��������������������ַ����ⶨ���������װ�â���������Һ�м������������Լ�__________ ��
A.��������Һ B.�Ȼ�����Һ C.����ʯ��ˮ D.���Ը��������Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com