
| A、将100g水倒入100g 98% 硫酸溶液中配制成49% 的硫酸溶液 |
| B、给试管里的液体加热时,液体体积不得超过试管容积的1/3 |
| C、使用胶头滴管时,应将滴管尖嘴伸进试管内,以免液体外流 |
| D、不小心将浓硫酸洒到桌面上,应先用抹布擦,再用大量水冲洗 |


科目:高中化学 来源: 题型:
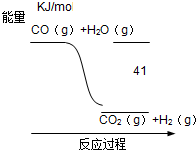
| A、CO+H2O═CO2+H2 △H=-41 KJ/mol |
| B、CO(g)+H2O(g)═CO2(g)+H2(g)△H=+41 KJ/mol |
| C、CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 KJ/mol |
| D、CO2(g)+H2(g)═CO(g)+H2O(g)△H=-41 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味 |
| B、用排水集气法便可以收集到纯净的氯气 |
| C、干燥的氯气有漂白性 |
| D、自来水常用氯气来杀菌、消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锥形瓶用待测溶液润洗 |
| B、碱式滴定管可不用碱液润洗 |
| C、盐酸滴定氢氧化钠溶液时可以用甲基橙作指示剂 |
| D、滴定操作时,眼睛应注视滴定管中液面的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
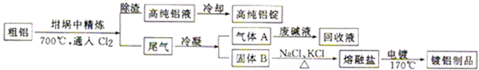
查看答案和解析>>
科目:高中化学 来源: 题型:
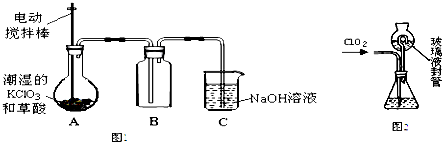
查看答案和解析>>
科目:高中化学 来源: 题型:
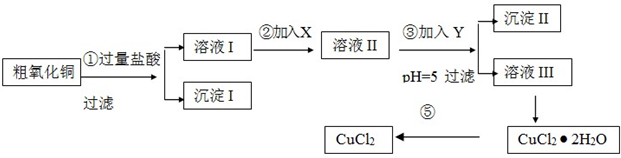
| 氧化剂 | 调节pH的物质 | ||
| A | 双氧水 | E | 氨水 |
| B | 高锰酸钾 | F | 碱式碳酸铜 |
| C | 氯水 | G | 氧化铜 |
| D | 硝酸 | H | 氢氧化铜 |
| 物质 | 开始沉淀时pH | 完全沉淀时pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 5.2 | 6.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com