
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.3 mol |
| B.n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
C
解析试题分析:由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n(NaClO)+n(NaClO3)=0.03L×10mol·L-1=0.3mol,根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3)=0.3mol,故参加反应的氯气n(Cl2)=0.15mol,故A错误;根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl-)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl-)最小为6:5,故6:5<n(Na+):n(Cl-)<2:1,7:3>2:1,故B错误;根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,为0.3mol×1 2 ×1=0.15mol,氧化产物只有NaClO3,转移电子数最多,为0.3mol×5 6 ×1=0.25mol,故C正确;令n(NaCl)=11mol,n(NaClO)=2mol,n(NaClO3)=1mol,生成NaCl获得的电子为11mol×1=11mol,生成NaClO、NaClO3失去的电子为2mol×1+1mol×5=7mol,得失电子不相等,故D错误;故选C。
考点:考查氧化还原反应计算。


科目:高中化学 来源: 题型:单选题
用0.1 mol/L的Na2SO3溶液30 mL,恰好将2×10-3 mol XO4-还原,则元素X在还原产物
中的化合价是
| A.+4 | B.+3 | C.+2 | D.+1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
2008年我国的“神舟七号”宇宙飞船搭载3名宇航员顺利升空,并成功实现宇航员太空行走。火箭和飞船升空所需的巨大能量可由下列化学反应提供:C2H8N2 + 2N2O4 = 2CO2↑ + 3N2↑ + 4H2O
有关该反应的说法正确的是( )
| A.该反应是分解反应 | B.反应中碳元素的化合价降低 |
| C.氧化剂是N2O4 | D.该反应不是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:(1)Tl3++2Ag=Tl++2Ag+,(2)Ag++Fe2+=Ag+Fe3+,(3)Fe+2Fe3+=3Fe2+,下列离子氧化性比较顺序正确的是 ( )。
| A.Tl3+>Fe3+>Ag+ | B.Fe3+>Ag+>Tl3+ |
| C.Tl+>Ag+>Fe2+ | D.Tl3+>Ag+>Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠
(Na2Cr2O7·2H2O),其主要反应:( )
①4FeO·Cr2O3+8Na2CO3+7O2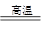 8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4
8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法不正确的是( )
| A.反应①和②均为氧化还原反应 |
| B.Na2Cr2O7在碱性条件下可转化为Na2CrO4 |
| C.高温下,O2的氧化性大于Fe2O3和Na2CrO4的 |
| D.生成1 mol Na2Cr2O7时转移电子的物质的量大于7 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中能表明金属甲的活动性比金属乙的活动性强的是( )。
| A.在氧化还原反应中,甲失电子数比乙多 |
| B.同价态阳离子甲比乙氧化性强 |
| C.甲能跟盐酸反应放出H2而乙可与冷水反应产生H2 |
| D.甲、乙与H2SO4溶液形成原电池,乙上冒气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙、丙三种溶液中各有一种X-(X-为Cl-、Br-或I-),向甲中加入淀粉溶液和氯水,溶液变为橙色,再加丙溶液,颜色无明显变化,则甲、乙、丙中依次含有( )。
| A.Br-、I-、Cl- | B.Br-、Cl-、I- | C.I-、Br-、Cl- | D.Cl-、I-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
200°C时,11.6克CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体的质量增加了3. 6克。从以上信息中,我们得出的下列结论中不正确的是( )
| A.可以计算出混合气体中CO2和水蒸气的质量 |
| B.可以判断出混合气体的平均摩尔质量 |
| C.可以计算出该反应中转移的电子数 |
| D.可以总结出Na2O2任何反应中既作氧化剂也作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片与稀H2SO4反应 |
| B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.灼热的炭与CO2反应 |
| D.甲烷在O2中的燃烧反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com