
【题目】某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。
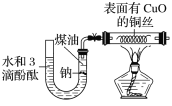
根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象________。
(2)U形管中溶液的颜色_____,说明有__________生成。
(3)铜丝的变化现象____________,说明有________生成;若去掉后面的装置,简述检验气体的方法____
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______。
【答案】在水和煤油的界面上逐渐变小并作上下跳动 从上到下逐渐由无色变为红色 NaOH 由黑色变红色 H2 在玻璃管口处点燃气体,有淡蓝色火焰产生 ![]() ×100%
×100%
【解析】
该实验的目的是检验钠与水的反应产物。观察装置,左边的U形管中有H2产生(2Na+2H2O=2NaOH+H2↑);在水中滴加了酚酞,若溶液变红,可以证明有NaOH生成;若铜丝表面由黑色变为红色,可以说明有H2生成。
(1)钠的密度比水小,比煤油大;钠与水接触后会产生H2(2Na+2H2O=2NaOH+H2↑),并被H2推起来,又由于重力的作用,钠块会称降到水和没有的界面上,再次与水接触产生H2,就这样不断往复地在水和没有的界面上上下跳动,由于每次跳动都有H2生成,所以可以看到钠块不断被消耗,逐渐变小,直至消失;
(2)钠和水反应有NaOH生成,故可以看到U形管中的溶液变红,故可以通过该现象证明有NaOH生成;
(3)钠和水反应有H2生成,H2可以在加热的条件下还原CuO为Cu,对应的现象是黑色固体变红,故可以通过铜丝表面颜色的变化来证明有H2生成;检验H2的方法还有其他,比如:①用试管收集气体之后,对准燃着的酒精灯,松开手指可以听到爆鸣声,也可以②通过观察燃烧时火焰的颜色,淡蓝色的火焰可以证明有H2生成;
(4)根据反应的现象可以推出水一定是过量的,故需要通过Na的质量来计算反应各体系消耗和生成的量:
2Na+2H2O=2NaOH+H2↑
2×23 2×40 2
a g ![]() g
g ![]() g
g
则w(NaOH)=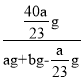 ×100%=
×100%=![]() ×100%。
×100%。


科目:高中化学 来源: 题型:
【题目】苯乙烯是制备聚苯乙烯的单体。工业上,利用乙苯催化脱氢制取苯乙烯的反应:
![]() (g)+CO2(g)
(g)+CO2(g)![]()
![]() (g)+CO(g)+ H2O(g) △H
(g)+CO(g)+ H2O(g) △H
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
![]()
利用上表数据估算△H为___________。
(2)在三个体积相同的恒容密闭容器中充入CO2和乙苯蒸气发生上述反应,有关数据如下:

①T1______T2(填“>”“<”或“=”,下同),a___________2.0。
②T1K时,容器I中平衡混合气体中苯乙烯体积分数为___________,假设容器I中起始压强为p0,用平衡分压代替平衡浓度表示的化学平衡常数Kp=___________。[气体分压(p分)=气体总压(p总)×气体体积分数]
(3)一定温度下,在某催化剂作用下发生上述反应,其反应历程如下:
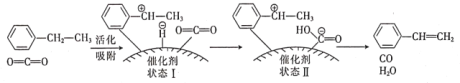
①由原料到状态I__________(填“放出”或“吸收”)能量,判断依据是_______。
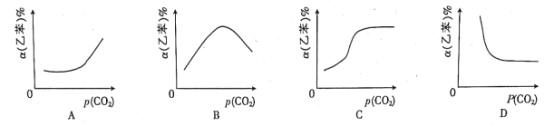
②如果其他条件不变,再通入CO2,如图所示的四幅图像中,符合乙苯平衡转化率与p(CO2)的关系的是___________。(填选项)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是探究某气体化学性质的实验装置,图中B为活塞。如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C中红色布条颜色褪去。则D瓶中盛有的溶液是( )
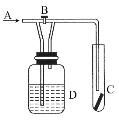
A.浓H2SO4B.饱和NaCl溶液
C.NaOH溶液D.NaBr溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科学家研制出一种高分子大规模储能二次电池,其示意图如下所示。这种电池具有寿命长、安全可靠等优点,下列说法错误的是
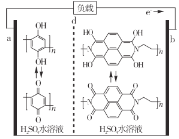
A.硫酸水溶液主要作用是增强导电性
B.充电时,电极b接正极
C.d膜是质子交换膜
D.充放电时,a极有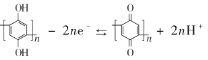
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用热的氢氧化钠溶液洗去试管内壁沾有的硫单质,发生反应6NaOH+3S![]() 2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
A. 硫既是氧化剂又是还原剂 B. 硫化钠是还原产物
C. 硫既表现氧化性又表现还原性 D. 消耗3 mol 硫,转移电子6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
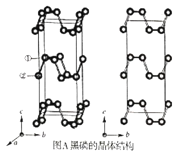
【题目】黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A,c=10.500A。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样,图A中编号为①的P原子的晶胞内坐标为(0.50,0.090,0.598)。请回答下列问题:
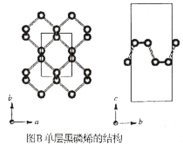
(1)写出P原子的价电子排布:___。
(2)P和F的电负性大小顺序是X(P)___X(F)。(填“<”“=”或“>”)P和F形成的分子PF3和PF5,它们的几何构型分别为__、__。
(3)①黑磷中P原子杂化类型是__。黑磷中不存在__(选填字母序号)。
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__,原因是__。
(4)图A中编号为②的P原子的晶胞内坐标为__,黑磷的晶胞中含有__个P原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用某酸性腐蚀废液(含Fe3+、Cu2+、NH4-、SO42-),制取铵明矾[NH4Al(SO4)2·12H2O]的流程如下:
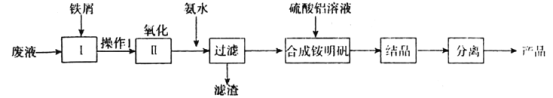
回答下列问题:
(1)加入铁屑的目的是______________________。
(2)第II步中用双氧水作为氧化剂。请写出步骤II氧化反应离子方程式__________________。
(3)检验溶液中含有NH4+的方法是______________________。
(4)工业上将流程中产生的滤渣用NaClO碱性溶液氧化可生成一种高效净水剂(Na2FeO4),写出对应的离子方程式:_________________________________。
(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示。
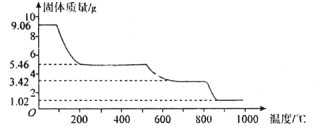
若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为___________。在温度从800℃到950℃的过程中得到的两种氧化物,一种为固体,一种为氧化性气体,该气体的名称是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象表示的意义与相关的化学反应完全正确的是
A.向FeCl3溶液中不断加入铁粉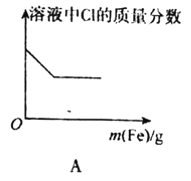
B.Fe(OH)2固体露置在空气中质量的变化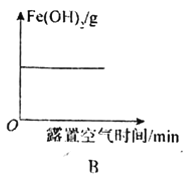
C.25℃时,向Cl2水溶液中通入二氧化硫(生成两种常见的酸) 
D.向AlCl3溶液中不断滴入烧碱溶液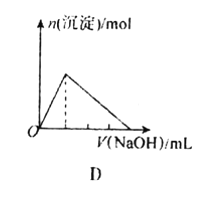
查看答案和解析>>
科目:高中化学 来源: 题型:
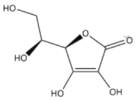
【题目】维生素C,结构简式如下图。可用碘量法测定含量。取2片维生素C片剂,溶于蒸馏水,定容至250mL,取50mL,用0.0l0mol/LI2标准液滴定至终点,重复实验,数据如下:
序号 | 滴定前读数 | 滴定后读数 |
1 | 1.00 | 25.98 |
2 | 1.24 | 25.36 |
3 | 1.38 | 26.40 |
已知:维生素C与I2按等物质的量恰好反应。
(1)该维生素C片溶液中维生素C的浓度为___mg/L。
(2)移取80mL橙汁于锥形瓶中,滴入lmL盐酸调节酸度,用0.010mol/LI2的标准溶液滴定至终点,消耗标准液10.12mL,则橙汁中维生素C的含量为____mg/L。简要写出计算过程。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com