
【题目】(1)碳能与氢、氮、氧三种元素组成化合物CO(NH2)2,该物质易溶于水的主要原因是____。
(2)碳元素能形成多种无机物。
①CO32-的立体构型是________。
②MgCO3分解温度比CaCO3低的原因是___________。
(3)图①为嘌呤的结构,嘌呤中轨道之间的夹角∠1比∠2大,请解释原因:____________。
(4)图②为碳的一种同素异形体C60分子,每个C60分子中含有![]() 键的数目为________。
键的数目为________。
(5)图③为碳的另一种同素异形体一一金刚石的晶胞结构,其中原子坐标参数A为(0,0,0),B为(![]() ),C为(
),C为(![]() );则D原子的坐标参数为________。
);则D原子的坐标参数为________。
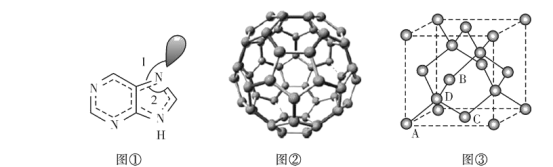
(6)副族元素Mn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图①所示,其中(〇为Se,●为Mn),则Se的配位数为____,Mn和Se的摩尔质量分别为M1 g/mol、M2 g/mol,该晶体的密度为![]() g/cm3,则Mn-Se键的键长为_____nm(写表达式即可)。
g/cm3,则Mn-Se键的键长为_____nm(写表达式即可)。
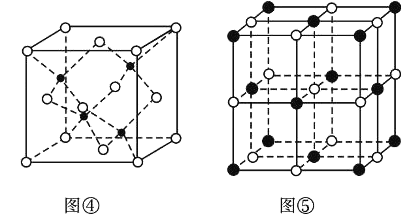
(7)KI的晶胞结构如图⑤所示,已知其晶体的密度为![]() g/cm3,K和I的摩尔质量分别为Mk gmol-1和MI gmol-1,原子半径分别为rk pm和rI pm,阿伏加德罗常数的值为NA,则KI晶胞中原子的体积占晶胞体积的百分率为______(写表达式即可)。
g/cm3,K和I的摩尔质量分别为Mk gmol-1和MI gmol-1,原子半径分别为rk pm和rI pm,阿伏加德罗常数的值为NA,则KI晶胞中原子的体积占晶胞体积的百分率为______(写表达式即可)。
【答案】CO(NH2)2分子与水分子之间能形成氢键 平面三角形 氧化镁晶格能比氧化钙大,使得Mg2+比Ca2+更容易结合CO32-在的氧离子 孤电子对与键合电子对之间的斥力大于键合电子对之间的斥力,斥力大,键角大 90 (![]() ) 4
) 4 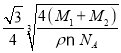 ×107
×107  ×100%
×100%
【解析】
(1)化合物CO(NH2)2分子与水分子之间存在氢键,增加了分子之间的吸引力;
(2)①用价层电子对数分析CO32-的立体构型;
②用晶格能大小分析解答;
(3)根据VSEPR理论,孤电子对对键合电子对之间的斥力大于键合电子对对键合电子对之间的斥力,导致键合电子对对键合电子对之间的夹角减少;
(4)每个碳原子形成3个σ键,每σ键为2个碳原子共有,则平均每个碳原子形成1.5个σ键;
(5)D与周围4个原子形成正四面体结构,D与顶点A的连线处于晶胞体对角线上,过面心B、C及上底面面心原子的平面且平行侧面将晶胞2等分,同理过D原子的且平衡侧面的平面将半个晶胞2等份,可知D到各坐标平面的距离均为晶胞棱长![]() ;
;
(6)在晶体中每个Se原子连接4个Mn原子、每个Mn原子连接4个Se原子;用均摊方法计算晶胞中Se、Mn原子个数,利用密度ρ=![]() 计算晶胞参数,然后根据距离最近的Se原子和Mn原子的距离为晶胞体长的
计算晶胞参数,然后根据距离最近的Se原子和Mn原子的距离为晶胞体长的![]() 计算距离最近的Se原子和Mn原子的距离;
计算距离最近的Se原子和Mn原子的距离;
(7)根据立体几何知识分析,晶胞边长根据密度和摩尔质量计算,据此计算。
(1)化合物CO(NH2)2分子与水分子之间存在氢键。增加了分子之间的吸引力,使尿素容易溶于水中;
(2)①CO32-的价层电子对数为3+![]() =3,无孤对电子,所以CO32-的立体构型为平面三角形;
=3,无孤对电子,所以CO32-的立体构型为平面三角形;
②Mg、Ca是同一主族的元素,MgCO3分解温度比CaCO3低的原因是由于氧化镁晶格能比氧化钙大,使得Mg2+比Ca2+更容易结合CO32-在的氧离子;
(3)根据VSEPR理论,孤电子对对键合电子对之间的斥力大于键合电子对对键合电子对之间的斥力,导致键合电子对对键合电子对之间的夹角减少,所以嘌呤中轨道之间的夹角∠1比∠2大;
(4)每个碳原子形成3个σ键,每σ键为2个碳原子共有,则平均每个碳原子形成1.5个σ键,则C60分子中有化学键σ键数目为60×1.5=90;
(5)D与周围4个原子形成正四面体结构,D与顶点A的连线处于晶胞体对角线上,过面心B、C及上底面面心原子的平面且平行侧面将晶胞2等分,同理过D原子的且平衡侧面的平面将半个晶胞2等份,可知D到各坐标平面的距离均为晶胞棱长![]() ;
;
(6)在晶体中每个Se原子连接4个Mn原子、每个Mn原子连接4个Se原子,所以Se原子的配位数是4;在一个晶胞中含有Se的原子个数为:![]() ×8+
×8+![]() ×6=4;含有的Mn原子数为4,晶胞密度为ρg/cm3,晶胞参数L=
×6=4;含有的Mn原子数为4,晶胞密度为ρg/cm3,晶胞参数L=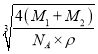 cm,晶胞体对角线长度为
cm,晶胞体对角线长度为![]() L=
L=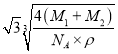 cm,由于距离最近的Se原子和Mn原子的距离为晶胞体长的
cm,由于距离最近的Se原子和Mn原子的距离为晶胞体长的![]() ,因此距离最近的Se原子和Mn原子的距离为
,因此距离最近的Se原子和Mn原子的距离为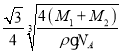 ×107nm;
×107nm;
(7)一个晶胞中,含有4个KI,所以一个晶胞中,V球=4×![]() π(
π(![]() +
+![]() )=
)=![]() π(
π(![]() +
+![]() ),KI晶体的密度为ρg/cm3,K和I的摩尔质量分别为MK g/mol和MI g/mol,则ρ=
),KI晶体的密度为ρg/cm3,K和I的摩尔质量分别为MK g/mol和MI g/mol,则ρ=![]() ,a3=
,a3=![]() ×1030,所以KI晶胞中原子的体积占晶胞体积的百分率为
×1030,所以KI晶胞中原子的体积占晶胞体积的百分率为![]() ×100%=
×100%=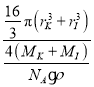 ×10-30×100%=
×10-30×100%=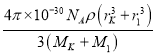 ×100%。
×100%。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g) ![]() xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。求:
xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。求:
①2 s内用物质A表示的平均反应速率为________________。
②2 s内用物质B表示的平均反应速率为__________________________。
③2 s时物质B的转化率为______________________。
④x=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源,某学习小组在实验室模拟从海水提取氯化钠晶体,其实验流程如下:

通过查阅资料可知:粗盐中含有CaCl2、MgCl2、Na2SO4等杂质。该学习小组通过讨论,设计实验在从粗盐精制得到食盐水的过程为:
①取一定量的粗盐溶解;
②向粗盐水中依次加入过量的Na2CO3溶液、加入过量的NaOH、加入过量的BaCl2溶液;
③过滤;
④向滤液中加入适量盐酸。
回答:
(1)溶解时需要的仪器有________。
(2)加入过量的Na2CO3溶液时观察到的现象是________;反应的化学方程式为_______________________________。
(3)实验后,通过进一步反复论证,向老师求证,发现在粗盐精制得到食盐水的设计方案中________(“有”或“没有”)不妥之处,理由是______________________。
(4)该学习小组同学要从食盐水得到氯化钠晶体时,还要进行________、______、过滤。
(5)该学习小组同学用实验得到的晶体配制1mol·L-1的NaCl溶液500mL,在配制过程中,下列操作会引起浓度偏高的是________。
①没有洗涤烧杯和玻璃棒
②容量瓶不干燥,含有少量蒸馏水
③定容时仰视刻度线
④定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空
(1)1.7gNH3与标况下_________LH2S中的氢原子数相同
(2)在标准状况((___________)℃ 、_____________KPa)下,CO和CO2的混合气体共4.48L,质量为7.2g。则两种气体的物质的量之和为____________mol,该混合气体的平均相对分子质量为___________,其中CO2为___________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟合成医药中间体X和Y。
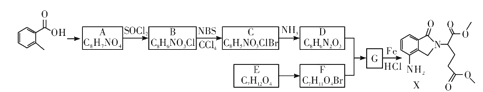
已知:①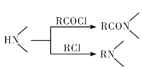 ;
;
②![]() ;
;
③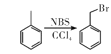 。
。
(1)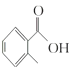 的名称是__________
的名称是__________
(2)G→X的反应类型是_____________。
(3)化合物B的结构简式为_____________。
(4)下列说法不正确的是__________(填字母代号)
A. 化合物A能使酸性KMnO4溶液褪色
B.化合物C能发生加成、取代、消去反应
C.化合物D能与稀盐酸反应
D.X的分子式是C15H16N2O5
(5)写出D+F→G的化学方程式:____________________
(6)写出化合物A(C8H7NO4)同时符合下列条件的两种同分异构体的结构简式_______。
①分子是苯的二取代物,1H—NMR谱表明分子中有4种化学环境不同的氧原子;
②分子中存在硝基和![]() 结构。
结构。
(7)参照以上合成路线设计E→![]() 的合成路线(用流程图表示,无机试剂任选)。
的合成路线(用流程图表示,无机试剂任选)。
____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )

A.反应的化学方程式为2N![]() M
M
B.t2时,正逆反应速率相等达到平衡状态
C.t1时,M的浓度是N浓度的2倍
D.t3时,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从香荚兰豆中提取的一种芳香化合物,其分子式为C8H8O3,遇FeCl3溶液会呈现特征颜色,能发生银镜反应。该化合物可能的结构简式是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是__,画出配合物离子[Cu(NH3)4]2+中的配位键__.
(2)根据VSEPR模型,H3O+的分子立体结构为__,BCl3的立体结构为__.
(3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种)
正四面体分子__,三角锥形分子__,V形分子______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钒炉渣(主要含V2O3,还有少量SiO2、P2O5等杂质)为原料可以制备氧钒碱式碳酸铵晶体[(NH4)5(VO)6(CO3)4(OH)9·10H2O],其生产工艺流程如下。
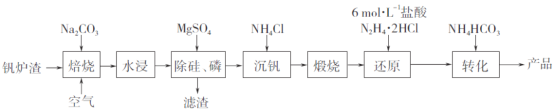
(1)焙烧过程中V2O3转化为可溶性NaVO3,该反应的化学方程式为_________________________________。
(2)滤渣的主要成分是________________(写化学式)。
(3)“沉钒”得到偏钒酸铵(NH4VO3),若滤液中c(VO3-)=0.1mol·L-1,为使钒元素的沉降率达到98%,至少应调节c(NH4+)为____mol·L-1。[已知Ksp(NH4VO3)=1.6×10-3]
(4)“还原”V2O5过程中,生成VOC12和一种无色无污染的气体,该反应的化学方程式为_______________________。用浓盐酸与V2O5反应也可以制得VOC12,该方法的缺点是____________________________。
(5)称量a g产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知滴定反应为VO2++Fe2++2H+==VO2++Fe3++H2O)
①KMnO4溶液的作用是______________。
②粗产品中钒的质量分数表达式为________(以VO2计)。
③若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果_____(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com