
【题目】大气污染的危害是多方面的,它既危害人体健康,又影响动植物的生长,严重时会影响地球的气候。大气污染主要是由人为排放的烟尘和有害气体造成的。
(1)工业接触法制硫酸的主要反应之一是2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol
①一定条件下,将SO2于空气充分混合并反应。t min后,SO2和SO3物质的量浓度分别为amol/L和bmol/L,则以SO2表示的化学反应速率为________________
②为了提高反应速率,同时提高SO2的转化率,从而减少SO2的排放,下列条件可改变的是_______
A 增大压强 b升高温度 c增大催化剂用量d降低温度
(2)CO2的过度排放会造成另一种大气污染——“温室效应”。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径
①下列措施中,有利于降低大气中CO2浓度的有_____________
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
②另一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l) = C2H4(g)+3O2(g) △H=+1411.0kJ/mol
2CO2(g)+3H2O(l) = C2H5OH(l)+3O2(g) △H=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是:____________________________________________。
③在一定条件下:6H2(g)+2CO2(g)![]() CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。

根据上表中数据分析:
i.温度一定时,提高碳氢比[n(H2)/n(CO2)],CO2的转化率________(填“增大”“减小”或“不变”)
ii.该反应的正反应为_______(填“吸”或“放”)热反应
iii.为了避免乙醇燃烧释放CO2,可以设计成乙醇燃料电池,右图为该电池的结构示意图(电解质溶液为KOH溶液)。则a处电极上的电极反应式为______________________________。

【答案】 b/t mol L-1 min-1 a abc C2H4(g)+H2O(l)=C2H5OH(l) △H =-44.2kJ/mol 增大 放 C2H5OH - 12e-+16OH-==2CO32-+11H2O
【解析】试题分析:(1)①根据![]() 计算SO2反应速率; ②增大压强、升高温度 、增大催化剂用量可以提高反应速率;2SO2(g)+O2(g)
计算SO2反应速率; ②增大压强、升高温度 、增大催化剂用量可以提高反应速率;2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6kJ/mol,升高温度平衡逆向移动、降低温度平衡正向移动、增大压强平衡正向移动;催化剂不能使平衡移动。(2)①减少化石燃料的用量 ,鼓励乘坐公交车出行,倡导低碳生活 ,利用太阳能、风能等新型能源替代化石燃料,可以减少二氧化碳的排放。②根据盖斯定律计算乙烯水化制乙醇的焓变;③i.增大一种反应物的浓度,平衡正向移动,可以提高另一种反应物的转化率。ii.根据表格数据,升高温度,CO2的转化率减小,平衡逆向移动。iii.根据电池的结构示意图,电子由a流向b,a极失电子是负极。
2SO3(g) △H=-196.6kJ/mol,升高温度平衡逆向移动、降低温度平衡正向移动、增大压强平衡正向移动;催化剂不能使平衡移动。(2)①减少化石燃料的用量 ,鼓励乘坐公交车出行,倡导低碳生活 ,利用太阳能、风能等新型能源替代化石燃料,可以减少二氧化碳的排放。②根据盖斯定律计算乙烯水化制乙醇的焓变;③i.增大一种反应物的浓度,平衡正向移动,可以提高另一种反应物的转化率。ii.根据表格数据,升高温度,CO2的转化率减小,平衡逆向移动。iii.根据电池的结构示意图,电子由a流向b,a极失电子是负极。
解析:(1)①t min后, SO3物质的量浓度分别为bmol/L,则消耗SO3物质的量浓度bmol/L,根据![]() ,
,![]() b/t mol L-1 min-1;②A 增大压强,反应速率加快、平衡正向移动,故A正确; b升高温度,平衡逆向移动,故b错误; c增大催化剂用量,平衡不移动,故c错误; d降低温度,反应速率减慢,故d错误。(2)①减少化石燃料的用量 ,鼓励乘坐公交车出行,倡导低碳生活 ,利用太阳能、风能等新型能源替代化石燃料,可以减少二氧化碳的排放,故选abc。
b/t mol L-1 min-1;②A 增大压强,反应速率加快、平衡正向移动,故A正确; b升高温度,平衡逆向移动,故b错误; c增大催化剂用量,平衡不移动,故c错误; d降低温度,反应速率减慢,故d错误。(2)①减少化石燃料的用量 ,鼓励乘坐公交车出行,倡导低碳生活 ,利用太阳能、风能等新型能源替代化石燃料,可以减少二氧化碳的排放,故选abc。
②a 2CO2(g)+2H2O(l) = C2H4(g)+3O2(g) △H=+1411.0kJ/mol
b 2CO2(g)+3H2O(l) = C2H5OH(l)+3O2(g) △H=+1366.8 kJ/mol
根据盖斯定律,b-a得C2H4(g)+H2O(l)=C2H5OH(l) △H =-44.2kJ/mol;
③i.温度一定时,提高碳氢比[n(H2)/n(CO2)],CO2的转化率增大;ii.升高温度,CO2的转化率减小,平衡逆向移动,正反应放热。iii. a极失电子发生氧化反应,电极反应式为C2H5OH - 12e-+16OH-==2CO32-+11H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】恒温恒容下,向2L密闭容器中加入MgSO4和CO(g),发生反应:
MgSO4(s)+CO(g)![]() MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是
A. 反应在0~2min内的平均速率为v(SO2)=0.6mol·L-1·min-1
B. 反应在2~4min内容器内气体的密度没有变化
C. 若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D. 保持其他条件不变,起始时向容器中充入1.00molMgSO4和1.00molCO,到达平衡时n(CO2)>0.60mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分散系的叙述不正确的是( )
A.分散系的分类: ![]()
B.用平行光照射FeCl3溶液和Fe(OH)3胶体,可以加以区分
C.如图显示的是树林的晨曦,该现象与丁达尔效应有关
D.在Fe(OH)3胶体中加入过量硫酸后会出现红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行Fe2+与Fe3+转化实验:向FeCl2溶液中加入少量KSCN溶液,溶液无明显变化,再加入少量双氧水,溶液变红,继续滴加至过量,发现溶液红色褪去,同时有气泡生成.他们针对此异常现象展开探究,请回答有关问题:
(1)该小组对于产生气体的原因有两种猜测:
猜测一:__________________________________________。
猜测二:红色褪去可能是SCN-被H2O2氧化,同时产生的气体中可能含有氮气、二氧化碳、二氧化硫。
(2)化学小组针对猜测二设计下面的实验来验证气体成分:
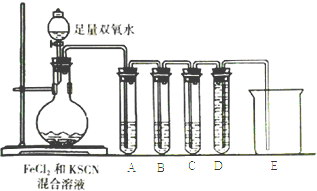
①试管A中盛放品红溶液,若实验中品红溶液褪色,证明气体中含有____________;
②试管B中的溶液是酸性高锰酸钾溶液,其目的是________________,预期试管B中的现象是________________________________。
③试管C中盛有澄清石灰水,目的是___________________;试管D和烧杯的作用是______________。④以上实验证明SCN-能被H2O2氧化.请写出该反应的离子方程式:___________________________________。
(3)根据题目信息及以上实验推断,Fe2+和SCN-中还原性较强的是_______,理由是_________。
(4)有人认为SCN-的氧化产物可能还有硫酸根离子,请设计一个简单实验证明该假设是否正确_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液溶质物质的量浓度为1 mol/L
C.0.5 L 2 molL﹣1的BaCl2溶液中,Ba2+和Cl﹣的总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 gcm﹣3)与10 mL18.4 molL﹣1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 常温下,23 g NO2含有NA个氧原子
B. 标准状况下,将22.4 L NO和11.2 L O2混合后,可以得到NA个NO2分子
C. 常温常压下,1 L 0. 1mol/L HF溶液中含有0.1NA个H+
D. 0.1 mol的羟基中含有电子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图中,甲烧杯中盛有100 mL 0.50 mol/L AgNO3溶液,乙烧杯中盛有100 mL 0.25 mol/L CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极增重2.7 g,则:

(1)E为电源的__________极,D为电解池的__________极。
(2)A极的电极反应式为__________________,析出物质______ mol。
(3)B极的电极反应式为__________________,析出气体__________ mL(标准状况)。
(4)C极的电极反应式为___________________,析出物质__________ mol。
(5)D极的电极反应式为__________________,析出气体_________ mL(标准状况)。
(6)甲烧杯中滴入石蕊试液,__________(选填“A”、“B”)极附近变红,如果继续电解,在甲烧杯中最终得到__________溶液(写溶质的化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com