
����Ŀ����ѡ��3:���ʽṹ�����ʡ�ͭԪ�ؿ��γɶ�����Ҫ������ش���������:
(1)ͭԪ��λ��Ԫ�����ڱ��е�_____��,���̬ԭ�ӵļ۵����Ų�ͼΪ_________��
(2)������ͭ��Һ�м��������ˮ,���γ�[Cu(NH3)4]SO4��Һ,����Һ�������ܽ���ά�ء�
��[Cu(NH3)4]SO4�������ӵ����幹����__________��
����[Cu(NH3)4]SO4��,Cu2+��NH3֮���γɵĻ�ѧ����Ϊ______���ṩ�µ��ӶԵijɼ�ԭ����_________��
�۳���Ԫ���⣬[Cu(NH3)4]SO4������Ԫ�صĵ縺����С�����˳��Ϊ________��
��NF3��NH3�Ŀռ乹����ͬ������ԭ�ӵĹ���ӻ����;�Ϊ_________����NF3������Cu2+�γɻ�ѧ������ԭ����_______________��
(3)һ��Hg-Ba-Cu-O���³������ϵľ���(������)��ͼ��ʾ��

�ٸ����ʵĻ�ѧʽΪ__________��
����֪�þ���������Ba2+�ļ��Ϊcpm.�����Ba2+�����Hg+��ĿΪ_____�������ߵ���̾���Ϊ_______pm��(�г�����ʽ���ɣ���ͬ)
��������ʵ�Ħ������ΪM,�����ӵ�������ֵΪNA����þ�����ܶ�Ϊ______g��cm-3��
���𰸡� ds ![]() �������� ��λ�� N Cu<H<N<O sp3 F�ĵ縺�Ա�N��,N-F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ,�����γ���λ������NF3������Cu2+�γ������� HgBa2CuO4 4
�������� ��λ�� N Cu<H<N<O sp3 F�ĵ縺�Ա�N��,N-F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ,�����γ���λ������NF3������Cu2+�γ������� HgBa2CuO4 4 ![]()
![]()
����������1��Cu��29��Ԫ�أ�ԭ�Ӻ��������Ϊ29��λ��Ԫ�����ڱ��е�ds����Cu��̬ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d104s1���۵����Ų�ʽΪ��3d104s1���۵����Ų�ͼΪ��![]() ��
��
�ʴ�Ϊ��ds��![]() ��
��
��2����SO42-��Sԭ�ӵŶԵ��Ӷ���=![]() ���۲���Ӷ���=4+0=4�����ӿռ乹��Ϊ�������塣
���۲���Ӷ���=4+0=4�����ӿռ乹��Ϊ�������塣
�ʴ�Ϊ������������
��Ni2+�ṩ�չ����NH3��Nԭ�Ӻ��йµ��Ӷԣ�����֮���γ���λ����
�ʴ�Ϊ����λ����N��
�۷ǽ�����Խǿ���縺��Խ��ͬ��������Ԫ�ش������ҵ縺����ǿ���ʵ縺��H��N��O��CuΪ����Ԫ�أ��������ӵ������dz������ʵ縺���������ʵ縺�Դ�С˳��Ϊ��Cu<H<N<O��
�ʴ�Ϊ��Cu<H<N<O��
��NH3��Nԭ���ӻ������Ϊ��5+3����2=4����ȡsp3�ӻ���ʽ��F�ĵ縺�Ա�N��,N-F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ,�����γ���λ������NF3������Cu2+�γ���������
�ʴ�Ϊ��sp3��F�ĵ縺�Ա�N��,N-F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ,�����γ���λ������NF3������Cu2+�γ���������
��3���ٸþ�����Baԭ�Ӹ���=2��Hgԭ�Ӹ���=8��![]() =1��Cuԭ�Ӹ���=4��
=1��Cuԭ�Ӹ���=4��![]() =1��Oԭ�ӵĸ���=8��
=1��Oԭ�ӵĸ���=8��![]() +4��
+4��![]() =4���ʻ�ѧʽΪHgBa2CuO4��
=4���ʻ�ѧʽΪHgBa2CuO4��
�ʴ�Ϊ��HgBa2CuO4��
�ڸ��ݾ����ṹͼ֪���������Ba2+Ϊ������Χ��������ҵȾ���ķֲ����µ����4�������ϣ����Ծ���Ba2+�����Hg+��ĿΪ4����Ba2+���µ������ĵľ���Ϊ![]() pm����Ba2+��Hg+����̾���Ϊx������x2=(
pm����Ba2+��Hg+����̾���Ϊx������x2=(![]() )2+��
)2+��![]() ��2�����x=
��2�����x=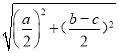 pm.
pm.
�ʴ�Ϊ�� 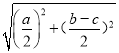 ��
��
�۸þ���������= ![]() �����=a2b pm3= a2b (10-10cm)3= a2b��10-30cm3�����Ըþ�����ܶ�=
�����=a2b pm3= a2b (10-10cm)3= a2b��10-30cm3�����Ըþ�����ܶ�=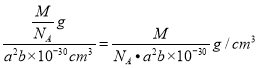 ��
��
�ʴ�Ϊ�� ![]() ��
��


 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д� С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦX(g)+3Y(g)![]() 2Z(g) ��H�������仯����ͼ��ʾ������˵����ȷ����
2Z(g) ��H�������仯����ͼ��ʾ������˵����ȷ����

A. ��H= E2- E1 B. ����������,E3����
C. ��ѹ�³���һ�����ĺ���n(Z)���� D. ѹ��������c(X)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������У����ǹ㷺�����Ż�ѧ��Ӧ�ͷŵ�����������˵����ȷ���ǣ�������
A.�������仯�Ķ��ǻ�ѧ�仯
B.���ʷ�����ѧ�仯����һ���������������仯
C.��ʵ�鷽�������۷����о���Ӧ�ȵĻ�ѧ��Ϊ�Ȼ�ѧ
D.�κη�Ӧ�е������仯������Ϊ�����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Te)Ϊ��VIAԪ�أ��䵥��ƾ�����������ܳ�Ϊ�����Ͻ����Ӽ����뵼�塢���Ԫ����������ϣ������㷺Ӧ����ұ�𡢺��պ��졢���ӵ����ɴӾ���ͭ��������(��Ҫ�ɷ�ΪCu2Te)�л����ڣ������������� :
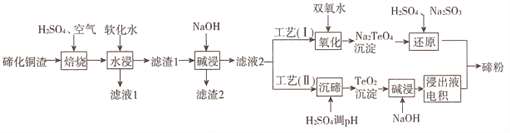
(1)�����ա���,����Ҫ��TeO2 ��ʽ����,д����Ӧ��Ӧ�Ļ�ѧ����ʽ:_____________��
(2)Ϊ��ѡ����ѵı��չ���,�������¶Ⱥ�������������������飬������±���ʾ:
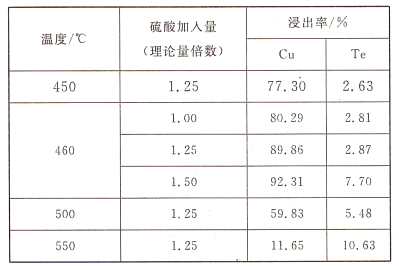
��ʵ����Ӧѡ�������Ϊ_______________��ԭ��Ϊ_______________��
(3)����( I)�У�����ԭ��ʱ�������ܵĻ�ѧ����ʽΪ_______________��
(4)���ڹ���(I)�С�����������Һ����������Ҫ��ߣ����о��߲��ù���(II)����ڡ�����������У������ĵ缫��ӦʽΪ_______________��
(5)��ҵ�����У�����2��������������Һ3������3��
����Һ3 ����Һ1�ϲ�������ͭ���ϵͳ���ô�����ʩ���ŵ�Ϊ________________��
������3������Au��Ag,����__________�����߷��롣(����ĸ)
A.��ˮ B.ϡ���� C.Ũ����������Һ D.Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�ⷴӦ���ӷ���ʽ��д��ȷ���ǣ�������
A.CH3COOH+OH��CH3COO��+H2O
B.S2��+2H2OH2S+2OH��
C.CH3COOH+H2OCH3COO��+H3O+
D.CO32��+H2OHCO3��+OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϊ16��7���������� SO2��CO ���Ӹ���֮��Ϊ����ԭ�Ӹ���֮��Ϊ��ͬ��ͬѹ�£���������SO2��CO�����Ϊ �� �ܶȱ�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����( )
A. ��ɢ����ֱ���Ĵ�С��ϵ����Һ�����壾��Һ
B. ���ö����ЧӦ����������Һ�뽺��
C. �������ӱȽ�С������ͨ����Ĥ
D. ��Ӿ�����֤���������ڵ������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ס��ҡ���������������ѧ��ѧ�г���������,��ת����ϵ��ͼ��ʾ����Ͷ���������
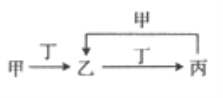
A. N2��O2 B. Cl2��Fe C. C��O2 D. SO2��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 L 1 mol��L��1 Na2SO4��Һ�У����и�����ȷ����
A��c(Na��)��1 mol��L��1 B��n(Na��)��3 mol
C��c(SO42-)��2 mol��L��1 D��m(Na2SO4)��142 g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com