
【题目】“纳米材料”是指粒子直径在几纳米到几十纳米的材料.若将“纳米材料”的粒子分散到液体分散剂中所得到的分散系是( )
A.溶液
B.胶体
C.悬浊液
D.乳浊液
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】对于反应:M+N﹣→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到30℃时,完成反应的10%需要的时间为( )
A.9 min
B.27 min
C.13.5 min
D.3 min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用固态不纯氯化钠(含少量NH4HCO3和Na2SO4杂质)制取纯净氯化钠溶液。下列操作可供选用:
①逐滴加入稀盐酸,调节pH值为5;
②煮沸;
③加蒸馏水溶解;
④加热至不再产生气体为止;
⑤加入稍过量的Na2CO3溶液;
⑥加入稍过量的BaCl2溶液;
⑦过滤。
上述实验操作的正确顺序应是
A.①②⑤⑥⑦③④ B.③④⑥⑤⑦①②
C.④③⑥⑤⑦①② D.④③⑤⑥⑦②①
【答案】C
【解析】
试题分析:NH4HCO3杂质可通过加热除去, Na2SO4杂质可通过BaCl2溶液除去,过量的BaCl2溶液可通过Na2CO3溶液除去,过量的Na2CO3溶液可通过滴加稀盐酸除去,答案选C。
考点:氯化钠的提纯
【题型】单选题
【结束】
22
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A. 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.2NA
B. 标准状况下11.2L二氧化硫中含有的原于数为2NA
C. 标准状况下,22.4L氯气发生反应转移电子数一定为2NA
D. 0.1mol/LCuCl2溶液中Cl-数目是0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,可以用铁或铝制的容器贮存浓硫酸,下列叙述中,错误的是
A.浓硫酸具有强还原性
B.贮存浓硫酸的容器要密封,因为浓硫酸容易吸收空气中的水蒸气
C.浓硫酸可以使硫酸铜晶体由蓝色变为白色
D.常温下,浓硫酸可以使铁或铝钝化,生成一层致密的氧化膜,阻止反应继续进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒容密闭容器中充入1mol CO2和3mol H2 , 一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.下列说法正确的是( )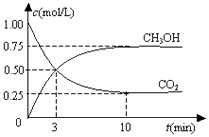
A.反应进行到3 min时,该反应达到平衡状态
B.从反应开始到平衡,CO2的转化率为25%
C.第3 min时,氢气的平均反应速率为1.5mol/(L?min)
D.该温度下,反应的平衡常数的值为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,硝酸只表现氧化性的是( )
A.3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
B.C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
C.Al(OH)3+3HNO3═Al(NO3)3+3H2O
D.3Zn+8HNO3═3Zn(NO3)2+2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将11.2LCO2缓缓通入300mL2mol·L-1的NaOH溶液中,待充分反应后将所得溶液蒸干并充分灼烧,最后所得固体物质的质量为
A. 31.8g B. 53g C. 63.6g D. 84g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》中记载“烧酒非古法也,自元时始创其法。用浓酒和糟入甑,蒸令气上,用器承取其露。”这里用到的方法可用于分离( )
A.碳酸钙和硝酸钾B.碘单质和氯化钠C.四氯化碳和水D.乙醇和乙酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com